По периоду для кислородосодержащих кислот слева направо возрастает сила кислот.
Так, 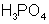 более сильная, чем
более сильная, чем 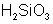 ; в свою очередь,
; в свою очередь,  более сильная, чем
более сильная, чем 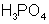 .
.
По группе кислородосодержащих кислот сверху вниз сила кислот уменьшается. Так угольная  более сильная, чем кремниевая
более сильная, чем кремниевая 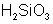
Чем выше степень окисления кислотообразующего элемента, тем сильнее кислота:
 ,серная кислота сильнее, чем сернистая.
,серная кислота сильнее, чем сернистая.
Сила бескислородных кислот в главных подгруппах с ростом атомного номера элемента возрастает:
 ,
,

 СИЛА КИСЛОТ РАСТЕТ
СИЛА КИСЛОТ РАСТЕТ
По периоду слева направо сила бескислородных кислот возрастает. Так  более сильная кислота, чем
более сильная кислота, чем  , а
, а  – чем
– чем  .
.
61.p-Элементы с водородом образуют соединения с ковалентно-полярными связями.
Степень полярности связи легко оценить по разности электроотрицательностей элементов (ΔЭО). Так, для B, C, P, Si, Ge, As, Sn, Sb связь в соединениях с водородом практически ковалентная.
Из рассмотрения изменения в группах и периодах электроотрицательности соответствующих p-элементов и радиусов их атомов (ионов) можно сделать следующее обобщение: в пределах каждой подгруппы элементов обычно уменьшается прочность водородных соединений; в пределах каждого периода возрастает их кислотность. Валентный угол в группе с ростом Z уменьшается (табл. 8.6). Это объясняется ослаблением способности валентных орбиталей элементов к sp3-гибридизации из-за увеличения разности энергии s- и p-подуровней.
Кроме общих закономерностей водородные соединения p-элементов обнаруживают аномалию в проявлении некоторых свойств, в частности, в температурах кипения (рис. 8.6) и плавления.
Обычно с увеличением молекулярной массы температуры кипения и плавления соединений увеличиваются. Ожидаемый ход кривой наблюдается только для водородных соединений IVА группы (CH4, SiH4, CeH4, SnH4), в трех других рассмотренных группах обнаруживаются аномально высокие точки кипения для NH3, H2O, NF. Это объясняется образованием из молекул этих веществ ассоциатов –H–F...H–F... за счет водородной связи *). Интересно отметить, что наиболее прочной является водородная связь между молекулами HF, т. к. фтор – наиболее электроотрицательный элемент, однако, как видно из рис. 8.6, самая высокая температура кипения у воды. Объясняется это тем, что каждая молекула воды может образовать две водородные связи, тогда как молекула фтористого водорода – только одну.
Среди водородных соединений p-элементов особое место принадлежит соединениям бора (бороводородам, боранам) B2H6, B4H10, B6H10, B5H11 и др. Они интересны тем, что относятся к электронодефицитным соединениям – число электронов в этих соединениях меньше, чем требуется для образования двухэлектронных двухцентровых связей. В диборане B2H6 двенадцать валентных электронов участвуют в восьми связях. В двух концевых группах BH2, которые лежат в одной плоскости, атомы бора и водорода связаны двухцентровыми двухэлектронными связями. Два же центральных атома водорода расположены симметрично над этой плоскостью и под нею и объединены с атомами бора трехцентровыми мостиковыми связями (рис. 8.7а), хорошо описываемыми с позиций ММО. На рис. 8.7б изображена схема трехцентровых МО диборана (фрагмент В–Н–В). Здесь две атомные sp3-гибридные орбитали бора (по одной от каждого атома) с одним электроном перекрываются с 1s-орбиталью атома водорода, которая дает еще один электрон, образуя связывающую, несвязывающую и разрыхляющую электронные орбитали. Пара электронов занимает связывающую орбиталь, что обеспечивает устойчивость этих мостиковых связей в молекуле B2H6.



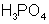 более сильная, чем
более сильная, чем 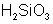 ; в свою очередь,
; в свою очередь,  более сильная, чем
более сильная, чем  более сильная, чем кремниевая
более сильная, чем кремниевая  ,серная кислота сильнее, чем сернистая.
,серная кислота сильнее, чем сернистая. ,
,
 СИЛА КИСЛОТ РАСТЕТ
СИЛА КИСЛОТ РАСТЕТ более сильная кислота, чем
более сильная кислота, чем  , а
, а  – чем
– чем  .
.


