И так без допольнительных затрат энергии все процессы идут в сторону возвратать энтальпию

Методами статичтическими оказались возмоно получить соотношение между Энтрорией и вероятрности находящии системы в данном состоянии
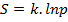
Где p: вероятность состояния
S: Энтропия системы
k: постоянно = 13,8.10-23 Дж/К
Таким образом, что энтропия есть мера вероятности данного состояния системы. Процессы в макросколическом изолированом системы протекают в направление от состояния с меньщей вероятности к состоянию с больщей вероятности.
28) Понятие эффективного диамегра молекулы и эффективного сечения
столкновения. Число столкновений одной молекулы газа в единицу времени. Средняя длина свободного пробега молекулы и ее зависимость от давления и температуры.
Эффективный диаметр – среднее расстояние между центрами молекул, на которое две молекулы сближаются при их столкновении. Площадь поперечного сечения «коридора», в который должны попасть центры соседних молекул, чтобы столкнуться с данной называется эффективным сечением столкновения:

Число столкновения молекул за единицу времени: 

Средняя длина свободного пробега молекулы – расстояние, которое она пролетает между двумя последовательными соударениями:

С учетом движения всех молекул, заменяя среднюю скорость на относительную скорость движения молекул:
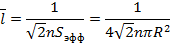
Так как p = nkT, то

29) Явления переноса в газах. Опытные законы диффузии, теплопроводности и
вязкости. Качественное и количественное описание этих процессов в молекулярно -
кинетической теории газов.
Явления, происходящие при нарушении равновесного состояния систем, назывеются явлениями переноса (например, столкновения молекул, диффузия, теплопроводность, вязкость).
Неравновесный процесс, вызываемый молекулярным тепловым движением и приводящий к установлению равновесного распределения концентраций путем взаимопроникновения и перемешивания молекул, наз. диффузией.
Диффузия – это перенос массы.
Назовем плотностью потока молекул их число, проходящее через единичное сечение, расположенное перпендикулярно вектору скорости, за единицу времени:

Коэффициент диффузии:

Закон диффузии (закон Фика):

Плотность диффузионного потока частиц пропорциональная градиенту концентрации частиц. При диффузии поток частиц направлен в сторону их концентрации (смысл знака «-»).
Молекулярный перенос теплоты в сплошной среде, обусловленный наличием градиента температуры, называется теплопроводностью.
Плотность теплового потока (количество теплоты, проходящее через единичную поверхность за единицу времени):

Плотность потока частиц: 
Коэффициент теплопроводности:

Закон теплопроводности (закон Фурье):  - плотность теплового потока при теплопроводности пропорциональна градиенту температуры в системе.
- плотность теплового потока при теплопроводности пропорциональна градиенту температуры в системе.
Свойство жидкостей и газов, характеризующее сопротивление действию внешних сил, вызывающих их течение, наз. вязкостью (внутренним трением). Можно рассматривать вязкость как перенос импульса.
Плотность потока импульса:

Коэффициент динамической вязкости:

Закон внутреннего трения (закон Пуазейля):

Плотность потока импульса молекул, переносимого в каком-то направлении, прямо пропорциональна градиенту скорости частиц в этом направлении.
30) Барометрическая формула. Распределение Вольцмана.

Больцман получил барометрическую формулу – зависимость давления газа от высоты в потенциальном поле тяжести Земли.
Рассмотрим равновесие некоторого объема (цилиндр высотой dh) газа, находящегося на высоте h от поверхности Земли, уровень которой выберем за условный ноль отсчета потенциальной энергии. Так как столбик газа находится в равновесии:
Энергия движения молекулы определяется, в свою очередь, энергией ее поступательного движения, энергией ее вращения и энергией колебания атомов в молекуле:

Минимальное число независимых переменных, однозначно определяющих положение тела в пространстве (или минимальное число независимых перемещений тела в пространстве) наз. числом степеней свободы (i) тела. Для одноатомной молекулы i = 3
Закон Больцмана о равномерном распределении энергии молекул по степеням свободы: если система молекул находится в тепловом равновесии при температуре Т, то средняя кинетическая энергия молекул равномерно распределена по степеням свободы, причем на каждую степень свободы приходится энергия 
31) Функция распределения и ее смысл. Распределение молекул газа по модулю
скорости (распределение Максвелла по модулю скорости). Наиболее вероятная, средняя и средняя квадратичная скорости молекулы. Зависимость функции распределения от температуры.




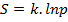




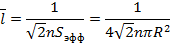







 - плотность теплового потока при теплопроводности пропорциональна градиенту температуры в системе.
- плотность теплового потока при теплопроводности пропорциональна градиенту температуры в системе.








