МАГНИЙ Исп. образец растворяют в воде, + р-р аммиака разведенного  образуется белый осадок, растворяющийся при прибавлении р-ра аммония хлорида. + р-р динатрия гидрофосфата
образуется белый осадок, растворяющийся при прибавлении р-ра аммония хлорида. + р-р динатрия гидрофосфата  образуется белый кристаллический осадок. Mg2+ + HPO42- + NH3 → NH4MgPO4↓
образуется белый кристаллический осадок. Mg2+ + HPO42- + NH3 → NH4MgPO4↓
НАТРИЙ а) Исп. образец растворяют в воде, + р-р калия карбоната и нагревают до кипения; осадок не образуется. + р-р калия пироантимоната и нагревают до кипения, затем охлаждают в ледяной воде и потирают внутренние стенки пробирки стеклянной палочкой  образуется осадок белого цвета.
образуется осадок белого цвета.

b) Исп. образец растворяют воде + метоксифенилуксусной к-ты реактива, охлаждают в ледяной воде  образуется объемный белый кристалл. осадок. Смесь помещают в воду при t= 20°С и перемешивают; осадок не исчезает. + р-р аммиака разведенного; осадок полностью растворяется. + р-р аммония карбоната; осадок не образуется.
образуется объемный белый кристалл. осадок. Смесь помещают в воду при t= 20°С и перемешивают; осадок не исчезает. + р-р аммиака разведенного; осадок полностью растворяется. + р-р аммония карбоната; осадок не образуется.

с) Соль натрия, смоченная кислотой хлористоводородной и внесенная в бесцветное пламя, окрашивает его в желтый цвет.
РТУТЬ а) Р-р исп. образца помещают на тщательно очищенную поверхность медной фольги; появляется темно-серое пятно, которое при натирании становится блестящим. Фольгу высушивают и нагревают в пробирке; пятно исчезает. b) К исп. р-ру+ р-р натрия гидроксида разведенный до сильнощелочной среды  образуется плотный осадок желтого цвета: Hg22+ + 2ОН− = Hg2O ↓ + Н2O. с) К р-ру исп. образца + осторожно по каплям р-р калия йодидa
образуется плотный осадок желтого цвета: Hg22+ + 2ОН− = Hg2O ↓ + Н2O. с) К р-ру исп. образца + осторожно по каплям р-р калия йодидa  образуется красный осадок, растворимый в избытке этого реактива: Hg22++2KI = Hg2I2↓ 2K+,
образуется красный осадок, растворимый в избытке этого реактива: Hg22++2KI = Hg2I2↓ 2K+,
СВИНЕЦ а) Исп. образец растворяют в к-те уксусной + р-р калия хромата  образуется желтый осадок, растворяющийся при прибавлении р-ра натрия гидроксида концентрированного: Pb2+ + CrO42-→ PbCrO4↓ b) Исп. образец растворяют в кислоте уксусной + воду и р-р калия йодида
образуется желтый осадок, растворяющийся при прибавлении р-ра натрия гидроксида концентрированного: Pb2+ + CrO42-→ PbCrO4↓ b) Исп. образец растворяют в кислоте уксусной + воду и р-р калия йодида  образуется желтый осадок. При кипячении осадок растворяется При охлаждении образуется осадок в виде блестящих желтых пластинок: Pb2+ + 2 I− → PbI2↓
образуется желтый осадок. При кипячении осадок растворяется При охлаждении образуется осадок в виде блестящих желтых пластинок: Pb2+ + 2 I− → PbI2↓
СЕРЕБРО а) Исп. образец растворяют в водt + HCl  образуется белый творожистый осадок, растворяющийся при прибавлении р-ра аммиака разведенного: Ag+ + Cl− → AgCl↓ b) К р-ру исп. образца + р-р аммиака разведенного до растворения образующегося вначале осадка, + р-р формальдегида и нагревают; на стенках пробирки образуется блестящий налет металлического серебра: AgCl↓ + 2NH3 → [Ag(NH3)2]+ + Cl−,
образуется белый творожистый осадок, растворяющийся при прибавлении р-ра аммиака разведенного: Ag+ + Cl− → AgCl↓ b) К р-ру исп. образца + р-р аммиака разведенного до растворения образующегося вначале осадка, + р-р формальдегида и нагревают; на стенках пробирки образуется блестящий налет металлического серебра: AgCl↓ + 2NH3 → [Ag(NH3)2]+ + Cl−,
2[Ag(NH3)2]++HCHO + 2H2O → 2Ag↓ + 2NH4+ + HCOONH4 + NH3∙H2O
СУРЬМА Исп. образец растворяют при нагревании в водном р-ре калия-натрия тартрата и охлаждают. + р-р натрия сульфида  образуется оранжево-красный осадок, растворяющийся при прибавлении р-ра натрия гидроксида разведенного: 3S2− + 2 Sb3+ → Sb2S3↓
образуется оранжево-красный осадок, растворяющийся при прибавлении р-ра натрия гидроксида разведенного: 3S2− + 2 Sb3+ → Sb2S3↓
ЦИНК а) Исп. образец растворяют в воде + р-р NaOH конц.  образуется белый осадок. + изб. р-ра NaOH конц. осадок растворяется. + р-р аммония хлорида; раствор остается прозрачным. К р-ру прибавляют р-р натрия сульфида
образуется белый осадок. + изб. р-ра NaOH конц. осадок растворяется. + р-р аммония хлорида; раствор остается прозрачным. К р-ру прибавляют р-р натрия сульфида  образуется белый хлопьевидный осадок: Zn2+ + Na2S→ZnS↓+ 2Na+
образуется белый хлопьевидный осадок: Zn2+ + Na2S→ZnS↓+ 2Na+
b) К исп. р-ру+ р-р калия ферроцианида 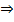 образуется белый осадок, нерастворимый в HCl разведенной: Zn2++ K4[Fe(CN)6] →ZnK2[Fe(CN)6] ↓+ 2K+.
образуется белый осадок, нерастворимый в HCl разведенной: Zn2++ K4[Fe(CN)6] →ZnK2[Fe(CN)6] ↓+ 2K+.



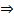 образуется белый осадок, растворяющийся при прибавлении р-ра аммония хлорида. + р-р динатрия гидрофосфата
образуется белый осадок, растворяющийся при прибавлении р-ра аммония хлорида. + р-р динатрия гидрофосфата 
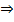 образуется объемный белый кристалл. осадок. Смесь помещают в воду при t= 20°С и перемешивают; осадок не исчезает. + р-р аммиака разведенного; осадок полностью растворяется. + р-р аммония карбоната; осадок не образуется.
образуется объемный белый кристалл. осадок. Смесь помещают в воду при t= 20°С и перемешивают; осадок не исчезает. + р-р аммиака разведенного; осадок полностью растворяется. + р-р аммония карбоната; осадок не образуется.



