Алканолы являются полярными соединениями; содержат две полярные связи

Диполи связей направлены в сторону атома кислорода.
Суммарный дипольный момент составляет 1,6 – 1,8D.
μ (С – О) ~ 0,9D; μ (О – Н) ~1,5D
Неподеленные пары электронов придают алканолам слабые электронодонорные свойства

Полярность связи О – Н и неподеленные электронные пары определяют возможность молекулярной ассоциации

Из-за наличия межмолекулярных водородных связей простейшие спирты (до С3) хорошо растворимы в воде.
С увеличением углеводородного радикала растворимость в воде уменьшается, возрастает гидрофобность молекулы и повышается липидная растворимость.
В связи с этим температуры кипения и плавления у спиртов выше, чем у соответствующих углеводородов и галогенпроизводных.
В полиолах наличие нескольких ОН-групп приводит к увеличению числа межмолекулярных водородных связей, оказывающих влияние на физ. св-ва. Полиолы существуют в виде ассоциатов полимерного характера

Такое межмолекулярное связывание ведет к заметному увеличению вязкости и темп-ры кипения полиолов.
В рез-те низшие полиолы – вязкие высококипящие жидкости с относительной плотностью несколько больше 1 (плотность глицерина 1,260).
Способность этилового спирта к образованию водородных связей лежит в основе его антисептических свойств.
Рентгено- и электронографические данные
 l (C-C) = 0,154 нм;
l (C-C) = 0,154 нм;
l (С-О) = 0,144 нм;
l (О-Н) = 0,097 нм
Химические свойства
Спирты обладают разнообразной реакционной способностью:

І. Кислотно-основные свойства.
Одноатомные спирты – очень слабые кислоты; содержание протонов в их водных растворах практические не меняется. Только в концентрированных спиртовых растворах щелочей происходит незначительная ионизация спиртов:

Разрыв связи О-Н происходит под действием активных Ме, их гидридов или амидов с образованием солей


Алкоголяты металлов – бесцветные твердые вещества, легко гидролизуются водой.
Легкость образования алкоголятов зависит от кислотности спиртов:
Чем выше кислотность, тем легче образуется алкоголят. В жидкой фазе ряд собственной кислотности обращается
СН3ОН > первичные > вторичные > третичные
Определяющим фактором стабилизации алкооксид-иона является эффект сольватации. Влияние заместителей на кислотные свойства подчиняются общим правилам:
ЭА стабилизируют анионы и повышают кислотность;
ЭД дестабилизируют анионы и понижают кислотность:

Полиолы способны взаимодействовать с акт. Ме и обратимо с безводными щелочами:

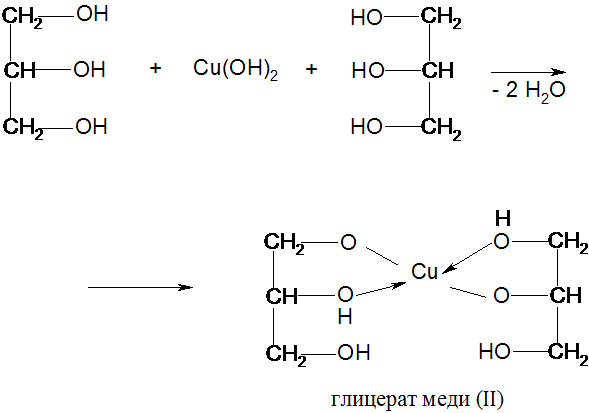
Многоатомные спирты как более сильные кислоты способны образовывать устойчивые комплексы – хелаты, реагируют с гидроксидами d-Ме в щелочной среде (качествен. р-ция):









 l (C-C) = 0,154 нм;
l (C-C) = 0,154 нм;











