Электролиты - это вещества, которые проводят электрический ток, в следствии диссоциации на ионы, которая проходит в растворах или расплавах.
К электролитам относится большинство кислот, оснований и солей. Попав в полярный растворитель они диссоциируют на ионы, это вызывает взаимодействие ионов вещества, молекул растворителя. И после этого это считается электролитом, и может проводить электрический ток.
Сильные электролиты это вещества, которые при растворении в воде практически полностью распадаются на ионы. Как правило, к сильным электролитам относятся вещества с ионными или сильно полярными связями: все хорошо растворимые соли, сильные кислоты (HCl, HBr, HI, HClO4, H2SO4,HNO3) и сильные основания (LiOH, NaOH, KOH, RbOH, CsOH, Ba(OH)2,Sr(OH)2,Ca(OH)2).
Слабые электролиты - вещества, частично диссоциирующие на ионы. Растворы слабых электролитов наряду с ионами содержат недиссоциированные молекулы. Слабые электролиты не могут дать большой концентрации ионов в растворе.
К слабым электролитам относятся:
1) почти все органические кислоты (CH3COOH, C2H5COOH и др.);
2) некоторые неорганические кислоты (H2CO3, H2S и др.);
3) почти все малорастворимые в воде соли, основания и гидроксид аммония (Ca3(PO4)2; Cu(OH)2; Al(OH)3; NH4OH);
4) вода.
Они плохо (или почти не проводят) электрический ток.
--------------------------------------------------------------------------------------------------------------------------
1) Превращения энергии в химических реакциях
При химических реакциях происходит освобождение части энергии, содержащейся в веществах, это носит название теплового эффекта реакции, по которому можно судить об изменении количества внутренней энергии вещества.
У ряда химических реакций можно наблюдать поглощение или выделение лучистой энергии.
В химических реакциях, протекающих с взрывом, внутренняя энергия превращается в механическую, причем частично сразу, частично переходя изначально в теплоту.
Во время химических реакций происходит взаимное превращение энергий – внутренней энергии веществ в тепловую, лучистую, электрическую и механическую, и наоборот.
Экзотермические химические реакции характеризуются выделением энергии во внешнюю среду. Эндотермические – поглощением энергии.
Выделяющиеся при химических реакциях энергия может быть превращена в другие виды энергии. Так, например, при сжигании топлива в соответствующих устройствах выделяющаяся энергия превращается в электрическую и т. д. При этом все эти процессы протекают в соответствии с законом сохранения и превращения энергии.
2) Понятие гидротация
Гидратация в растворах — процесс присоединения молекул воды к молекулам или ионам растворенного вещества.
Понятие «гидратация» относится к водным растворам;
Процесс, обратный гидратации, называют дегидратацией.
Гидратация является важным условием растворения веществ и устойчивости их в растворе, в частности стабильности растворов белковых и других биополимеров.
Степень гидратации различных ионов и молекул неодинакова и зависит от размеров частиц и величины их заряда. Чем больше заряд и меньше размеры иона, то есть выше удельная плотность заряда, тем больше степень гидратации. Ион L+ гидратирован больше, так как удельная плотность заряда у него выше, чем у ионов К+
ГИДРАТАЦИЯ- присоединение воды к молекулам, атомам или ионам. Может осуществляться без разрушения или с разрушением молекул воды. Г. без разрушения молекул воды приводит к гидратам
3) Na2S + HCl
Na2S+2HCl = 2NaCl + H2S (cероводородная к-та) - реакция обмена
Na2S + 2HCl(разб.) = 2NaCl + H2S
2Na(+)+S(-2) + 2H(+)+2Cl(-)(разб.) = 2Na(+)+Cl (-)+ 2H(+)+S(-2)
--------------------------------------------------------------------------------------------------------------------------
1.овр
2. закон разбавления оствальда
3. реакция гидролиза
--------------------------------------------------------------------------------------------------------------------------
1)Энергия Гиббса, её связь с константой равновесия
Величина изменения свободной энергии Гиббса складывается из энтальпийной составляющей DН и энтропийной составляющей ТDS. Каждая из этих величин отражает влияние определенного фактора на возможность самопроизвольного протекания реакции.
Классическим определением энергии Гиббса является выражение

где  — внутренняя энергия,
— внутренняя энергия,  — давление,
— давление, 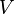 — объём,
— объём,  — абсолютная температура,
— абсолютная температура,  — энтропия.
— энтропия.
Энергия Гиббса — это величина, показывающая изменение энергии в ходе химической реакции и дающая таким образом ответ на вопрос о принципиальной возможности протекания химической реакции;
В химических процессах одновременно действуют два противоположных фактора — энтропийный ( ) и энтальпийный (
) и энтальпийный (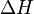 ). Суммарный эффект этих противоположных факторов в процессах, протекающих при постоянном давлении и температуре, определяет изменение энергии Гиббса (
). Суммарный эффект этих противоположных факторов в процессах, протекающих при постоянном давлении и температуре, определяет изменение энергии Гиббса ( ):
):

Между стандартным изменением энергии Гиббса и константой равновесия существует непосредственная связь
При равновесии изменение энергии Гиббса равно нулю. Если Δ G < 0, то реакция должна протекать в сторону образования соединения D, а если Δ G > 0, то будет происходить его диссоциация.
Существует полезное соотношение, связывающее изменение свободной энергии Гиббса 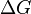 в ходе химической реакции с её константой равновесия
в ходе химической реакции с её константой равновесия  :
:

где Кр - равновесная константа по давлению (только в атмосферах),
Вообще говоря, любая реакция может быть рассмотрена как обратимая (даже если на практике она таковой не является). При этом константа равновесия определяется как

где  — константа скорости прямой реакции,
— константа скорости прямой реакции,  — константа скорости обратной реакции.
— константа скорости обратной реакции.
2)Основные классы неорганических соединений

Основные классы неорганических соединений.
Оксиды – соединения элемента с кислородом.
Оксиды не образующие кислот, оснований и солей при обычных условиях, называются не солеобразующими.
Солеобразующие оксиды подразделяются на кислотные, основные и амфотерные (обладающие двойственными свойствами). Неметаллы образуют только кислотные оксиды, металлы – все остальные и некоторые кислотные.
Основания – сложные вещества, молекулы которых состоят из атома металла и одной или нескольких гидроксогрупп, способных замещаться на кислотный остаток.
Кислоты – сложные вещества, содержащие атомы водорода, которые могут замещаться катионами металла (или ионами аммония).
Соли – продукты замещения (полного или частичного) атомов водорода в молекулах кислот катионами металла (а также ионами аммония), либо гидроксогрупп в молекулах оснований кислотными остатками.
Соли делятся на средние, кислые, основные, двойные, смешанные и комплексные.
K2Cr2O7+14HCl=2KCl+2CrCl3+7H2O+3Cl2
KMnO4+MnCl2= гидролиз
MnCl2+2KMnO4+H20=MnO2+2KCl+H2O




 — внутренняя энергия,
— внутренняя энергия,  — давление,
— давление, 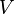 — объём,
— объём,  — абсолютная температура,
— абсолютная температура,  — энтропия.
— энтропия. ) и энтальпийный (
) и энтальпийный (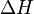 ). Суммарный эффект этих противоположных факторов в процессах, протекающих при постоянном давлении и температуре, определяет изменение энергии Гиббса (
). Суммарный эффект этих противоположных факторов в процессах, протекающих при постоянном давлении и температуре, определяет изменение энергии Гиббса ( ):
):
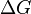 в ходе химической реакции с её константой равновесия
в ходе химической реакции с её константой равновесия  :
:

 — константа скорости прямой реакции,
— константа скорости прямой реакции,  — константа скорости обратной реакции.
— константа скорости обратной реакции.


