Изменение энергии в химической реакции в каком-либо направлении определяется изменением энергии Гиббса
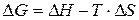 , D G < 0 (4)
, D G < 0 (4)
Изменение стандартной свободной энергии Гиббса связано со стандартной разностью потенциалов следующим уравнением:
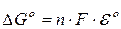 , DG < 0 (5)
, DG < 0 (5)
Стандартная разность потенциалов (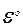 ) в равновесном процессе (сила тока I = 0) будет максимальной. Ее называют электродвижущей силой (ЭДС). Приравняв правые части уравнений (4) и (5) (уравнение (6)) можно определить электродвижущую силу (
) в равновесном процессе (сила тока I = 0) будет максимальной. Ее называют электродвижущей силой (ЭДС). Приравняв правые части уравнений (4) и (5) (уравнение (6)) можно определить электродвижущую силу (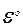 ) в равновесных условиях (уравнение (7))
) в равновесных условиях (уравнение (7))
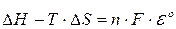 , (6)
, (6)
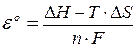 . (7)
. (7)
Из этого уравнения можно сделать вывод о том, что любой самопроизвольно развивающийся окислительно-восстановительный процесс, для которого D G < 0, может быть источником электрической энергии.
Термодинамические функции, в том числе и D Gо, позволяют рассчитать с определенной степенью точности e о, или ЭДС, для окислительно-восстановительных процессов, являющихся источниками электрической энергии. Но отдельные потенциалы электродов они определить не могут, так как ЭДС представляет собой разность потенциалов
e 0 = j 0к – j 0а, (8)
где j 0к – стандартный потенциал катода, В;
j 0а – стандартный потенциал анода, В.
Для измерения потенциала какого-либо электрода собирают гальванический элемент, состоящий из стандартного водородного электрода (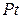 ,
, 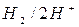 ) и исследуемого металлического электрода (
) и исследуемого металлического электрода (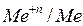 ). Каждый электрод называется полуэлементом. Объединяем два полуэлемента и получаем схему гальванического элемента
). Каждый электрод называется полуэлементом. Объединяем два полуэлемента и получаем схему гальванического элемента
 .
. 
Одна черта показывает границу между жидкой и твердой фазами, две черты – между жидкими фазами.
Электродвижущая сила такого элемента равна величине потенциала исследуемого электрода
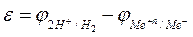 (9)
(9)
Знак электродного потенциала определяется направлением тока при замыкании цепи. Если электроны текут по металлическому проводнику от изучаемого электрода к водородному, то его потенциал отрицательнее, чем у стандартного водородного электрода


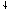


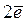
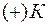

 .
.
Анодом является цинковый электрод, а катодом – водородный электрод.
Если электроны проходят по проводнику от водородного электрода к исследуемому, то потенциал изучаемого электрода положительнее, чем у стандартного водородного электрода






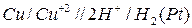
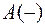 .
.
Анодом в этом случае является водородный электрод, а катодом - медный электрод.
Бекетов расположил металлы в определенной последовательности изменения электродных потенциалов. В начале ряда находятся металлы с наиболее отрицательным потенциалом, обладающие значительными восстановительными свойствами, а в конце ряда – металлы с наиболее положительным потенциалом, являющиеся сильными окислителями. Такой ряд стандартных (или нормальных)потенциалов металлов назван рядом напряжения Бекетова.
В любой электрохимической системе, в том числе в гальваническом элементе, на катоде происходит восстановление, а на аноде – окисление. Например, в гальваническом элементе Даниэля-Якоби
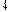




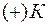
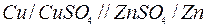


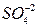
проходят следующие процессы:
анодный процесс окисления цинка  ;
;
катодный процесс восстановления ионов меди Cu +2 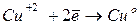 ;
;
cуммарный процесс:  .
.
ЭДС этого элемента  = +0,34 – (-0,76) = 1,1 В.
= +0,34 – (-0,76) = 1,1 В.
Электродный потенциал можно измерить, используя не только водородный электрод, но и любой другой электрод сравнения, например, каломельный электрод, хингидронный электрод и другие.
Особенность электродов сравнения состоит в том, что потенциал этого электрода очень мало меняется со временем, и можно с некоторым приближением считать, что он остается неизменным. Например, потенциал каломельного электрода  меняется незначительно (в диапазоне температур 293-323 К – от 0,2471 до 0,2438 В).
меняется незначительно (в диапазоне температур 293-323 К – от 0,2471 до 0,2438 В).
Например, в лесосушильных камерах необходимо измерить потенциал нержавеющей стали, которой обшиты стены и потолок камеры. Потенциал несет информацию о протекающих процессах на сплаве и о стойкости сплава в агрессивной кислой среде лесосушильных камер. Степень кислотности среды взависимости от применяемых режимов сушки, породы и начальной влажности высушиваемой древесины изменяется от рН 3,4 до рН 4,2. Среда включает уксусную кислоту, которая скапливается на стенках в виде конденсационной влаги. Для измерения потенциала используют каломельный электрод сравнения и составляют следующую схему:



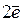

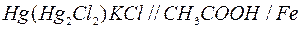
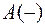 .
.
(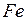 - основной компонент стали)
- основной компонент стали)
Показания ЭДС гальванического элемента (рис. 3) определяютпо вольтметру (V).

Рис. 3. Схема гальванического элемента для измерения потенциала металла



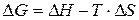 , D G < 0 (4)
, D G < 0 (4)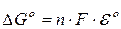 , DG < 0 (5)
, DG < 0 (5)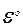 ) в равновесном процессе (сила тока I = 0) будет максимальной. Ее называют электродвижущей силой (ЭДС). Приравняв правые части уравнений (4) и (5) (уравнение (6)) можно определить электродвижущую силу (
) в равновесном процессе (сила тока I = 0) будет максимальной. Ее называют электродвижущей силой (ЭДС). Приравняв правые части уравнений (4) и (5) (уравнение (6)) можно определить электродвижущую силу (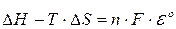 , (6)
, (6)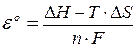 . (7)
. (7)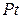 ,
, 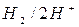 ) и исследуемого металлического электрода (
) и исследуемого металлического электрода (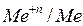 ). Каждый электрод называется полуэлементом. Объединяем два полуэлемента и получаем схему гальванического элемента
). Каждый электрод называется полуэлементом. Объединяем два полуэлемента и получаем схему гальванического элемента .
. 
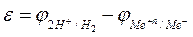 (9)
(9)

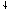


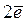
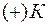

 .
.





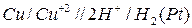
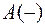 .
.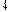


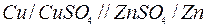

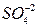
 ;
;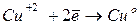 ;
; .
. = +0,34 – (-0,76) = 1,1 В.
= +0,34 – (-0,76) = 1,1 В. меняется незначительно (в диапазоне температур 293-323 К – от 0,2471 до 0,2438 В).
меняется незначительно (в диапазоне температур 293-323 К – от 0,2471 до 0,2438 В).

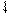

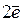

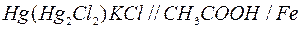
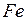 - основной компонент стали)
- основной компонент стали)


