Дмитрий Иванович Менделеев, великий русский химик, в 1869г. сформулировал периодический закон на основе блестящего теоретического анализа огромного числа экспериментальных данных и предсказал на его основе существование и свойства элементов, которые вскоре были обнаружены экспериментально. Правильность закона была подтверждена. Но сам Д.И. Менделеев предполагал, что причина изменяемости свойств элементов кроется в «основных началах внутренней механики атомов». Строение атомов еще не было известно.
Современная формулировка Периодического закона строится на основе строения атома: свойства химических элементов и образуемых ими простых и сложных веществ находятся в периодической зависимости от заряда ядра этих элементов. Периодическая система по сути является графическим отображением периодического закона
На основе современной формулировки периодического закона и с использованием периодической системы можно определить строение атома любого химического элемента, класс элемента, предсказать свойства простого вещества, образованного этим элементом, а также состав и свойства соединений этого элемента. Периодический закон и периодическая система – это основа основ химии как науки и одновременно универсальный справочник, в котором можно найти ответы на множество простых и сложных вопросов. Периодическая система состоит из семи периодов (строк) и восьми групп (столбцов). Положение элементов в периодической системе определяется строением их атомов.
Для четкого понимания периодического закона и для умения пользоваться периодической системой необходимо иметь представление о строении атома.
 Атом
Атом
– это электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов.
Различные виды атомов названы химическими элементами. Строение и свойства атомов зависят от заряда ядра.
Химический элемент
– это вид атомов с одинаковым зарядом ядра.
Ядро атома
 – часть атома, находящаяся в его центре и заряженная положительно; в ядре сосредоточена основная масса атома. Ядро состоит из нуклонов (протонов и нейтронов) Сумма числа протонов и нейтронов в атоме называется массовым числом.
– часть атома, находящаяся в его центре и заряженная положительно; в ядре сосредоточена основная масса атома. Ядро состоит из нуклонов (протонов и нейтронов) Сумма числа протонов и нейтронов в атоме называется массовым числом.
Число протонов + число нейтронов = массовое число
Например, массовое число изотопа бора (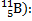
5(число протонов) + 6(число нейтронов) = 11(массовое число)
Протоны
– положительно заряженные частицы ядра атома (относительная масса протона округленно равна 1). Каждый элемент имеет свое специфическое число протонов. Оно определяет общий положительный заряд ядра и место элемента в периодической системе. Число протонов равно порядковому номеру элемента.
Число протонов = заряд ядра = порядковый номер элемента
Химический элемент
– определенный вид атомов с одинаковым зарядом ядра
Порядковый номер элемента = заряд ядра = число протонов
Нейтроны
– электрически нейтральные частицы (относительная масса примерно равна массе протона) Число нейтронов в ядрах одного и того же элемента может быть различным.
Электроны
– отрицательно заряженные частицы (масса равна примерно 1/1836 массы протона), совмещающие в себе свойства частицы и электромагнитной волны.
Электроны образуют оболочку атома. Число электронов в оболочке атома равно числу протонов в ядре атома.
Число протонов = заряд ядра = число электронов = порядковый номер элемента
Главное квантовое число n
Определяет общую энергию электрона. Электроны с близкими энергиями располагаются на соответствующих энергетических уровнях, которые обозначаются арабскими цифрами, равными главному квантовому числу (n = 1,2,3,4,…). Число энергетических уровней равно номеру периода, в котором расположен элемент.
Число энергетических уровней = номеру периода



 Атом
Атом – часть атома, находящаяся в его центре и заряженная положительно; в ядре сосредоточена основная масса атома. Ядро состоит из нуклонов (протонов и нейтронов) Сумма числа протонов и нейтронов в атоме называется массовым числом.
– часть атома, находящаяся в его центре и заряженная положительно; в ядре сосредоточена основная масса атома. Ядро состоит из нуклонов (протонов и нейтронов) Сумма числа протонов и нейтронов в атоме называется массовым числом.