

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...

Археология об основании Рима: Новые раскопки проясняют и такой острый дискуссионный вопрос, как дата самого возникновения Рима...

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...

Археология об основании Рима: Новые раскопки проясняют и такой острый дискуссионный вопрос, как дата самого возникновения Рима...
Топ:
Теоретическая значимость работы: Описание теоретической значимости (ценности) результатов исследования должно присутствовать во введении...
Оснащения врачебно-сестринской бригады.
Генеалогическое древо Султанов Османской империи: Османские правители, вначале, будучи еще бейлербеями Анатолии, женились на дочерях византийских императоров...
Интересное:
Что нужно делать при лейкемии: Прежде всего, необходимо выяснить, не страдаете ли вы каким-либо душевным недугом...
Берегоукрепление оползневых склонов: На прибрежных склонах основной причиной развития оползневых процессов является подмыв водами рек естественных склонов...
Финансовый рынок и его значение в управлении денежными потоками на современном этапе: любому предприятию для расширения производства и увеличения прибыли нужны...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Объект изучения – система, в которой проходит обратимая экзотермическая реакция между йодом и крахмалом. Продуктом реакции является сложное соединение (условно его обозначаем йод-крахмал), окрашенное в синий цвет.
Схема химического равновесия в системе:
йод + крахмал 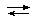 йод-крахмал, DH<0
йод-крахмал, DH<0
Цель опыта
Для обратимой реакции определить направление смещения равновесия при изменении температуры и проверить согласование с принципом Ле Шателье.
Ход опыта
· В пробирку налейте 3–5 мл дистиллированной воды и прибавьте по 2–3 капли растворов йода и крахмала. Отметьте окраску раствора.
· Полученный раствор нагрейте на спиртовке до кипения и отметьте изменение его окраски.
· Охладите раствор в холодной воде до комнатной температуры и отметьте окраску раствора.
Результаты и наблюдения
· Начальная окраска раствора _________________________________________.
· Окраска раствора при нагревании ____________________________________.
· Окраска раствора при охлаждении ___________________________________.
Обработка результатов
· В системе
____________________________________________________________________
(схема равновесной системы)
в равновесии находятся вещества:
____________________________________________________________________
____________________________________________________________________
· Изменение концентрации веществ и смещение химического равновесия (на основании изменения окраски раствора):
| Внешнее воздействие | Изменение концентрации (увеличение – или уменьшение – ¯) | Направление смещения равновесия | |||
| йод, крахмал | йод-крахмал | ||||
| вправо, влево | в сторону экзо- или эндотермической реакции | ||||
| нагревание | |||||
| охлаждение | |||||
Вывод
При нагревании системы химическое равновесие смещается в сторону
|
|
__________________________________ реакции, при охлаждении – в сторону
(эндо- или экзотермической)
_____________________________ реакции, что ___________________________
(эндо- или экзотермической) (согласуется, не согласуется)
с принципом Ле Шателье.
Лабораторная работа 4
«Электролиты»
Опыт 1. Влияние соли слабой кислоты на диссоциацию этой кислоты
Цель опыта
Установить влияние увеличения концентрации одноименного аниона на степень диссоциации кислоты.
Ход опыта
· В две пробирки внесите по 2 мл 0,1М раствора уксусной кислоты.
· В каждую пробирку добавьте по 1 капле индикатора метилового оранжевого.
· Одну пробирку с уксусной кислотой оставьте в качестве контрольной.
· В другую пробирку внесите 3–4 микрошпателя ацетата натрия, перемешать раствор стеклянной палочкой.
· Сравните окраски полученного раствора и раствора в контрольной пробирке.
Обработка результатов
· Окраска метилового оранжевого в растворе уксусной кислоты указывает
на наличие в растворе ионов _________ .
(формула)
· Уравнение диссоциации уксусной кислоты:
____________________________________________________________________
· Математическое выражение и численное значение константы диссоциации:
____________________________________________________________________
· Ацетат натрия – _____________________ электролит:
(сильный, слабый)
____________________________________________________________________
(уравнение диссоциации)
· Изменение окраски метилового оранжевого при добавлении ацетата натрия
вызвано ____________________ концентрации ионов водорода, вследствие
(увеличением, снижением)
смещения химического равновесия диссоциации уксусной кислоты в сторону
___________________________________________ .
(недиссоциированного вещества, продуктов диссоциации)
Вывод
· Добавление ацетатов в раствор уксусной кислоты ____________________________ степень
(увеличивает, снижает)
ее диссоциации.
· Введение в раствор слабой кислоты одноименного аниона приводит к
______________________ степени ее диссоциации.
|
|
(увеличению, снижению)
|
|
|

Папиллярные узоры пальцев рук - маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни...

Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов (88‰)...

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...

Таксономические единицы (категории) растений: Каждая система классификации состоит из определённых соподчиненных друг другу...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!