

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

Эмиссия газов от очистных сооружений канализации: В последние годы внимание мирового сообщества сосредоточено на экологических проблемах...

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

Эмиссия газов от очистных сооружений канализации: В последние годы внимание мирового сообщества сосредоточено на экологических проблемах...
Топ:
История развития методов оптимизации: теорема Куна-Таккера, метод Лагранжа, роль выпуклости в оптимизации...
Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов...
Определение места расположения распределительного центра: Фирма реализует продукцию на рынках сбыта и имеет постоянных поставщиков в разных регионах. Увеличение объема продаж...
Интересное:
Мероприятия для защиты от морозного пучения грунтов: Инженерная защита от морозного (криогенного) пучения грунтов необходима для легких малоэтажных зданий и других сооружений...
Наиболее распространенные виды рака: Раковая опухоль — это самостоятельное новообразование, которое может возникнуть и от повышенного давления...
Принципы управления денежными потоками: одним из методов контроля за состоянием денежной наличности является...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
ХРОМАТОГРАФИЧЕСКИЙ АНАЛИЗ
Утверждено Редакционно-издательским советом университета
в качестве учебного пособия
Магнитогорск
2017
УДК
Рецензенты:
Кандидат технических наук, доцент,
Заведующий кафедрой геологии, маркшейдерского дела
и обогащения полезных ископаемых
ФГБОУ ВО «МГТУ им. Г.И.Носова»
И.А. Гришин
Кандидат технических наук, доцент,
Советник по технологической подготовке кадров
АНО ДПО «КЦПК «Персонал»»
В.Л. Корнилов
Махоткина Е.С., Свечникова Н.Ю., Шубина М.В.
Хроматографический анализ: [Электронный ресурс]: учебное пособие / Елена Станиславовна Махоткина, Наталия Юрьевна Свечникова, Марианна Вячеславовна Шубина. Магнитогорск: ФГБОУ ВО «Магнитогорский государственный технический университет им. Г.И. Носова». – Электрон. текстовые дан. (… Мб). – Магнитогорск: ФГБОУ ВО «МГТУ им. Г.И.Носова», 201…- 1 электрон.опт. диск (CDR). – Систем. требования: IBM PC, любой, более 1 GHz; 512 Мб RAM; 10 Mб HDD; MS Windows XP и выше; Adobe Reader 8.0 и выше; CD/DVD-ROM дисковод; мышь. – Загл. С титул. Экрана.
Учебное пособие составлено в соответствие с образовательными программами обучения в высших учебных заведениях по дисциплинам «Физическая химия», «Методы контроля и анализа веществ», «Аналитическая химия и физико-химические методы анализа». Пособие также может быть использовано в учебных лабораториях и учебно-научных центрах университета, так как в настоящее время хроматографический анализ получил широкое распространение и развитие и используется в различных областях науки и техники.
Пособие содержит краткое изложение теоретических основ хроматографического анализа: история открытия, виды хроматографии, их особенности, основные принципы хроматографических методов. Кроме того, в нем представлены лабораторные работы по определению содержания лёгких углеводородов, …, а также приводятся контрольные вопросы для оценки полученных знаний.
|
|
Учебное пособие предназначено для студентов высших учебных заведений, обучающихся по образовательным программам (ОП) ФГОС ВО по направлениям 18.03.01 «Химическая технология», 22.03.02 Металлургия, 27.03.01 «Стандартизация и метрология», 20.03.01 «Техносферная безопасность», 44.03.01 «Педагогическое образование» (направленность «Химия»), 13.03.01 «Теплоэнергетика и теплотехника».
УДК
Махоткина Е.С., Свечникова Н.Ю., Шубина М.В., 2017
ФГБОУ ВО «Магнитогорский
Государственный технический
университет им. Г.И. Носова», 2017
СОДЕРЖАНИЕ
ВВЕДЕНИЕ
Быстрый технический прогресс и возрастание внимания общества к проблемам окружающей среды даёт прочную уверенность в том, что число аналитических задач и их сложность будут постоянно возрастать. В таких условиях, совершенно очевидно, современными методами анализа должны обладать не только химики-аналитики, химики-технологи, но и специалисты самых разных областей науки и техники. Контроль за качеством и анализ различных объектов проводится при производстве металлов и сплавов, при выпуске пищевых продуктов, при мониторинге степени чистоты воздуха, воды и почв, при изучении геологических объектов, при проверке марки бензина.
По современным оценкам приблизительно 60% всех анализов в мире выполняется хроматографически. Изучение теоретических основ хроматографического анализа, работа на современном хроматографическом комплексе «Хроматэк Кристалл 5000», позволит студентам не только глубже понять физико-химические законы, но и научиться применять их для решения конкретных задач.
Материал данного пособия расположен в логической последовательности: краткие теоретические основы хроматографии, лабораторные работы, вопросы для проверки знаний, примеры решения типовых задач, задачи для самостоятельного решения. Выполнение лабораторных работ на современном оборудовании стимулирует студентов к его освоению, прививает им вкус к осмыслению эксперимента, вооружает студентов разнообразными методиками анализа и тем самым помогает им приобретать некоторый опыт экспериментальной работы.
|
|
Учебное пособие составлено в соответствии с образовательными программами (ОП) ФГОС ВО по направлениям 18.03.01 «Химическая технология», 22.03.02 Металлургия, 27.03.01 «Стандартизация и метрология», 20.03.01 «Техносферная безопасность», 44.03.01 «Педагогическое образование» (направленность «Химия»), 13.03.01 «Теплоэнергетика и теплотехника», а также может быть полезно при проведении исследований в учебно-научных центрах университета.
ХРОМАТОГРАФИЯ
Общие сведения
Перед качественным и количественным определением компонентов очень часто приходится проводить их разделение, так как селективных аналитических реакций немного. Если содержание компонентов незначительно, то перед определением необходимо провести их концентрирование. Операции разделения и концентрирования веществ часто совмещаются. Многие методы проведения таких операций основаны на различии распределения веществ между двумя фазами. При любом разделении компонентов необходимо проведение следующих стадий процесса: контакт фаз и установление равновесия между ними; разделение фаз.
Разделение можно проводить одноступенчатым способом. При этом контакт между двумя несмешивающимися фазами обычно осуществляется путем перемешивания или встряхивания в замкнутом объёме. Движение одной фазы относительно другой в этом случае беспорядочное. Компоненты смеси можно разделить таким способом, если различие между коэффициентами распределения веществ в двух фазах очень велико. В тех случаях, когда коэффициенты распределения компонентов смеси между фазами незначительно отличаются, разделить их одноступенчатым способом не удастся. Более эффективными являются динамические, хроматографические методы.
Хроматография [гр. chromatos – цвет + grapho - пишу] – это метод разделения и анализа смесей веществ, основанный на различном распределении компонентов смеси между двумя несмешивающимися фазами, одна из которых должна быть подвижной (ПФ), а другая – неподвижной (НФ).
|
|
Создателем хроматографического метода анализа является русский ученый Михаил Семенович Цвет. В 1903 году в трудах Варшавского университета появилась программная статья М. С. Цвета “О новой категории адсорбционных явлений и их применению к биохимическому анализу”. Как оказалось впоследствии, именно в этой работе впервые были изложены основы хроматографического метода.
Михаил Семенович Цвет был ботаником-биохимиком с широкими чисто химическими интересами. Одним из основных научных вопросов, которым он занимался, был вопрос выяснения состава хлорофилла. М. С. Цвет установил, что считавшийся однородным зеленый пигмент растений – хлорофилл - на самом деле состоит из нескольких веществ, т.е. М. С. Цвету удалось открыть явление разделения сложной по составу смеси на индивидуальные компоненты.
М. С. Цвет не только открыл само явление разделения, правильно понял физический смысл происходящих процессов, но даже предложил и терминологию, которая сохранилась до настоящего времени. Более того, М. С. Цвет прекрасно понимал, что открытый им метод успешно применим не только для разделения смесей окрашенных соединений, но и для разделения смесей бесцветных веществ, т.е. понимал универсальность этого метода. Он писал: “Конечно, описанные адсорбционные явления наблюдаются не только в случае окрашенных пигментов хлорофилла. Можно предполагать, что все виды окрашенных и бесцветных веществ подчиняются тем же законам”.
Хроматографию сначала использовали очень редко, она появилась слишком рано и в то время еще не могла быть понята и принята по достоинству. Заметное развитие хроматографических методов началось в 30-е годы ХХ в. после того, как Э. Ледерер, прочитав сделанный Г. Вильштетером рукописный перевод книги М. С. Цвета на немецкий язык, провел хроматографическое разделение каротинов. К этому времени возникла острая потребность в новом методе разделения сложных смесей и очистке веществ, разлагающихся при нагревании. Своего расцвета хроматография достигла после того, как А. Дж. П. Мартин и А.Т. Джеймс в 1952 году предложили новый метод хроматографии – газожидкостную распределительную хроматографию.
|
|
В настоящее время заслуги М. С. Цвета признаны во всем мире. По оценке ЮНЕСКО открытие хроматографии Цветом М.С. на рубеже ХIX – XX вв. вошло в десятку величайших открытий ХХ века.
Хроматография продолжает бурно развиваться и в настоящее время является одним из перспективных методов анализа.
Каждый вид хроматографии основан на отдельном, особом физическом процессе, но при этом все эти методы разделения объединяются в одну науку – хроматографию, т.к. они обладают общими принципами, типичными для всех хроматографических методов.
Этими общими принципами являются следующие:
• хроматография – это процесс динамический, всегда обязательно имеем одну подвижную фазу относительно другой неподвижной фазы;
• разделение смеси веществ достигается в результате многократного повторения по высоте колонки одного и того же элементарного акта: для адсорбционной хроматографии – повторение акта адсорбции-десорбции, для ионообменной хроматографии – повторение реакции ионного обмена.
Таким образом, можно сформулировать следующие определения хроматографии, в дополнение к приведенному ранее:
1. Хроматография − это физико-химический метод анализа и исследования веществ и их смесей, основанный на разделении компонентов за счет различия в параметрах распределения их между фазами при перемещении через слой неподвижной фазы потоком подвижной фазы.
2. Хроматография − это процесс разделения молекул за счет дифференциальной миграции, т.е. разделения за счет различных скоростей перемещения различных молекул.
Вещество, сильнее взаимодействующее с НФ, будет медленнее двигаться через хроматографическую систему по сравнению с веществом, слабее взаимодействующим с НФ. Для разделения разных молекул НФ должна обладать хотя бы одним из основных свойств:
- физически сорбировать1 вещества, находящиеся в ПФ;
- химически сорбировать вещества, находящиеся в ПФ;
- растворять разделяемые вещества;
- удерживать одни вещества и не задерживать другие, в зависимости от их размеров или формы.
Совпадение формы хроматографического максимума с гауссовой кривой становится объяснимым с позиций кинетической теории. Гауссовой кривой в статистике описывают частоту (вероятность) появления отклонений случайного характера измеряемой величины от её среднего значения при большом числе повторных измерений. Величина скорости молекул, движущихся по хроматографической колонке, тоже носит статистический характер. Двигаясь хаотически, молекулы на своём пути претерпевают множество случайных столкновений, поэтому одни молекулы будут продвигаться быстрее, чем другие. Границы хроматографической зоны при этом расширяются. Отклонения от среднего значения скорости движения молекул в положительные и отрицательные значения приводят к распределению молекул в хроматографической зоне, описываемому гауссовой кривой.
|
|
На продвижение частиц влияет ряд факторов, которые искажают форму пиков и снижают эффективность колонки (структура неподвижной фазы, массообмен (скорость установления равновесия, диффузия молекул). Решая уравнения кинетической теории, учитывающие влияние различных факторов, можно определить оптимальную высоту, эквивалентную теоретической тарелке. Таким образом, кинетическая теория даёт основу для оптимизации хроматографического процесса.
Таблица 1.2
| Газ - носитель | Характеристика свойств |
Азот
Водород
Гелий
Аргон
Углекислый газ
Воздух
Очистка газа-носителя. Требования к степени чистоты газа-носителя определяют следующие факторы:
• требования применяемой системы детектирования;
• природа разделяемых компонентов;
• природа используемой неподвижной фазы;
• температурный режим процесса разделения;
• необходимая точность получения воспроизводимых величин параметров удерживания.
Основными примесями, мешающими выполнению газохроматографических разделений, являются вода, кислород, органические соединения. Обычным способом очистки газа-носителя от названных примесей является пропускание его через осушительную колонку, заполненную силикагелем, и колонки, заполненные молекулярными ситами и активированным углем. Для очистки гелия используют молекулярные сепараторы, мембраны или низкотемпературную очистку. Для удаления кислорода из газа-носителя чаще всего используют катализаторы, содержащие, например, медно-магниевый силикат.
Некоторые газы-носители используются в качестве вспомогательных газов в целях обеспечения функционирования некоторых типов детекторов. Например, водород и воздух – для работы детектора пламенно-ионизационного, кислород – для пламенно-фотометрического детектора, добавки кислорода к газу-носителю – для детектора электронного захвата, получение озона из кислорода – при использовании хемилюминесцентного детектора.
ЦЕЛЬ РАБОТЫ
1.1. Ознакомиться с устройством и принципом действия хроматографического комплекса «Хроматэк Кристалл 5000».
1.2. Определить содержание легких углеводородов в смеси газохроматографическим методом.
ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
Хроматография – это метод разделения и определения веществ, основанный на распределении компонентов между двумя фазами – подвижной и неподвижной. Неподвижной (стационарной) фазой служит твердое пористое вещество (часто его называют сорбентом) или пленка жидкости, нанесенная на твердое вещество. Подвижная фаза представляет собой жидкость или газ, протекающий через неподвижную фазу, иногда под давлением. Компоненты анализируемой смеси (сорбаты) вместе с подвижной фазой передвигаются вдоль стационарной фазы. Ее обычно помещают в стеклянную или металлическую трубку, называемую колонкой. В зависимости от силы взаимодействия с поверхностью сорбента (за счет адсорбции или по какому-либо другому механизму) компоненты будут перемещаться вдоль колонки с разной скоростью. Одни компоненты останутся в верхнем слое сорбента, другие, в меньшей степени, взаимодействующие с сорбентом, окажутся в нижней части колонки. Таким образом, происходит быстрое разделение сложных смесей компонентов.
Существуют различные классификации хроматографических методов. Одной из самых распространенных является классификация по физической природе неподвижной и подвижной фаз: жидкостная хроматография (ЖХ) (если подвижная фаза жидкая) и газовая хроматография (ГХ) (если подвижная фаза газообразная).
В ГХ подвижной фазой служит инертный газ (газ-носитель), протекающий через неподвижную фазу, имеющую большую поверхность. В качестве подвижной фазы можно использовать водород, гелий, азот, аргон и углекислый газ. Наиболее часто используют азот, как более доступный и дешевый. Газ-носитель обеспечивает перенос разделяемых компонентов по хроматографической колонке и не взаимодействует ни с разделяемыми веществами, ни с неподвижной фазой.
Разделение в ГХ системах достигается за счет многократно повторяющегося процесса распределения компонентов смеси между движущейся газовой фазой и неподвижной твердой или жидкой фазой, нанесенной на инертный носитель. Процесс разделения основан на различии в растворимости и летучести анализируемых компонентов. Быстрее через хроматографическую колонку движется тот компонент, растворимость которого в неподвижной фазе меньше, а летучесть при данной температуре больше. Данным методом могут быть проанализированы не только газообразные, но и жидкие и твердые вещества. Их анализ возможен при нагревании, что необходимо для преведения веществ в газообразное состояние.
Достоинствами ГХ являются:
– сравнительная простота аппаратурного оформления;
–широкие границы применимости (можно определять соединения, для которых достигается давление насыщенного пара 0,001-1 мм Т.ст.);
– возможность определения с высокой точностью малых количеств газов органических соединений с высокой точностью;
– быстрота анализа;
– широкий выбор сорбентов и неподвижных фаз;
– высокая гибкость изменения условий разделения;
–возможность осуществления химических реакций в хроматографической колонке или детекторе, что расширяет круг анализируемых соединений (реакционная газовая хроматография).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Основное оборудование
В работе используется хроматографический комплекс «Хроматэк кристалл 5000» (рис. 3.1.) включающий:
- пламенно-ионизационный детектор;
- колонку хроматографическую насадочную из нержавеющей стали длиной 5 м, внутренним диаметром 3 мм, внутренняя составляющая колонки 10% ПЭГ 1000 Сферохром;

Рис. 6. Принципиальная схема «Хроматэк кристалл 5000»
-программное обеспечение (ПО) «Хроматэк Аналитик» для сбора и обработки хроматографической информации, поступающей с хроматографа.
ПО «Хроматэк Аналитик» позволяет:
- осуществлять автоматизированный сбор и хранение хроматографической информации;
- выполнять обработку хроматографической информации с выдачей результатов анализов;
- оформлять отчеты по выполненным анализам в соответствии с требованиями пользователя;
- преобразовывать хроматографические данные в различные файловые форматы для использования этих данных в программах других производителей;
- выполнять различные узкоспециализированные расчеты по конкретным аналитическим задачам.
Материалы
В работе для проведения хроматографического анализа используются легкие углеводороды – октан, толуол, бензол и ундекан. Для идентификации пиков используют:
- стандартные смеси:
- 40% октан+60% толуол;
-20% бензол + 80% ундекан;
- исследуемый образец, содержащий октан, толуол, бензол и ундекан произвольного состава (задаётся преподавателем);
- шприц вместимостью 10 мкл с ценой деления 0,1 мкл;
- ацетон для промывки микрошприца.
Подготовка к анализу
4.3.1.Включить и подготовить к работе хроматограф, генератор водорода, компрессор, баллон для подачи газа-носителя (азот) в соответствии с инструкциями по эксплуатации.
4.3.2. Для запуска соединения выполнить двойной щелчок мышью на ярлыке соединения, расположенном на рабочем столе. Программа Панель управления подключится к хроматографу, после чего будет запущена программа Хроматэк Аналитик 2.6. (рис.7.)
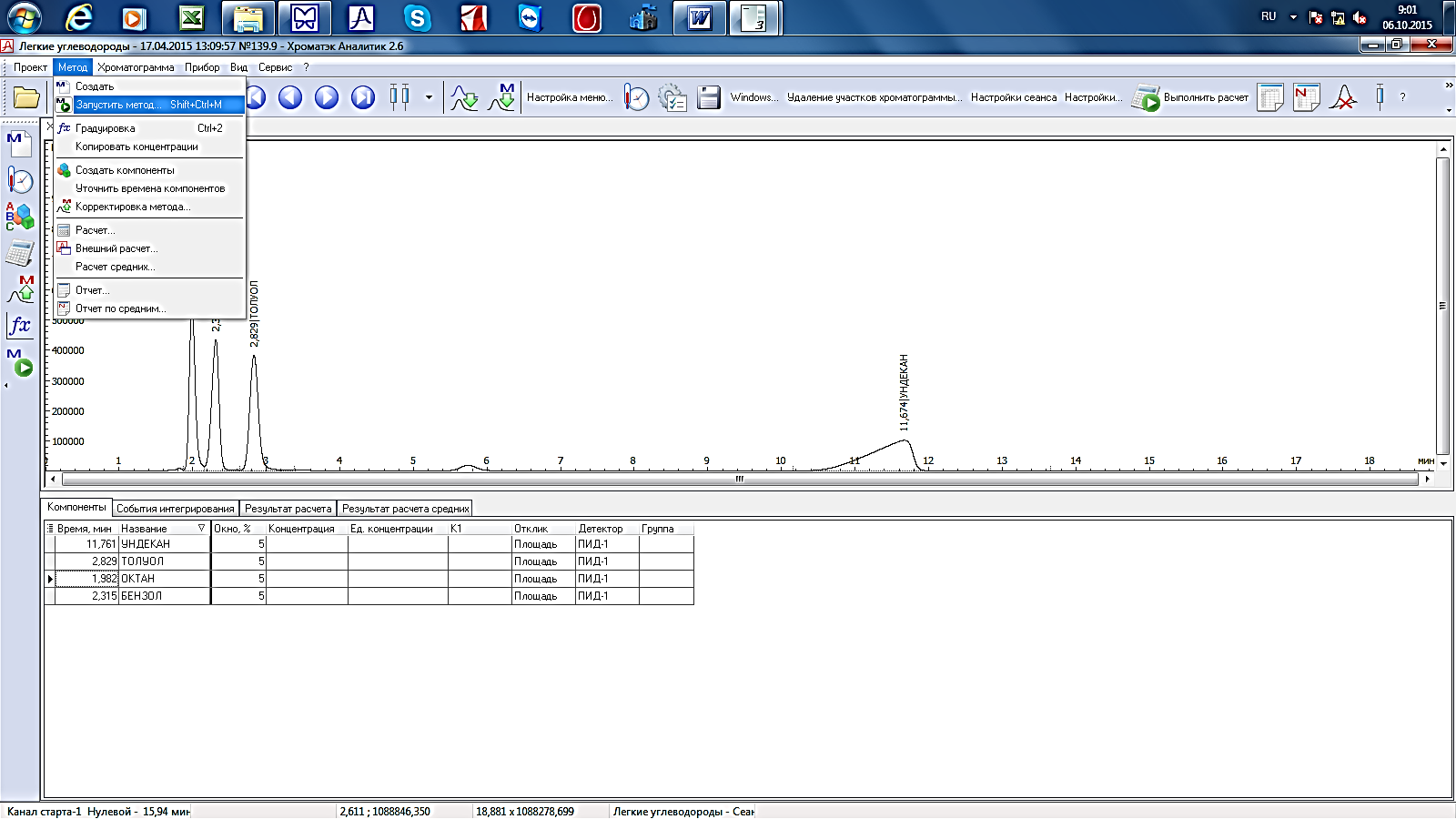
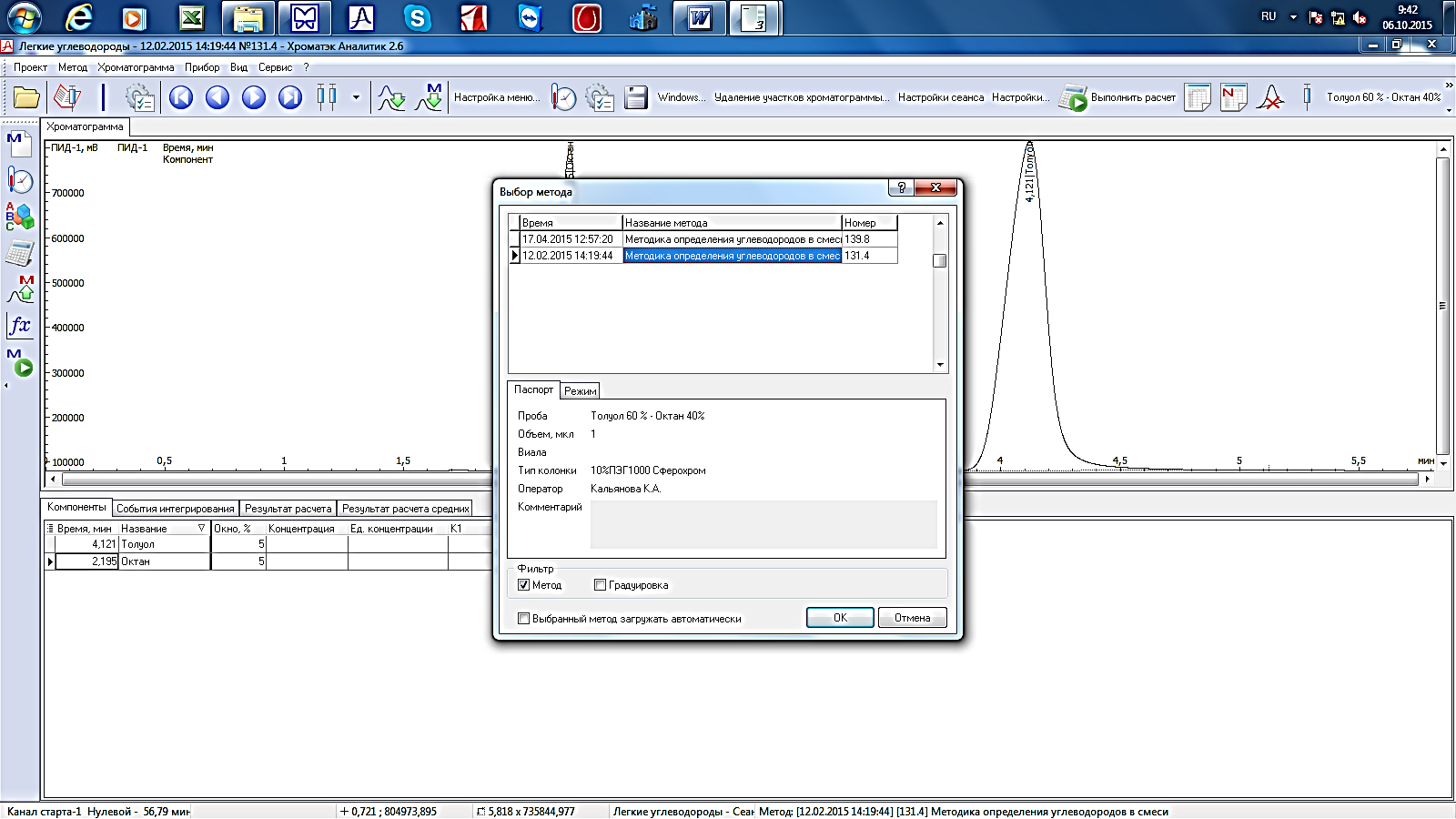
После загрузки программы Хроматэк Аналитик 2.6 в меню Метод выберите команду – Запустить метод или на боковой панели инструментов нажмите соответствующую кнопку (рис. 8, 9, 10).
| |
Рис. 7. Запуск соединения с хроматографом
|
Рис.8. Выбор команды
«Запустить метод»
Настроить параметры режима хроматографа в соответствии с табл. 1. Прибор будет готов к работе после того, как на хроматографе загорится зеленый сигнал «ГОТОВНОСТЬ».
4.3.3. Подготовить микрошприц для набора пробы. Для этого необходимо его промыть ацетоном и исследуемой жидкостью (не менее двух раз каждым). Затем «продуть» шприц воздухом подсоединив его к специальной трубке для «продувания», которая прикреплена к компрессору (продолжительность операции 2 минуты).
| ||
| Рис.9. Запуск метода |
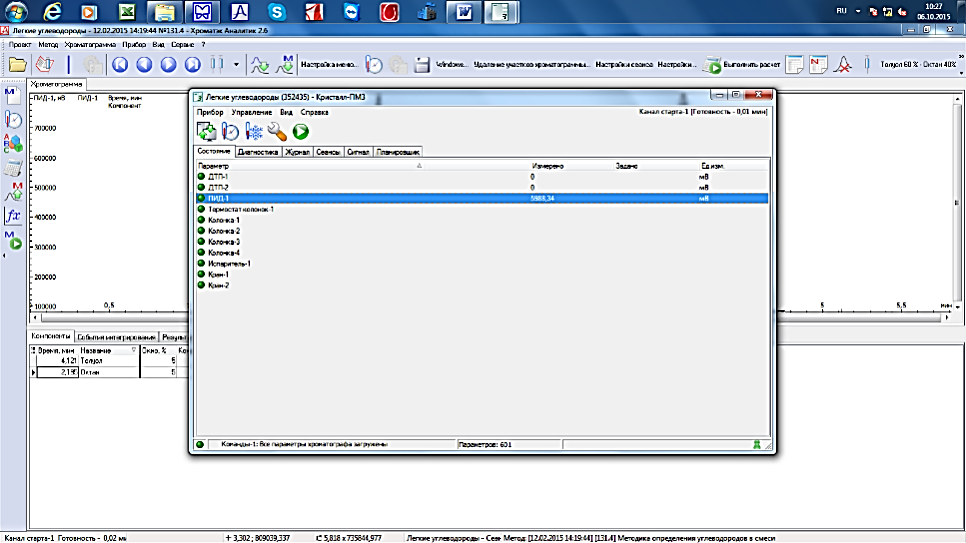
Рис.10. Хроматограф в состоянии готовности
4.3.4. Отобрать пробу испытуемого образца объёмом 0,5 мкл в микрошприц.
Примечание: При образовании пузырьков воздуха в микрошприце при отборе пробы необходимо их удалить. Для этого шприц держать вертикально иглой вверх, на кончик шприца аккуратно надеть резиновую прокладку и слегка надавить на поршень шприца до полного удаления воздуха из пробы.
Таблица 1
Режим работы хроматографа
| Параметр | Значение параметра |
| Канал старта | 15 минут |
| ПИД | Температура [150°C] Расход водорода [25 мл/мин] Расход воздуха [250 мл/мин] |
| Термостат колонок | Температура [85°C] |
| Колонка «10% ПЭГ 100 Сферохром» | Расход [30 мл/мин] Газ-носитель Азот |
| Испаритель | Температура [120°C] |
Проведение испытания
Последовательно провести хроматографический анализ стандартных проб для идентификации пиков, а затем два параллельных испытания (для расчета погрешности испытания) исследуемой смеси неизвестного состава (задается преподавателем).
4.3.1. Подготовленную пробу испытуемого образца объёмом 0,5 мкл ввести в испаритель.
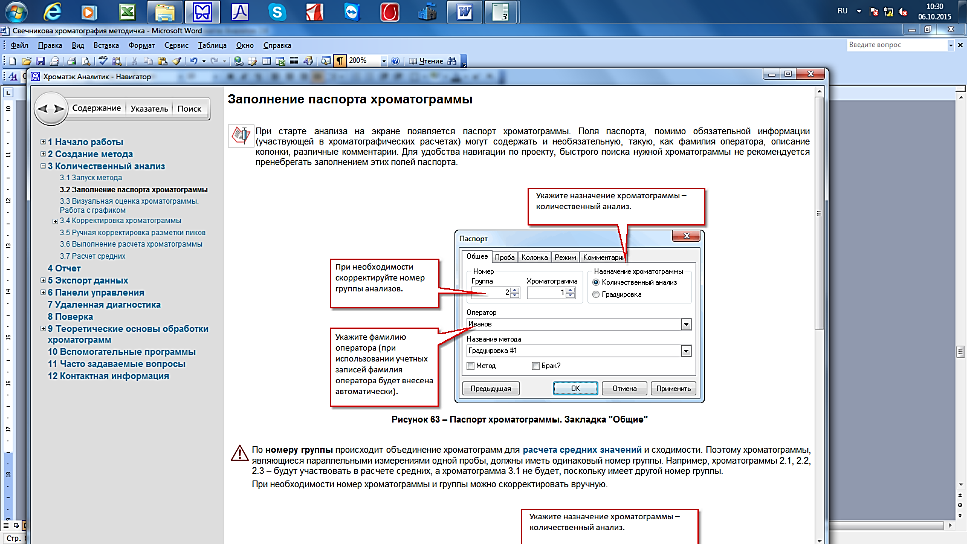
4.3.2. Включить «Старт» и провести анализ в течении 20 минут. По мере проведения анализа на экране будет строиться хроматограмма. При старте анализа на экране появляется паспорт хроматограммы. Поля паспорта помимо обязательной информации могут содержать и дополнительную, такую как фамилия оператора, описание колонки, различные комментарии (рис. 11.).
По номеру группы происходит объединение хроматограмм для расчета средних значений и сходимости. Поэтому хроматограммы являющиеся параллельными измерениями одной пробы, должны иметь одинаковый номер группы. При необходимости номер хроматограммы и группы можно скорректировать вручную (рис.12.).
| |
| Рис.11. Паспорт хроматограммы |
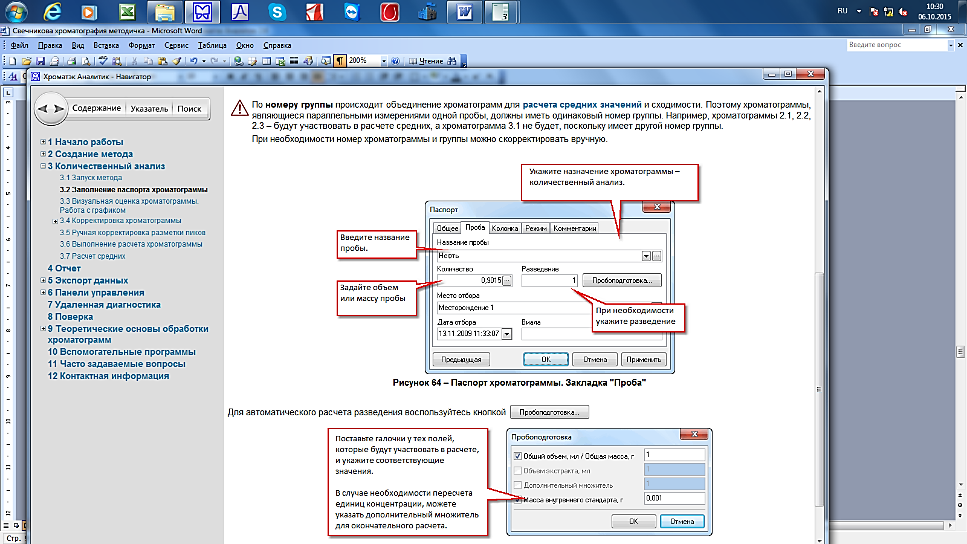
| Рис.12. Корректировка паспорта хроматограммы вручную |
По окончании анализа хроматограф автоматически перейдет в режим Подготовка и на экране монитора будет видна вся хроматограмма. Далее необходимо провести идентификацию пиков методом сравнения времени удерживания анализируемого компонента с временем удерживания известного соединения при строго заданных условиях анализа.
Для этого рекомендуется оценить разметки пиков, величину и характер шумов нулевой линии.
По умолчанию автоматически устанавливается масштаб, при котором видна вся хроматограмма. Для того чтобы оценить характер хроматограммы у подножия пиков, необходимо воспользоваться операциями масштабирования, которые выполняются с помощью мыши и клавиатуры.
Для того чтобы увеличить участок хроматограммы, нажмите левую кнопку мыши в одном из углов интересующей области и, не отпуская, переместите указатель мыши в противоположный угол. После отпускания выбранная область будет увеличена (рис. 13.).

Рис.13. Выделение рамкой области хроматограммы
Масштабирование хроматограммы с помощью мыши удобно сочетать с ТОльзованиием курсорных кнопок клавиатуры (рис. 14).
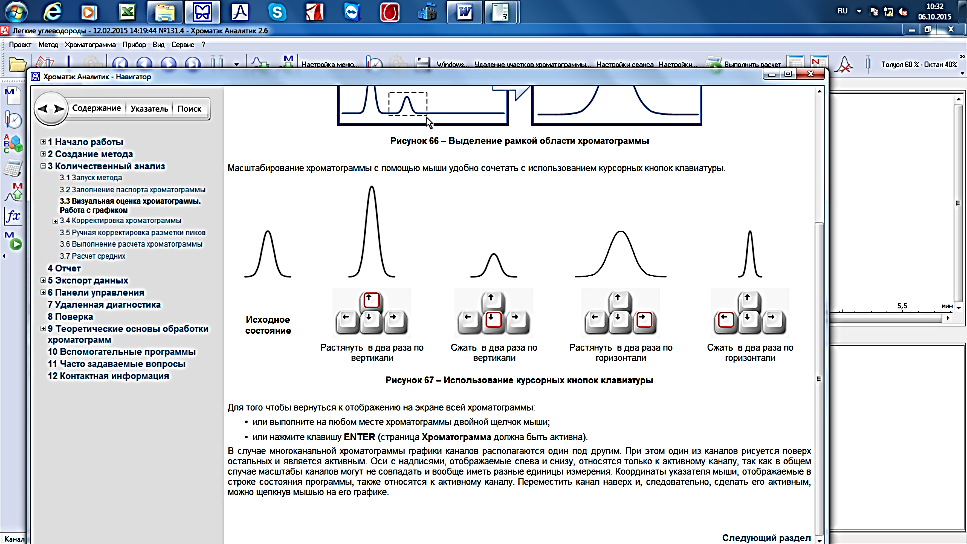
Рис.14. Использование курсорных кнопок клавиатуры
Для того чтобы вернуться к отображению на экране всей хроматограммы:
- или выполните на любом месте хроматограммы двойной щелчок мыши;
- или нажмите клавишу ENTER (страница Хроматограмма должна быть активна).
В случае многоканальной хроматограммы графики каналов располагаются один под другим. При этом один из каналов рисуется поверх остальных и является активным. Оси с надписями, отображаемые слева и снизу, относятся только к активному каналу, так как в общем случае масштабы каналов могут не совпадать и вообще иметь разные единицы измерения. Координаты указателя мыши, отображаемые в строке состояния программы, также относятся к активному каналу. Переместить канал наверх и, следовательно, сделать его активным можно щелкнув мышью на его графике.
С помощью настройки параметров операции Интегрирование не всегда удается добиться автоматической корректной разметки пиков на хроматограмме. Для устранения этой проблемы прямо на графике можно визуально откорректировать положение характерных точек пика (рис.15.).
Для того чтобы изменения в разметке вступили в силу, нажмите на кнопку выполнить расчет  .
.
Если в канале хроматограммы присутствуют пики, созданные или измененные вручную, то автоматического обнаружения новых пиков в данном канале не производится.
После проведения ручной корректировки пиков на хроматограмме, при выполнении Расчета хроматограммы, операция Интегрирование не производит поиск новых пиков, а только пересчитывает площади и высоты существующих. Это сделано для того чтобы вся работа по ручной корректировке пиков, выполненная во время текущего анализа не была сведена на нет автоматической разметкой по его окончании.

Рис. 15. Ручная корректировка разметки пиков
Для того чтобы производилось автоматическое обнаружение новых пиков на хроматограмме не должно быть пиков, скорректированных вручную. Если возникла необходимость провести автоматическую разметку после процедуры ручной корректировки, все пики нужно удалить.
Для удаления пиков в меню Хроматограмма | Операции выберите одноименную команду или на панели инструментов нажмите соответствующую кнопку  (рис. 16.).
(рис. 16.).

Рис.16. Удаление разметки пиков
Операцию Удаление пиков с критерием Неидентифицированные удобно включать в последовательность Расчет хроматограммы после операции Идентификация.
Разметка пика может быть удалена вручную (рис. 17.).
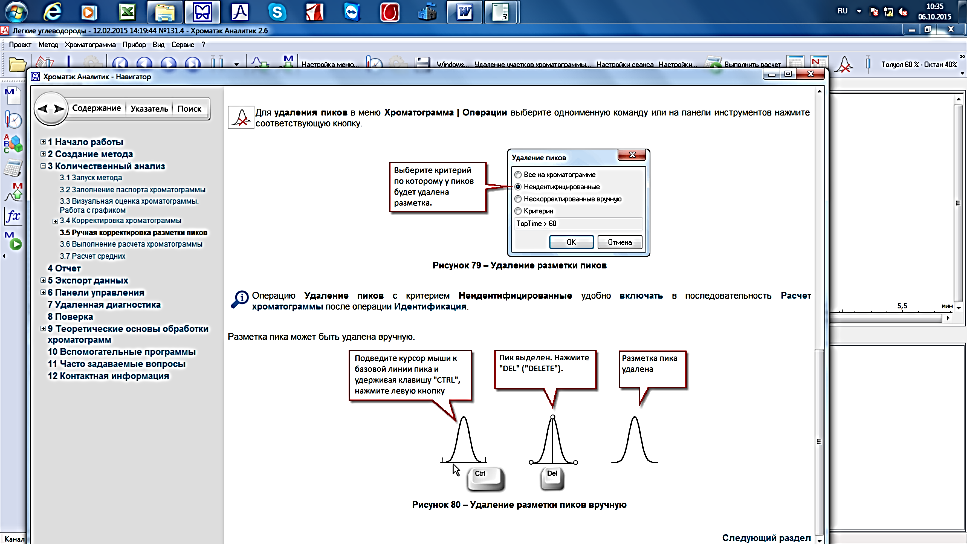
Рис. 17. Удаление разметки пиков вручную
Расчет хроматограммы выполняется автоматически при завершении записи хроматограммы.
Оператор может выполнить его вручную в любой момент записи, нажав на панели инструментов кнопку 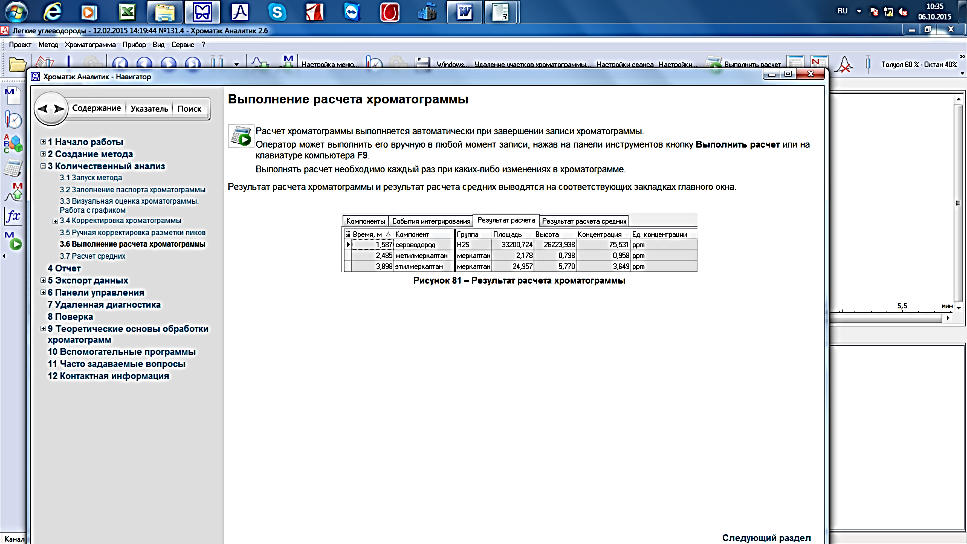 - Выполнить расчет или на клавиатуре компьютера F9.
- Выполнить расчет или на клавиатуре компьютера F9.
Выполнять расчет необходимо каждый раз при каких-либо изменениях в хроматограмме.
Результат расчета хроматограммы и результат расчета средних выводятся на соответствующих закладках главного окна (рис. 18.).

Рис. 18. Результат расчета хроматограммы
Для создания отчета по хроматограмме в меню Метод выберите команду Отчет или нажмите на панели инструментов соответствующую кнопку 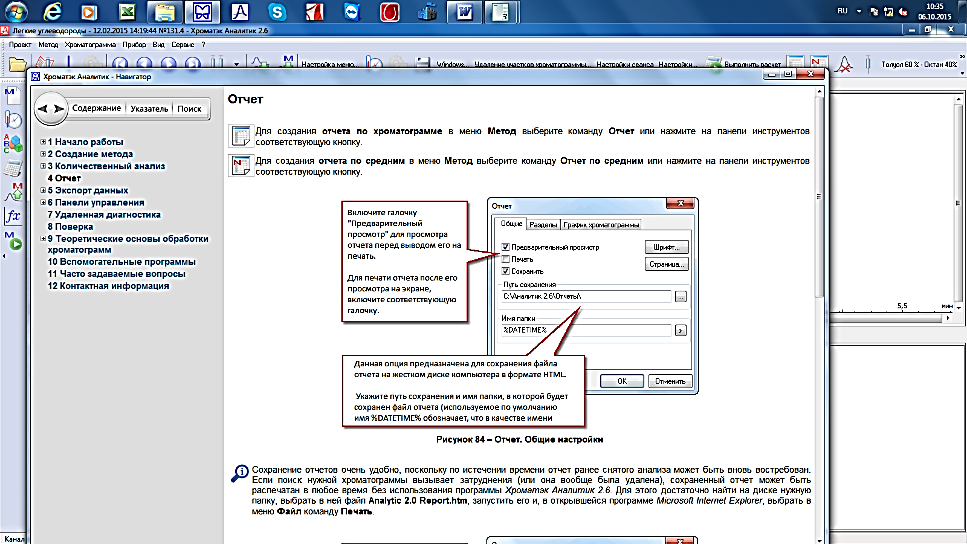 .
.
Для создания отчета – по средним – в меню Метод выберите команду Отчет по средним или нажмите на панели инструментов соответствующую кнопку 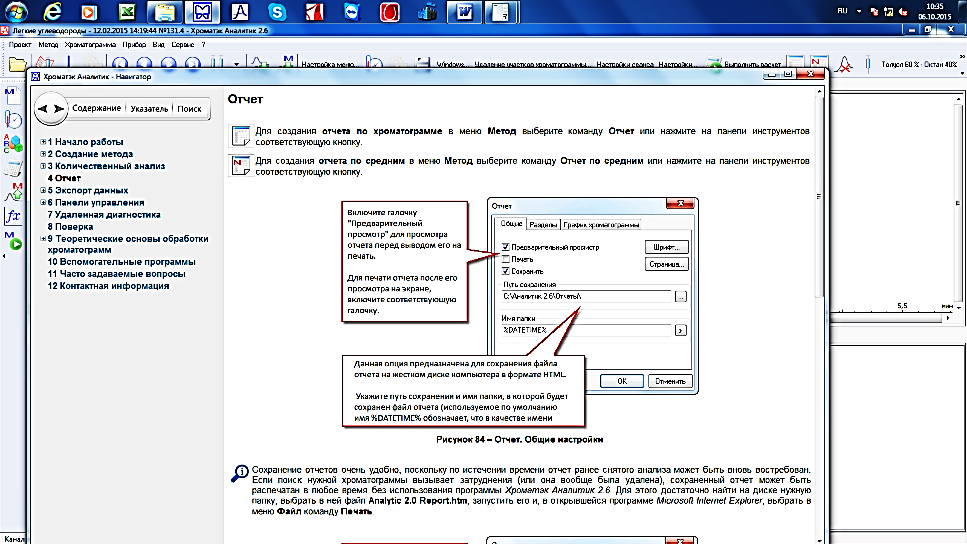 (рис. 19.).
(рис. 19.).

Рис. 19. Отчет. Общие настройки
Сохранение отчетов очень удобно, поскольку по истечении времени отчет ранее снятого анализа может быть вновь востребован. Если поиск нужной хроматограммы вызывает затруднения (или она вообще была удалена), сохраненный отчет может быть распечатан в любое время без использования программы Хроматэк Аналитик 2.6. Для этого достаточно найти на диске нужную папку, выбрать в ней файл Analytic 2.0 Report. Htm, запустить его и, в открывшейся программе Microsoft Internet Explorer, выбрать в меню Файл команду Печать (рис. 20.).
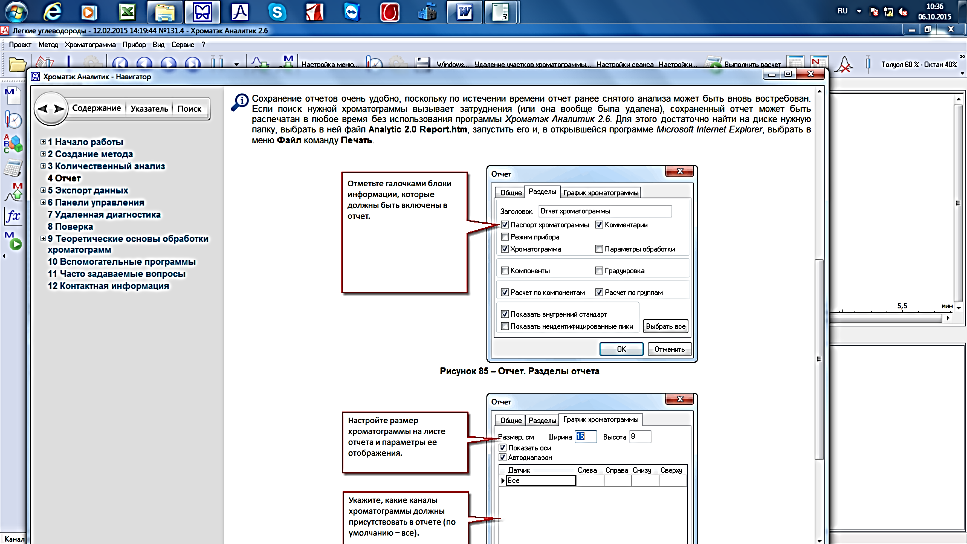
Рис. 20. Отчет. Разделы отчета
График хроматограммы можно распечатать как целиком, так и по частям. В случае необходимости распечатки части графика нажмите кнопку Добавить столько раз, сколько участков графика требуется распечатать. Задайте для каждого участка время (в столбцах Слева и Справа) и амплитуду (в столбцах Сверху и Снизу). В столбце Датчик укажите нужный канал хроматограммы. По умолчанию печататься будут все каналы хроматограммы (рис. 21.).
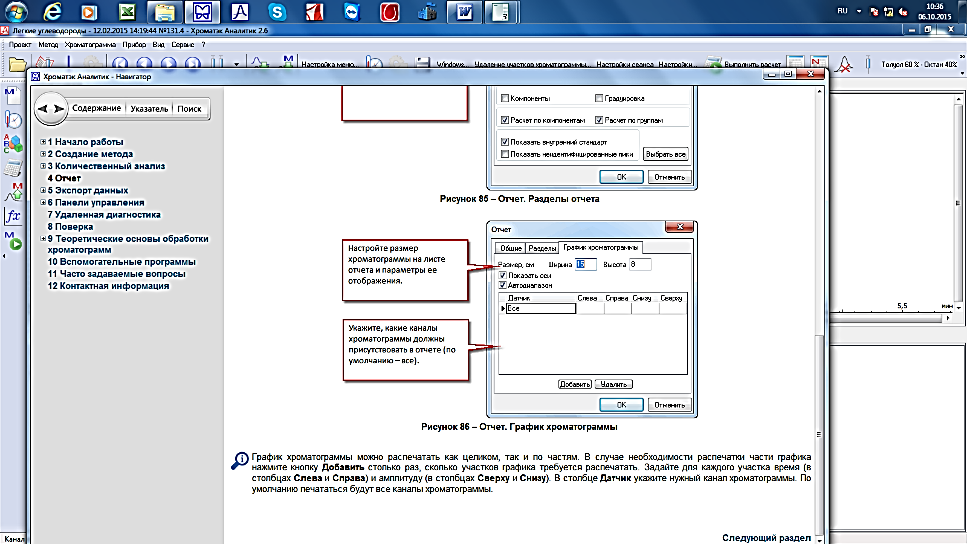
Рис.21. Отчет. График хроматограммы
Обработка результатов
5.1. Полученные результаты внести в таблицу 2.
5.2. Рассчитать процентное содержание веществ в пробе по формуле:
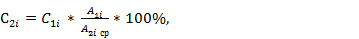 (1)
(1)
где:
С2 i – процентное содержание i-го компонента в исследуемой пробе;
А2 i ср – среденее значение площади пика i-го компонента в исследуемой пробе;
С1 i - процентное содержание i-го компонента в стандартной пробе;
А1 i – площадь пика i-го компонента в стандартной пробе.
5.3. Определить относительную и абсолютную погрешность полученных результатов по формулам:
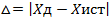 (2)
(2)
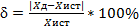 (3)
(3)
5.4. Сравнить полученные результаты с истинными значениями, результаты внести в табл. 3.
5.5. Сделать выводы по работе.
Таблица 2
Результаты хроматографического анализа
| Вещество | Стандартная проба | Испытуемая проба | ||||||||
| Содержание в пробе, С1i, % | Площадь пика, А1i, мВ*мин | Время выхода t, мин | Площадь пика, мВ*мин | Время выхода | Содержание в пробе, С2i,% | |||||
| В первом испытании (А2I i) | Во втором испытании (А2II i) | Среднее значение (А2iср) | В первом испытании,tI, мин | Во ТОром испытании, tII, мин | Среднее значение, tср,, мин | |||||
Таблица 3
Расчет погрешности испытания
| Вещество | Истинное содержание в пробе, С, % | Расчетное содержание в пробе, С2,% | Абсолютная погрешность, D,% | Относительная погрешность, d,% | Максимальное значение абсолютной погрешности, Dmax,% | Максимальное значение относительной погрешности, dmax,% |
|
|
| |||||
КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Что такое хроматография?
2. Какие виды хроматографии существуют? В чем их главное отличие?
3. В газовой хроматографии, что выступает в качестве подвижной фазы, неподвижной фазы?
4. Перечислите преимущества газовой хроматографии.
5. Какой инертный газ используется в данном методе и почему?
6. Опишите общее устройство газового хроматографа.
7. Расскажите принцип действия пламенно-ионизационного детектора. Почему в данном методе применялся ПИД?
8. Какие дополнительные газы необходимы для работы ПИД? В каком соотношении они должны подаваться в ПИД?
9. Что такое режим работы прибора? На что он влияет? Как изменится общий вид хроматографических пиков, если увеличить температуру в колонке и увеличить расход газа?
10. Какова последовательность методики определения процентного содержания углеводородов в смеси? Что такое стандартная проба?
Б иблиографический список
1. Ягодовский, В.Д. Адсорбция [Электронный ресурс]: В.Д.Ягодовский. – Эл. изд. – Элек. Текст. Дан. (1файл pdf: 219 с.) – М.: БИНОМ. Лаборатория знаний, 2015.- (учебник для высшей школы). – Систем. требования: Adobe Reader XI; Экран 10”. ISBN 978-5-9963-2929.
2. Аналитическая химия и физико-химические методы анализа [Текст]: учебник: в 2 т. Т. 1 / [Ю. М. Глубоков, В. А. Головачева, В. И. Дворкин и др.]; под ред. А. А. Ищенко. – М.: Академия, 2010. – 352 с.: ил., граф., схемы, табл. – (Высшее проф. Образование: Химические технологии).
РЕШЕНИЕ ТИПОВЫХ ЗАДАЧ
Пример 1
Определить массовую долю компонентов газовой смеси по следующим данным:
| Компонент смеси | Пропан | Бутан | Пентан | Циклогексан |
| S, мм2 | 175 | 203 | 182 | 35 |
| k | 0,68 | 0,68 | 0,69 | 0,85 |
Решение: расчёты проводим по методу внутренней нормализации, согласно которому
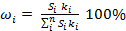 ,
,
где 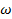

Архитектура электронного правительства: Единая архитектура – это методологический подход при создании системы управления государства, который строится...

Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов (88‰)...

Состав сооружений: решетки и песколовки: Решетки – это первое устройство в схеме очистных сооружений. Они представляют...

Опора деревянной одностоечной и способы укрепление угловых опор: Опоры ВЛ - конструкции, предназначенные для поддерживания проводов на необходимой высоте над землей, водой...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!