

Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов (88‰)...

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...

Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов (88‰)...

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...
Топ:
Установка замедленного коксования: Чем выше температура и ниже давление, тем место разрыва углеродной цепи всё больше смещается к её концу и значительно возрастает...
Методика измерений сопротивления растеканию тока анодного заземления: Анодный заземлитель (анод) – проводник, погруженный в электролитическую среду (грунт, раствор электролита) и подключенный к положительному...
Интересное:
Как мы говорим и как мы слушаем: общение можно сравнить с огромным зонтиком, под которым скрыто все...
Искусственное повышение поверхности территории: Варианты искусственного повышения поверхности территории необходимо выбирать на основе анализа следующих характеристик защищаемой территории...
Влияние предпринимательской среды на эффективное функционирование предприятия: Предпринимательская среда – это совокупность внешних и внутренних факторов, оказывающих влияние на функционирование фирмы...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Пусть 100,0 мл 0,1 М раствора HCl титруют 0,1 М раствором NaOH. Допустим, что ионная сила раствора близка к нулю (это, конечно, не так, но учет ионной силы затруднит расчеты). Пренебрежём также и изменением объёма. Ионы Na+ и Сl- не влияют на кислотно-основное равновесие. Составим таблицу значений рН и построим кривую титрования.
Таблица 3.1. Титрование 100 мл 0,1 М раствора соляной кислоты 0,1 М раствором гидроксида натрия
| F= VT/Vo | Состав раствора | рН-определяющий компонент | Формула расчета рН | Значение рН |
| 0/100=0 | HCl, H2O | HCl | pH=-lgCкисл | 1 |
| 90/100=0.9 | HCl, H2O | HCl | pH=-lgC кисл | 2 |
| 99/100=0.99 | HCl, H2O | HCl | pH=-lgC кисл | 3 |
| 9.9/100=0.999 | HCl, H2O | HCl | pH=-lgC кисл | 4 |
| 100/100=1 | H2O, NaCl | H2O | pH=pOH | 7 |
| 100.1/100=1.001 | H2O, NaCl, NaOH | NaOH | pH= 14+lgCосн | 10 |
| 101/100=1.01 | H2O, NaCl, NaOH | NaOH | pH= 14+lgCосн | 11 |
| 110/100=1.1 | H2O, NaCl, NaOH | NaOH | pH= 14+lgCосн | 12 |
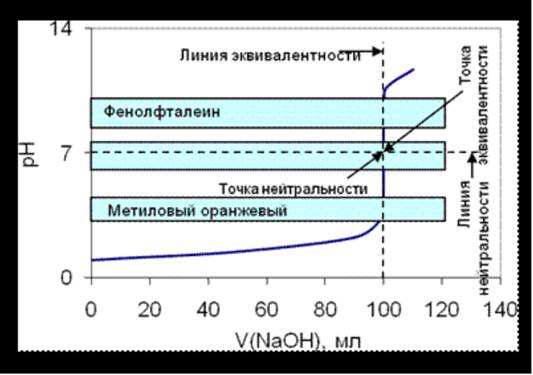
Рисунок 3.1. Кривая титрования сильной кислоты сильным основанием.
· Прямую, параллельную оси абсцисс и пересекающую ось ординат при pH 7,0, называют линией нейтральности.
· Прямую, параллельную оси ординат и пересекающую ось абсцисс при значении эквивалентного объема щелочи (VNaOH=100,0 мл), называют линией эквивалентности.
· Точку пересечения кривой титрования с линией эквивалентности, называют точкой эквивалентности, а пересечение кривой титрования с линией нейтральности – точкой нейтральности.
· Резкое изменение pH в области точки эквивалентности называют скачком титрования.
Выводы из кривой титрования
· Кривая симметрична относительно точки эквивалентности
· Точка эквивалентности совпадает с линией нейтральности
· Скачек титрования имеет большой интервал
Кривая титрования слабой кислоты сильным основанием
Пусть 100.0 мл 0,1 М раствора СН3СООН титруют 0,1 М раствором NaOH. В основе титрования лежит реакция СН3СООН + NaOH = СН3СООNa + H2O.
|
|
В начале титрования в растворе находится только слабая кислота. До точки титрования при титровании получается сопряженное слабое основание СН3СООNa и раствор представляет собой буферную смесь. В точке эквивалентности вся кислота оттитрована и рН раствора определяется наличием соли СН3СООNa. После точки эквивалентности основным источником гидроксильных ионов будет добавленное сильное основание. Составим таблицу значений рН, сделав те же допущения, что и в п. 5.2.1.
Таблица 3.2. Тирование100 мл 0,1 н. раствора уксусной кислоты 0,1 н. раствором гидроксида натрия
| f = Vт/Vo | состав раствора | рН-определяющий компонент | формула расчета рН | значение рН |
| 0/100=0 | СН3СООН,Н2О | СН3СООН | pH=1/2pKк-1/2lgCk | 3 |
| 9/100=0,09 | СН3СООН, Н2О СН3СООNa | буферная смесь | pH=pKk – lg Ck/Cc | 3,8 |
| 50/100=0,5 | СН3СООН, Н2О СН3СООNa | буферная смесь | pH=pKk – lg Ck/Cc | 4,8 |
| 91/100=0,91 | СН3СООН, Н2О СН3СООNa | буферная смесь | pH=pKk – lg Ck/Cc | 5,8 |
| 99,9/100=0,999 | СН3СООН, Н2О СН3СООNa | буферная смесь | pH=pKk – lg Ck/Cc | 6,8 |
| 100/100=1 | СН3СООNa, Н2О | СН3СООNa | pH=7-1/2lgKk+1/2lgCo | 8,75 |
| 100,1/100=1,001 | СН3СООNa, Н2О NaOH | NaOH | pH= 14 + lgCo | 9,7 |
| 101/100=1,01 | СН3СООNa, Н2О NaOH | NaOH | pH= 14 + lgCo | 10,7 |
| 110/100=1,1 | СН3СООNa, Н2О NaOH | NaOH | pH= 14 + lgCo | 10,7 |
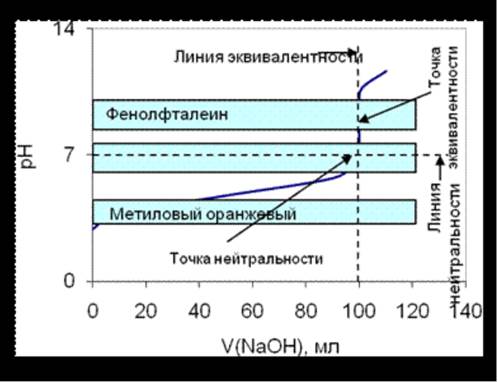
Рисунок 3.2. Кривая титрования слабой кислоты сильным основанием
Выводы из кривой титрования
1. Несовпадение точки эквивалентности с точкой нейтральности и расположение точки эквивалентности в щелочной области.
2. Скачок титрования 0,1 М уксусной кислоты намного меньше, чем соляной или другой сильной кислоты.
3. Кривая несимметрична относительно линии нейтральности
|
|
|

Своеобразие русской архитектуры: Основной материал – дерево – быстрота постройки, но недолговечность и необходимость деления...

Автоматическое растормаживание колес: Тормозные устройства колес предназначены для уменьшения длины пробега и улучшения маневрирования ВС при...

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...

Типы сооружений для обработки осадков: Септиками называются сооружения, в которых одновременно происходят осветление сточной жидкости...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!