

Биохимия спиртового брожения: Основу технологии получения пива составляет спиртовое брожение, - при котором сахар превращается...

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

Биохимия спиртового брожения: Основу технологии получения пива составляет спиртовое брожение, - при котором сахар превращается...

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...
Топ:
Особенности труда и отдыха в условиях низких температур: К работам при низких температурах на открытом воздухе и в не отапливаемых помещениях допускаются лица не моложе 18 лет, прошедшие...
Марксистская теория происхождения государства: По мнению Маркса и Энгельса, в основе развития общества, происходящих в нем изменений лежит...
Характеристика АТП и сварочно-жестяницкого участка: Транспорт в настоящее время является одной из важнейших отраслей народного хозяйства...
Интересное:
Искусственное повышение поверхности территории: Варианты искусственного повышения поверхности территории необходимо выбирать на основе анализа следующих характеристик защищаемой территории...
Берегоукрепление оползневых склонов: На прибрежных склонах основной причиной развития оползневых процессов является подмыв водами рек естественных склонов...
Национальное богатство страны и его составляющие: для оценки элементов национального богатства используются...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Явление концентрирования газов на границе твёрдое тело-газ было открыто в конце XVIII в. независимо шведским химиком и фармацевтом К. Шееле (1742 – 1786) и итальянским профессором Ф. Фонтана (1730 – 1805).
Ф. Фонтана обнаружил, что свежепрокаленный древесный уголь обладает способностью поглощать различные газы. К. Шееле установил, что в ряде случаев этот процесс обратим: при изменении условий поглощенный газ может выделяться.
Твёрдое тело, на поверхности которого происходит адсорбция, называется адсорбентом; вещество, которое адсорбируется на поверхности адсорбента, называется адсорбтивом или адсорбатом.
Любая твёрдая поверхность при рассмотрении в электронном микроскопе оказывается шероховатой. Наличие таких неровностей (микродефектов) обуславливает некоторый избыточный запас поверхностной энергии Гиббса системы. Эта энергия тем больше, чем больше удельная поверхность системы.
Адсорбция обусловлена силами, действующими на поверхности адсорбента. Эти силы имеют ту же природу, что и силы молекулярного притяжения (ван-дерваальсовы силы), обусловливающие, например, конденсацию пара в жидкость. Так же, как в жидкости, силовое поле любой молекулярной частицы адсорбента, находящейся в его объеме, полностью компенсировано силовыми полями соседних частиц. Силовые поля частиц адсорбента, расположенных на его поверхности, компенсированы частично. Поэтому, на поверхности адсорбента действуют остаточные силы, способные притягивать молекулы веществ, находящихся в контакте с поверхностью адсорбента. В энергетическом отношении участки поверхности твёрдого тела неравноценны. Адсорбция в первую очередь происходит на участках поверхности с наибольшим локальным запасом поверхностной энергии Гиббса.
|
|
Характер адсорбционных явлений на границе твёрдый адсорбент – газ (пар) описывается теорией И. Ленгмюра. И. Ленгмюр исходил из следующих молекулярно-кинетических положений:
1. Адсорбция вызывается силами, близкими к химическим.
2. Адсорбция молекул адсорбата происходит не всей поверхности адсорбента, а только на вполне определённых её участках, называемых адсорбционными центрами.
3. Адсорбционный центр удерживает только одну молекулу адсорбата. При больших давлениях адсорбционных центров образуется мономолекулярный слой, соответствующий адсорбции.
4. Адсорбционный процесс находится в динамическом равновесии с процессом десорбции. При равновесии скорости адсорбции и десорбции равны. На основании этих положений Ленгмюр вывел уравнение изотермы адсорбции:
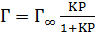 ;
;
где Г∞ – количество адсорбтива, адсорбированное единицей массы адсорбента и соответствующее, по-иному, заполнению всех активных центров; К – константа адсорбционного равновесия
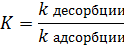
или 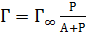 ,
,
где А=1/К, Р – давление газа. Это уравнение хорошо описывает экспериментальные данные, объясняя линейную зависимость адсорбции при малых концентрациях (давлениях):
при Р → 0, Г=Г∞∙Р,
а также адсорбции к насыщению при высоких концентрациях (давлениях) газообразных веществ:
при Р → ∞ 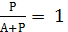 и Г = Г∞
и Г = Г∞
Адсорбция газов существенно зависит от температуры. Чем выше температура, тем меньше адсорбция, поскольку в этом случае молекулы газа обладают большей кинетической энергией и легче отрываются от поверхности адсорбента (рис. 8).
| Г моль м2 |
| Т3 |
| Т2 |
| Т1 |
| Т |
Рис. 8. Зависимость адсорбции от температуры (Т1 > Т2 > Т3)
На практике чаще приходится иметь дело с адсорбцией твёрдым адсорбентом не одного какого-либо газа или пара, а сразу нескольких, поэтому изучение адсорбции из смеси особенно важно. Именно на этом основано применение противогаза, когда через адсорбент должно проходить не только отравляющее вещество, но и в большем количестве кислород и азот воздуха.
|
|
На адсорбции из смеси газов основано кондиционирование воздуха. Из смеси газов каждый её компонент адсорбируется хуже, чем, если бы он адсорбировался в чистом виде, причём газ, имеющий большую адсорбционную способность, лучше адсорбируется и из смеси.
Таким образом, адсорбция газов на твёрдых поверхностях – процесс сложный, зависящий от природы адсорбента, адсорбтива и от внешних условий – давления, температуры. Очень часто изотермы адсорбции имеют более сложный вид (S – образный, ступенчатый) (рис. 9). Для объяснения подобных кривых привлекается теория полимолекулярной адсорбции Поляни или теория Брунауэра, Эммета и Теллера (БЭТ). Основные положения этой теории следующие:
1. На поверхности адсорбента имеется определенное число равноценных в энергетическом смысле активных центров.
2.Взаимодействие соседних адсорбированных молекул в первом и последних слоях отсутствуют.
3.Каждая молекула предыдущего слоя представляет собой возможный активный центр для адсорбции следующего адсорбционного слоя (рис. 10).
4.Предполагается, что все молекулы во втором и более далеких слоях ведут себя подобно молекулам жидкости.
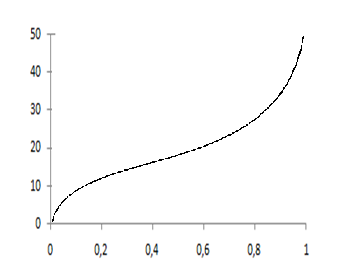
| Г, моль/м2 |
| С(х), моль/дм3 |
| Рис. 9. Изотерма полимолекулярной адсорбции |
Рис. 10. Схема строения адсорбционного слоя по теории БЭТ
Адсорбционная способность зависит от пористости и физического состояния адсорбента. Аморфные адсорбенты обычно лучше адсорбируют газ, чем кристаллические, это объясняется, очевидно, тем, что поверхность аморфного адсорбента шероховата, в то время как поверхность кристалла, за исключением рёбер и углов, гладкая.
Пористые адсорбенты применяют в виде гранул и таблеток. В качестве тонкопористых адсорбентов наиболее часто применяют древесный уголь, животный (костный) уголь, силикагель, различные природные силикаты, алюмогель, алюмосиликаты.
|
|
В последнее время широкое применение в качестве адсорбентов получили молекулярные сита. Примером таких сит являются цеолиты, кристаллы которых построены из чередующихся кремне - и алюмокислородных тетраэдров и содержат поры диаметром (4–7.5)·10-10 м в зависимости от типа цеолита.
Адсорбция из растворов
Адсорбция растворённых веществ твёрдыми адсорбентами является более сложным процессом, чем адсорбция газов твёрдыми телами, так как она осложнена рядом факторов:
1) присутствием третьего компонента – растворителя, молекулы которого могут конкурировать с молекулами адсорбента за места на поверхности адсорбента;
2) взаимодействием между молекулами адсорбата и растворителя;
3) электростатическим взаимодействием между поверхностью адсорбента и молекулами адсорбата, если он является электролитом.
Явление адсорбции из растворов твердыми телами было открыто и изучено в 1785г. русским химиком и фармацевтом Т. Е. Ловицем. Различают два вида адсорбции из раствора на твёрдых адсорбентах: молекулярную, т.е. адсорбцию неэлектролитов или слабых электролитов, когда адсорбируются молекулы адсорбтива, и ионную адсорбцию сильных электролитов, когда избирательно адсорбируются один из ионов электролита.
Молекулярная адсорбция
Неэлектролиты и слабые электролиты на поверхности адсорбента адсорбируются из растворов в виде молекул. Такой процесс называется молекулярной адсорбцией.
Большое влияние на адсорбцию молекул растворённого вещества оказывает природа растворителя и адсорбента, температура, удельная поверхность адсорбента. Твердые поверхности можно разделить на гидрофильные, если они хорошо смачиваются водой, и гидрофобные, если они не смачиваются. Из наиболее широко применяемых на практике гидрофильной поверхностью обладают силикагели, глины; гидрофобной – угли, графит, тальк, парафин и другие.
Советский физико-химик П. А. Ребиндер сформулировал правило выравнивания полярности фаз, согласно которому растворённое вещество тем лучше адсорбируется, чем больше разность полярностей между ним и растворителем:
|
|
ε адсорбента ˂ ε адсорбтива ˂ ε растворителя
Отсюда вытекает, что:
- на полярных адсорбентах лучше адсорбируются полярные адсорбаты из малополярных растворителей; на полярных адсорбентах – неполярные адсорбаты из полярный растворителей;
- чем лучше в данном растворителе растворяется данный адсорбат, тем он хуже адсорбируется; чем хуже растворяется – тем лучше из него адсорбируется.
При этом на границе раздела адсорбент – среда дифильные молекулы будут адсорбироваться таким образом, чтобы полярная часть молекулы была обращена к полярной фазе, а неполярная – к неполярной (рис. 10).
| Бензол (неполярный растворитель) |
| Вода (полярный растворитель) |
| Силикагель (полярный адсорбент) |
| Активированный уголь (неполярный адсорбент) |
Рис. 10. Ориентирование молекул ПАВ на границе твёрдое тело – раствор
В системах неполярный растворитель - малополярный адсорбент адсорбция ПАВ подчиняется правилу Дюкло – Траубе. При адсорбции ПАВ из неполярных растворителей полярными адсорбентами выполняется обращённое правило Дюкло – Траубе: с ростом длинны углеводородного радикала адсорбция уменьшается.
Механизмы молекулярной адсорбции лежат в основе одного из самых современных методов лечения – гемосорбции, т.е. очистки крови от токсичных веществ с помощью различных адсорбентов. В медицинской практике этот метод применяется при почечной недостаточности, при сильных отравлениях снотворными, фосфорорганическими соединениями.
|
|
|

Типы сооружений для обработки осадков: Септиками называются сооружения, в которых одновременно происходят осветление сточной жидкости...

Двойное оплодотворение у цветковых растений: Оплодотворение - это процесс слияния мужской и женской половых клеток с образованием зиготы...

Поперечные профили набережных и береговой полосы: На городских территориях берегоукрепление проектируют с учетом технических и экономических требований, но особое значение придают эстетическим...

Индивидуальные очистные сооружения: К классу индивидуальных очистных сооружений относят сооружения, пропускная способность которых...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!