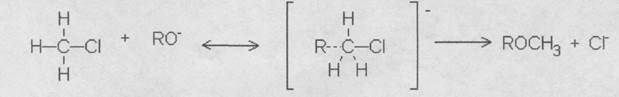Введение
Метилцеллюлоза является первым членом гомологического ряда 0-алкильных производных целлюлозы (простых эфиров). По степени замещения метиловые эфиры целлюлозы можно разделить на низкозамещенные, растворимые в водных растворах сильных щелочей определенной концентрации, и высокозамещенные, растворимые как в воде, так и в органических растворителях. Метиловые эфиры целлюлозы могут быть получены при реакции целлюлозы с различными алкилирующими реагентами: диметилсульфатом, хлористым (или йодистым и бромистым) метилом, диазометаном, метиловым эфиром бензолсульфоновой кислоты. В настоящее время метилцеллюлоза (главным образом водорастворимая) является промышленным продуктом.
Препараты 0-карбоксиметилцеллюлозы в зависимости от степени замещения, так же как и других 0-алкильных производных, можно разделить на низкозамещенные и высокозамещенные. Получение препаратов КМЦ со степенью замещения γ более 100, однако, весьма затруднено ввиду электростатических эффектов отталкивания заряженных одноименно групп (хлорацетатного иона и карбоксиметильной группы). Поэтому практически «высокозамещенными» препаратами КМЦ являются продукты, имеющие степень замещения γ=50—100 и являющиеся водорастворимыми.
Получение метилцеллюлозы
В промышленности для получения метилцеллюлозы чаще всего применяют метод, основанный на алкилировании щелочной целлюлозы хлористым метилом [1].
Процесс алкилирования алкилгалогенидами происходит при температурах 353—373 К. Так как хлористый метил имеет точку кипения 248К, реакция алкилирования производится в автоклавах под высоким давлением.
В процессе алкилирования происходят побочные реакции между хлористым метилом и щелочью с образованием спирта и соли и между спиртом и хлористым метилом с образованием диметилового эфира:
NaOH+CH3Cl+CH3OH→CH3OCH3+NaCl+H2O
CH3Cl+NaOH→CH3OH+NaCl
Поэтому необходимо применять избыток хлористого метила и значительное количество твердой щелочи, так как с увеличением концентрации щелочи разложение хлористого метила уменьшается.
Легче всего подвергается обмену (наиболее подвижен) атом йода, что связано с его большей поляризуемостью, однако алкилиодиды относительно дороги. Хлориды и бромиды мало различаются по реакционной способности, поэтому в промышленных синтезах предпочитают использовать более доступные хлористые алкилы.
| Первичные (и вторичные) галоидопроизводные реагируют через переходное соединение[2]:
|
Скорость реакции, протекающей через переходное состояние, пропорциональна концентрации каждого из реагентов. Следует полагать, что и реакция целлюлозы с хлористым метилом происходит по указанной выше схеме, т. е. является бимолекулярной реакцией нуклеофильного замещения –SN2.
Получение метилцеллюлозы связано с определенными трудностями ввиду больших расходов реагентов, необходимости работы под давлением и т. п. Поэтому изыскание новых путей синтеза метилцеллюлозы имеет большое практическое значение. С этой точки зрения представляются интересными работы [3,4]. Авторами были применены в качестве алкилирующих агентов эфиры ароматических сульфокислот, а именно эфиры п-толуолсульфоки- слоты, толуолдисульфокислоты, бензолсульфокислоты и нафталинсульфокислоты.
Алкилирование этими эфирами идет по схеме:
С6Н7О2(ОН)3 +xRSO2OR'→С6Н7О2(ОН)3-х(ОR')x+ xRSО2ОН,
где R= —С6Н5, —СН3С6Н4, —С10Н7; R'= —СН3, —С2Н5 и т. п.
Было установлено, что с ростом длины алкилирующего радикала скорость реакции уменьшается. Основываясь на экспериментальных данных, можно расположить эфиры сульфокислот в следующий ряд по реакционной способности:
С6Н5SО2ОСН3 > С6Н5SО2ОС2Н5 > С6Н5SО2ОС6Н7.
Наиболее часто для алкилирования целлюлозы в лабораторных условиях применяют диметилсульфат (СН3)2S04, который имеет температуру кипения 461К и позволяет получать продукты при нормальном давлении. Но, несмотря на это, применение его в производстве ограничено из-за высокой токсичности. Образование простого эфира целлюлозы в случае действия диметилсульфата может быть выражено в общем виде следующим уравнением:
С6Н7О2(ОН)3 + x(СН3)2SО4 → СбН7O2(ОН)3-x(ОСH3)x + xСН3ОSО3Na + xН2О.
Одновременно с основной реакцией алкилирования целлюлозы протекает и побочная реакция разложения диметилсульфата по схеме:
(СН3)2SО4 + 2NаОН → Nа2SО4 + 2СН3ОН.
Образующаяся при главной реакции метилсерная кислота может реагировать с метиловым спиртом, давая диметиловый эфир и в присутствии избытка щелочи сульфат Nа:

Реакция метилирования протекает только в щелочной среде, что, очевидно, связано с преимущественным реагированием целлюлозы в виде диссоциированного щелочного соединения.
Получение полностью замещенных продуктов при метилировании целлюлозы по этому методу встречает значительные трудности. Так, после 18 — 20 операций метилирования хлопка Денхам и Вудхоуз[5] получили продукт с содержанием 44.6 % ОСН3 (теоретическая величина для триметилцеллюлозы 45.58 %ОСН3), а Ирвайн и Хирст[5] - - с содержанием 42 — 43 %ОСН3; Берль и Шупп[5] после 28-кратного метилирования получили эфир с содержанием 44.9 %ОСН3.
Существование вышеописанной побочной реакции является одной из причин, обусловливающих трудность получения высокозамещенного продукта. Разложение диметилсульфата во время получения метилцеллюлозы требует применения его большого избытка, что, в свою очередь, приводит к необходимости использовать и большой избыток щелочи, ибо реакция среды всегда должна оставаться щелочной.
Было установлено, что при более высокой концентрации щелочи удается получить более высокую степень замещения метилцеллюлозы[5,6]. Этот факт объясняют различными причинами. Во-первых, было показано, что степень разложения диметилсульфата уменьшается при увеличении концентрации щелочи. Во-вторых, можно предположить, что при повышении концентрации NаОН сдвигается вправо равновесие в системе
С6Н7О2(ОН)3 + Na+ + ОН − → С6Н7О2(ОН)2О − + Nа+ + Н2О.
Однако в ряде случаев удается получить высокозамещенную метилцеллюлозу и без многократных повторений метилирования.
Так, Хэуорз и др. [7], предварительно размельчив фильтровальную бумагу до состояния тонкого порошка и суспендировав ее в ацетоне, получили содержание метоксилов 45 % уже после 2-кратного метилирования. Наиболее просто высокое содержание метоксилов может быть получено при растворении вторичной ацетилцеллюлозы в ацетоне и постепенном добавлении диметилсульфата и водной щелочи. Таким путем в одну операцию может быть достигнуто содержание метоксилов в продукте реакции близкое к 45 % [5].
Применение метилцеллюлозы
Наибольшее значение получили высокозамещенные растворимые в воде препараты метилцеллюлозы (γ=150—200) [5]. Эти продукты обладают комплексом ценных технических свойств и выпускаются промышленностью в виде мелких гранул или порошка белого или слегка желтоватого цвета. Практически не имеют запаха и вкуса. При температуре 433 К окрашиваются и разлагаются. Водные растворы метилцеллюлозы дают нейтральную реакцию.
В большинстве случаев метилцеллюлозу применяют для загущения водной среды. Эффективность загущения зависит от вязкости (т. е. от степени полимеризации). Метилцеллюлоза позволяет водонерастворимые вещества переводить в водной среде в устойчивое тонкодисперсное состояние, так как она образует гидрофильные мономолекулярные защитные слои вокруг отдельных частиц.
Ценными свойствами метилцеллюлозы являются ее высокое связующее действие для пигментов, высокая адгезия в сухом состоянии и способность образовывать пленки. Эти интересные свойства используются при приготовлении водных малярных красок и клеящих веществ. Особенно пригодны для этого метилцеллюлозы с низкой величиной вязкости, так как их можно наносить на самые различные подложки.
В текстильной промышленности метилцеллюлоза используется в качестве шлихты для шерстяной основы и для мягкого аппретирования тканей с целью получения элегантного грифа и глянца.
Метилцеллюлоза с успехом применяется в мыловаренной промышленности. В фармацевтической практике она используется в качестве обезжиренной основы для так называемых слизистых и эмульсионных мазей типа масло/вода, которые служат для защиты кожи от световых ожогов и для обработки ран. Кроме того, метилцеллюлоза служит самостоятельным лекарственным препаратом.
В косметике водорастворимые простые эфиры целлюлозы используют для получения зубных паст и элексиров, защитных эмульсий и обезжиренных кремов для кожи.
Во всевозможных эмульсиях метилцеллюлозу применяют в качестве эмульгаторов и стабилизаторов для растительных масел.
Очень широко используется она также в пищевой промышленности.
Так, в производстве мороженого ее применение обеспечивает необходимую пышность, стабильность и вкус. Метилцеллюлоза используется в ароматических эмульсиях, подливах, для фруктовых соков, консервов и т. д.
Любопытное применение в пищевой промышленности находит способность растворов метилцеллюлозы желатинизироваться при нагревании. Так, например, добавление метилцеллюлозы к фруктовым начинкам пирогов или к сладкой начинке из варенья препятствует вытеканию этих компонентов при выпечке, что значительно улучшает внешний вид и сохраняет вкус изделий.
На карандашных фабриках метилцеллюлоза используется вместо гуммитрагаканта для цветных и копировальных стержней, для пастельных стержней, школьных мелков и красок и т. д.
Таким образом, применение водорастворимой метилцеллюлозы, хотя и является меньшим по масштабу, чем КМЦ, чрезвычайно разнообразно.
Что же касается низкозамещенной (щёлочерастворимой) метил-целлюлозы, то она не получила пока значительного применения.
Литература
1. Прокофьева М.В., Родионов Н.А., Козлов М.П.//Химия и технология
производных целлюлозы. Владимир, 1968.С. 118.
2. Несмеянов А.Н., Несмеянов Н.А. Начала органической химии. М.,1969.Т.1.
663с.
3. Плиско Е.А.//ЖОХ.1958. Т. 28, № 12. С, 3214.
4. Плиско Е.А.//ЖОХ.1961. Т. 31, №2. С. 474
5. Heuser E. The Chemistry of Cellulose. New York, 1944. 660 p.
6. Глузман MX., Левитская И.Б. //ЖПХ. 1960. Т. 33, N 5. С. 1172
7. Петропавловский Г.А., Васильева Г.Г., Волкова Л. А. // Cell. Chem.
Technol. 1967. Vol. 1, N2. P. 211.
8. Никитин Н.И., Петропавловский Г.А. //ЖПХ. 1956. Т. 29. С. 1540
9. Петропавловский Г.А., Никитин Н.И. //Тр. Ин-та леса АН СССР. 1958. Т.45.
С. 140.
10. Васильева Г.Г. Свойства щелочерастворимой карбоксиметилцеллюлозы и
возможности ее использования в бумажной промышленности: Дис. канд.
техн. наук. Л. 1960.
11. VinkH. //Macromoleculare Chemie. 1966. Bd. 94. S. 1.
12. Vole K., Meyerhoff G. //Macromoleculare Chemie. 1961. Bd. 47. S. 168.
13. NeelyW.B.//J. Organ. Chem. 1961. Vol. 26. P. 3015.
14. Savage A.B. //Ind. Eng. Chem. 1957. Vol. 49. P. 99.
15. Allgen L. //J. Polymer Sci. 1954. Vol. 14, N 75.P. 281.
16. Подгородецкий Е. К. Технология производства пленок из
высокомолекулярных соединений. М: Искусство, 1953. 77 с.
Оглавление
Введение стр. 2
Получение метилцеллюлозы стр. 2
Получение карбоксиметилцеллюлозы стр. 4
Свойства растворов метилцеллюлозы стр. 6
Свойства водорастворимой метилцеллюлозы стр. 8
Свойства растворов карбоксиметилцеллюлозы стр. 11
Свойства регенерированной из растворов метилцеллюлозы
(пленок) стр. 12
Свойства регенерированной из щелочного раствора Na-КМЦ
(в виде пленок) стр. 15
Применение метилцеллюлозы стр. 16
Применение карбоксиметилцеллюлозы стр. 18
Литература стр. 19
Введение
Метилцеллюлоза является первым членом гомологического ряда 0-алкильных производных целлюлозы (простых эфиров). По степени замещения метиловые эфиры целлюлозы можно разделить на низкозамещенные, растворимые в водных растворах сильных щелочей определенной концентрации, и высокозамещенные, растворимые как в воде, так и в органических растворителях. Метиловые эфиры целлюлозы могут быть получены при реакции целлюлозы с различными алкилирующими реагентами: диметилсульфатом, хлористым (или йодистым и бромистым) метилом, диазометаном, метиловым эфиром бензолсульфоновой кислоты. В настоящее время метилцеллюлоза (главным образом водорастворимая) является промышленным продуктом.
Препараты 0-карбоксиметилцеллюлозы в зависимости от степени замещения, так же как и других 0-алкильных производных, можно разделить на низкозамещенные и высокозамещенные. Получение препаратов КМЦ со степенью замещения γ более 100, однако, весьма затруднено ввиду электростатических эффектов отталкивания заряженных одноименно групп (хлорацетатного иона и карбоксиметильной группы). Поэтому практически «высокозамещенными» препаратами КМЦ являются продукты, имеющие степень замещения γ=50—100 и являющиеся водорастворимыми.
Получение метилцеллюлозы
В промышленности для получения метилцеллюлозы чаще всего применяют метод, основанный на алкилировании щелочной целлюлозы хлористым метилом [1].
Процесс алкилирования алкилгалогенидами происходит при температурах 353—373 К. Так как хлористый метил имеет точку кипения 248К, реакция алкилирования производится в автоклавах под высоким давлением.
В процессе алкилирования происходят побочные реакции между хлористым метилом и щелочью с образованием спирта и соли и между спиртом и хлористым метилом с образованием диметилового эфира:
NaOH+CH3Cl+CH3OH→CH3OCH3+NaCl+H2O
CH3Cl+NaOH→CH3OH+NaCl
Поэтому необходимо применять избыток хлористого метила и значительное количество твердой щелочи, так как с увеличением концентрации щелочи разложение хлористого метила уменьшается.
Легче всего подвергается обмену (наиболее подвижен) атом йода, что связано с его большей поляризуемостью, однако алкилиодиды относительно дороги. Хлориды и бромиды мало различаются по реакционной способности, поэтому в промышленных синтезах предпочитают использовать более доступные хлористые алкилы.
| Первичные (и вторичные) галоидопроизводные реагируют через переходное соединение[2]:
|
Скорость реакции, протекающей через переходное состояние, пропорциональна концентрации каждого из реагентов. Следует полагать, что и реакция целлюлозы с хлористым метилом происходит по указанной выше схеме, т. е. является бимолекулярной реакцией нуклеофильного замещения –SN2.
Получение метилцеллюлозы связано с определенными трудностями ввиду больших расходов реагентов, необходимости работы под давлением и т. п. Поэтому изыскание новых путей синтеза метилцеллюлозы имеет большое практическое значение. С этой точки зрения представляются интересными работы [3,4]. Авторами были применены в качестве алкилирующих агентов эфиры ароматических сульфокислот, а именно эфиры п-толуолсульфоки- слоты, толуолдисульфокислоты, бензолсульфокислоты и нафталинсульфокислоты.
Алкилирование этими эфирами идет по схеме:
С6Н7О2(ОН)3 +xRSO2OR'→С6Н7О2(ОН)3-х(ОR')x+ xRSО2ОН,
где R= —С6Н5, —СН3С6Н4, —С10Н7; R'= —СН3, —С2Н5 и т. п.
Было установлено, что с ростом длины алкилирующего радикала скорость реакции уменьшается. Основываясь на экспериментальных данных, можно расположить эфиры сульфокислот в следующий ряд по реакционной способности:
С6Н5SО2ОСН3 > С6Н5SО2ОС2Н5 > С6Н5SО2ОС6Н7.
Наиболее часто для алкилирования целлюлозы в лабораторных условиях применяют диметилсульфат (СН3)2S04, который имеет температуру кипения 461К и позволяет получать продукты при нормальном давлении. Но, несмотря на это, применение его в производстве ограничено из-за высокой токсичности. Образование простого эфира целлюлозы в случае действия диметилсульфата может быть выражено в общем виде следующим уравнением:
С6Н7О2(ОН)3 + x(СН3)2SО4 → СбН7O2(ОН)3-x(ОСH3)x + xСН3ОSО3Na + xН2О.
Одновременно с основной реакцией алкилирования целлюлозы протекает и побочная реакция разложения диметилсульфата по схеме:
(СН3)2SО4 + 2NаОН → Nа2SО4 + 2СН3ОН.
Образующаяся при главной реакции метилсерная кислота может реагировать с метиловым спиртом, давая диметиловый эфир и в присутствии избытка щелочи сульфат Nа:

Реакция метилирования протекает только в щелочной среде, что, очевидно, связано с преимущественным реагированием целлюлозы в виде диссоциированного щелочного соединения.
Получение полностью замещенных продуктов при метилировании целлюлозы по этому методу встречает значительные трудности. Так, после 18 — 20 операций метилирования хлопка Денхам и Вудхоуз[5] получили продукт с содержанием 44.6 % ОСН3 (теоретическая величина для триметилцеллюлозы 45.58 %ОСН3), а Ирвайн и Хирст[5] - - с содержанием 42 — 43 %ОСН3; Берль и Шупп[5] после 28-кратного метилирования получили эфир с содержанием 44.9 %ОСН3.
Существование вышеописанной побочной реакции является одной из причин, обусловливающих трудность получения высокозамещенного продукта. Разложение диметилсульфата во время получения метилцеллюлозы требует применения его большого избытка, что, в свою очередь, приводит к необходимости использовать и большой избыток щелочи, ибо реакция среды всегда должна оставаться щелочной.
Было установлено, что при более высокой концентрации щелочи удается получить более высокую степень замещения метилцеллюлозы[5,6]. Этот факт объясняют различными причинами. Во-первых, было показано, что степень разложения диметилсульфата уменьшается при увеличении концентрации щелочи. Во-вторых, можно предположить, что при повышении концентрации NаОН сдвигается вправо равновесие в системе
С6Н7О2(ОН)3 + Na+ + ОН − → С6Н7О2(ОН)2О − + Nа+ + Н2О.
Однако в ряде случаев удается получить высокозамещенную метилцеллюлозу и без многократных повторений метилирования.
Так, Хэуорз и др. [7], предварительно размельчив фильтровальную бумагу до состояния тонкого порошка и суспендировав ее в ацетоне, получили содержание метоксилов 45 % уже после 2-кратного метилирования. Наиболее просто высокое содержание метоксилов может быть получено при растворении вторичной ацетилцеллюлозы в ацетоне и постепенном добавлении диметилсульфата и водной щелочи. Таким путем в одну операцию может быть достигнуто содержание метоксилов в продукте реакции близкое к 45 % [5].
Получение карбоксиметилцеллюлозы
Низкозамещенную Nа-карбоксиметилцеллюлозу получали при взаимодействии щелочной целлюлозы с монохлоруксусной кислотой в различных условиях. В связи с тем, что хлоруксусная кислота является твердым, кристаллическим веществом и для получения низкозамещенных продуктов она требуется в небольшом количестве по сравнению с целлюлозой, особенное значение имеет равномерное распределение реагирующих компонентов смеси. В одном из способов [8,9] реакция была осуществлена путем обработки воздушно-сухой целлюлозы раствором натриевой соли монохлоруксусной кислоты в 17.5— 18%-ном растворе NaOН при жидкостном модуле, равном 5 (отношение количества жидкости в мл к массе целлюлозы в г). Раствор соли приготавливался перед реакцией путем растворения соответствующей навески монохлоруксусной кислоты в щелочи такой концентрации, чтобы после нейтрализации она оставалась в пределах указанной величины.
Степень замещения низкозамещенной Nа-соли карбоксиметилцеллюлозы определяют по содержанию в ней Na.Содержание натрия в карбоксиметилцеллюлозе можно определить весовым методом в виде сульфата, путем озоления навески в тигле, обработки золы серной кислотой и прокаливания при 973 К или объемным методом путем обратного титрования избытка серной кислоты щелочью в присутствии бромфенолсинего в качестве индикатора (область перехода должна быть в кислой среде, чтобы не происходило обратного связывания щелочи карбоксильными группами).
Растворимость, вязкость растворов и другие свойства карбоксиметил- целлюлозы в значительной степени зависят от способа ее получения.
Известно несколько способов получения Nа-КМЦ, основанных на одной и той же реакции:
Целл(ОН)n + 2mNaОН + mСН2С1СООН →
Целл(ОН)n-m(ОСН2СОONa)m + mNаСl + 2mН20,
но выполненных в различных модификациях. Поэтому представляет интерес сравнительное сопоставление образцов Nа-КМЦ, полученных из одной и той же целлюлозы, но различными методами.
Применялись следующие методы получения КМЦ.
1.Мерсеризованная 17.5%-ным раствором NаОН целлюлоза отжималась до 3-кратной массы и обрабатывалась в измельчителе типа Вернера и Пфлейдерера сухой натриевой солью монохлоруксусной кислоты (СН2С1СООNа) при температуре 313 К в течение 30 мин. Затем реакционная смесь выдерживалась в стационарных условиях при 295 К и в течение 24 ч в закрытом сосуде. За это время происходит окислительно-щелочная деструкция целлюлозы: степень полимеризации снижается с 1200 до 300—400 и растворимость образцов КМЦ в воде улучшается. По этому способу алкилирование протекает при максимальных концентрациях действующих масс (целлюлозы и монохлоруксусной кислоты), в результате чего достигается высокая степень алкилирования. Однако условия смешения компонентов реакции не благоприятствуют получению равномерно алкилированных образцов Nа-КМЦ.
П. Воздушно-сухую целлюлозу обрабатывали раствором натриевой соли монохлоруксусной кислоты в 18%-ном растворе NаОН при жидкостном модуле 5 и температуре 313 К. Окислительно-щелочную деструкцию проводили вышеописанным способом 1 после отжима реакционной смеси до
3-кратной массы по отношению к целлюлозе. Этот метод характеризуется равномерным проникновением алкилирующего реагента — монохлоруксусной кислоты — внутрь целлюлозных волокон при набухании, что позволяет получать однородно замещенные продукты [10]. Однако, как было показано [9], большая часть взятого количества СH2СlСООН идет на побочную реакцию ее омыления.
III. Целлюлозу мерсеризовали 18%-ным раствором NаОН. Отжатую до 5-кратной массы алкалицеллюлозу промывали на воронке Бюхнера пропанолом (с настаиванием) от избытка NаОН и воды. Добавляли пропанол до желаемого модуля и помещали целлюлозную массу в измельчитель. После 10 мин измельчения добавляли сухую соль СH2ClCOONa. Реакцию вели при постоянной температуре. По этому способу размеры побочной реакции омыления СН2ClCOONa сведены до минимума, тем самым эффективность использования алкилирующего реагента повышается. Промывка образцов КМЦ во всех случаях проводилась горячим 70%-ным этанолом в аппарате Сокслетта до отрицательной реакции на NаОН по фенолфталеину и на Cl− с раствором AgNO3.
Как видно наибольшая степень замещения при одинаковом количестве СН2С1СООН достигается по способу III - в среде пропанола. Это объясняется, очевидно, уменьшением расхода СH2ClСООН на побочную реакцию омыления.