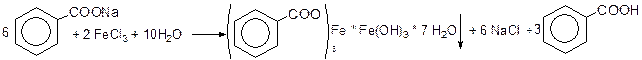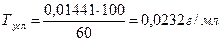Реакции подлинности и количественное определение магния сульфат.
Фармакопейный анализ магния сульфата – MgSO4
Описание
Белый или почти белый кристаллический порошок или бесцветные призматические кристаллы.
Подлинность
Препарат дает характерные реакции на магний и сульфаты:
Mg 2+: 1) К 0,5 мл лекарственной формы прибавляют по 0,3 мл раствора аммония хлорида, натрия фосфата и 0,2 мл раствора аммиака. образуется белый кристаллический осадок, растворимый в разведенных минеральных кислотах и уксусной кислоте.
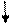 Mg2+ + Na2HPO4 + NH4OH
Mg2+ + Na2HPO4 + NH4OH  MgNH4PO4¯ + 2Na+ + H2O
MgNH4PO4¯ + 2Na+ + H2O
2) 8–оксихинолин в аммиачной среде при рН 9,5–12,7 образует с ионами магния зеленовато-желтый кристаллический осадок внутрикомплексной соли оксихинолята магния Mg(C9H6NO)2·2H2O (нефармакоп):
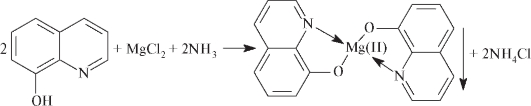
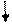 SO 4 2-: К 2 мл раствора сульфата (5 – 50 мг сульфат-иона) прибавляют 0,5 мл бария хлорида раствора 5 %; образуется белый осадок, нерастворимый в разведенных минеральных кислотах.
SO 4 2-: К 2 мл раствора сульфата (5 – 50 мг сульфат-иона) прибавляют 0,5 мл бария хлорида раствора 5 %; образуется белый осадок, нерастворимый в разведенных минеральных кислотах.
MgSO4 + BaCl2 → BaSO4¯ + MgCl2
Количественное определение:
1. Комплексонометрический метод. Вариант прямого титрования. Метод основан на свойстве ионов магния количественно вступать в реакцию с комплексоном (трилоном Б) с образованием прочных, растворимых в воде, бесцветных внутрикомплексных соединений.
Титрант: раствор трилона Б – динатриевая соль этилендиаминотетрауксусной кислоты (сокращенно – Na2H2ТrБ).
Индикаторы: металлоиндикаторы – органические красители, имеющие различную окраску в свободном виде и виде комплекса с металлом, который менее прочный, чем комплекс трилона Б с металлом. Изменение окраски металлоиндикаторов зависит от pH среды.
Определение солей магния проводят в среде аммиачного буфера при рН 9,5-10,0. Индикатор – кислотный хром черный специальный (эриохром черный Т). Переход окраски от красно-фиолетовой к синей.
Магния оксид предварительно растворяют в кислоте хлороводородной разведенной.
Mg2+ + H2Ind ® MgInd + 2H+
Окраска раствора за счет
комплекса металла с индикатором
В точке эквивалентности:
MgInd + Na2H2ТrБ ® MgNa2ТrБ + H2Ind
Окраска раствора за счет
свободного индикатора
fэкв (ЛВ) = 1
2. Ацидиметрический метод нейтрализации (вариант обратного титрования). Используется для количественного определения магния оксида. Метод основан на свойстве магния оксида количественно взаимодействовать с кислотой хлороводородной с образованием соли:
MgO + 2HCI → MgCI2 + 2H2O
Избыток
HCI + NaOH → NaCI + H2O
Остаток
fэкв (магния оксида) = Ѕ
Применение
Магния оксид – антацидное средство с легким послабляющим эффектом.
Магния сульфат – спазмолитическое, противосудорожное, успокаивающее, желчегонное и слабительное средство.
Реакции подлинности и количественное определение гексаметилентетрамина.
Фармакопейный анализ раствора гексаметилентетрамина
Описание
Бесцветный, прозрачный р-р, без запаха, жгучего и сладкого, а затем горького вкуса.
Подлинность
По новой статье: ИК спектр
По ГФ 10.
1) Определяют по запаху.
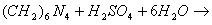
2) По запаху аммиака и посинению красной лакмусовой бумажки.
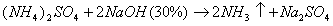
НЕ ГФ.
1. Обнаружение HCHO - реакция серебрянного зеркала, реакция с ауриновым красителем (розовое окрашивание) и с хромотроповой кислотой (фиолетовое окрашивание).
2. Реакция на третичный азот. С осадительными веществами:
с фосфорно-вольфрамовой кислотой -> бел, амфотерный осадок,
с фосфорно-молибденовой кислотой -> желтый осадок,
с пикриновой кислотой -> желтый осадок.
3. С раствором йода дает полийодид, осадок бурого цвета.
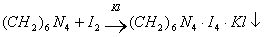
можно использовать эту реакцию для к.о.
4. С бромом образует бледно-желтый осадок, растворимый в избытке реактива.
5. с AgNO3 в нейтральной среде:
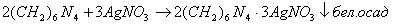
Количественное определение: Обратная ацидиметрия.

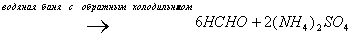
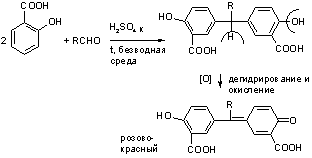
избыток H2SO4 титруем NaOH с индикатором метиленовым Красным.
f=1/4 % = T(NaOH/(CH2)6N4) * (Vконтр(NaOH) - Vопыт(NaOH)) * 100/ a.
Нельзя использовать серную кислоту, т.к. хлорид аммония возгоняется, нельзя использовать ФФ, чтобы не оттитровать (NH4)2SO4.
Не ГФ. Прямая ацидиметрия.
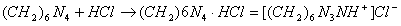
Протон присоединяется по одной электронной паре. Индикатор - смесь МО и МС. Титруют от зеленой окраски до фиолетовой. f=1
2) Йодометрия (используется редко, т.к. необходим специальный титрованный раствор йода).
В результате реакции с йодом образуются перйодиды, которые выпадают в осадок, которые отфильтровывают. Избыток йода титруют тиосульфатом. Если не отфильтровать осадка, он будет разрушаться тиосульфатом.
Контрольный опыт. f=1/4
3) Обратная йодхлорметрия.
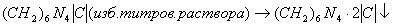
комплекс желтого цвета, устойчивый в нейтральной среде.
избыток ICl + KI -> I2 + KCl
I2 + Na2S2O3 -> NaI + Na2S4O6
f=1/4
4) Аргентометрия.
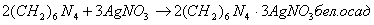
Определяют: гравиметрически, или титруя избыток нитрата серебра по методу Фаянса.
Требование. Лекарственную форму считают выдержавшей испытание, если не более 2 индивидуальных масс отклоняются от средней массы на величину, превышающую допустимое отклонение, указанное в таблице. При этом ни одна индивидуальная масса не должна отклоняться от средней массы на величину, в 2 раза превышающую значение, указанное в таблице. (ОФС.1.4.2.0009.15 Однородность массы дозированных лекарственных форм)
Для определения средней массы таблеток и однородности по массе используют стеклянный или полимерный бюкс известной массы. Среднюю массу таблеток устанавливают взвешиванием вместе 20 таблеток с точностью до 0,001г и рассчитывают по формуле:
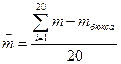 , где
, где 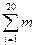 - суммарная масса 20 таблеток, г.
- суммарная масса 20 таблеток, г.
Для определения отклонения отдельных таблеток от средней массы взвешивают порознь каждую из 20 таблеток с точностью до 0,001 г.
Oтклонения отдельной таблетки от средней массы рассчитывают в %
по формуле:
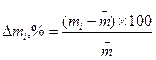
где: 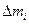 - отклонение отдельной испытуемой таблетки от средней массы, %;
- отклонение отдельной испытуемой таблетки от средней массы, %; 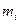 - масса таблетки, г;
- масса таблетки, г; 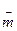 - средняя масса таблеток.
- средняя масса таблеток.
Полученное значение средней массы таблетки оценивают в соответствии с нормативами, приведенными в фармакопейной статье на соответствующую лекарственную форму в разделе «Средняя масса таблетки». Отклонения отдельных таблеток от средней массы (за исключением таблеток, по крытых оболочкой методом наращивания) оценивают, исходя из следующих допустимых пределов:
- для таблеток массой 0,1 г и менее ±10%,
- для таблеток массой более 0,1 г и менее 0,3 г ±7,5%;
- для таблеток массой 0,3 г и более + 5%.
Для таблеток, покрытых оболочкой методом наращивания, масса отдельных таблеток не должна отличаться от средней массы более чем на ± 15%.
Отклонение отдельных таблеток считается соответствующим требованиям нормативной документации, если все значения отклонения от средней массы укладываются в допустимые пределы или только для двух таблеток превышают соответствующие допустимые пределы, но не более чем в 2 раза.
Подлинность.
Кофеин-бензоат натрия
Coffeinum natrio-benzoicum
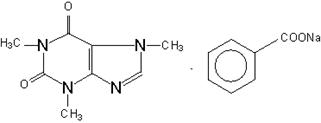
Получение. Взаимодействие водных растворов бензоата натрия и кофеина, полученный раствор выпаривают до образования сухого порошка.
1. реакции на кофеин после выделения щелочью и хлороформом.
2. реакция на бензоат ион с трихлоридом железа образуется осадок телесного цвета.
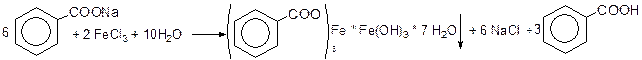
3. препарат дает реакции, характерные для иона натрия.
ГФ X:
1. определение кофеина йодометрическим методом после осаждения его из препарата кислотой в виде основания кофеина, содержание кофеина должно быть 38 - 40% в пересчете на сухое вещество.
Точную навеску препарата растворяют в воде, прибавляют разбавленную серную кислоту и 0,1 М раствор йода, после отстаивания в течение 15 минут раствор фильтруют и в фильтрате избыток йода оттитровывают 0,1 М раствором тиосульфата натрия, в конце титрования прибавляют раствор крахмала.
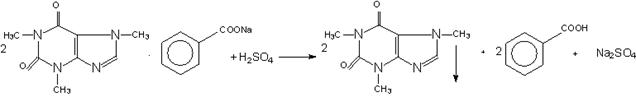
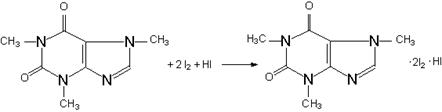
I2 + 2Na2S2O3 = 2NaI + Na2S4O6
УЧ=1/4; формула обратного титрования
2. В другой навеске определяют количество бензоата натрия методом нейтрализации. Титрование ведут в присутствии эфира, который извлекает выделяющуюся бензойную кислоту.
Точную навеску препарата растворяют в воде, прибавляют эфир, смешанный индикатор (метиловый оранжевый и метиленовый синий) и титруют 0,5 М раствором соляной кислоты до появления сиреневой окраски водного слоя
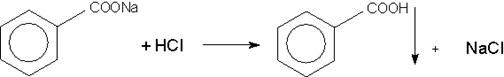
Бензоата натрия должно быть 58 - 62%.
Хранение. в хорошо укупоренной таре.
Применение. Стимулятор ЦНС, кардиотоническое средство.
Формы выпуска. Растворы для инъекций 10, 20%-ный, таблетки 0,1; 0,2.
Вопрос был пустой ес чо
Описание
Белый или почти белый кристаллический порошок или бесцветные кристаллы без запаха или со слабым запахом.
Подлинность
ИК-спектр. Инфракрасный спектр субстанции, снятый в диске с калия бромидом, в области частот от 4000 до 400 см-1, по положению полос поглощения должен соответствовать рисунку спектра стандартного образца ацетилсалициловой кислоты (Приложение).
УФ-спектр. Ультрафиолетовый спектр поглощения 0,007 % раствора субстанции в хлороформе в области от 260 до 350 нм дожен иметь максимум поглощения при 278 нм.
УФ-спектр. Ультрафиолетовый спектр поглощения 0,001 % раствора субстанции в 0,1 М растворе серной кислоты в области от 220 до 350 нм должен иметь максимумы поглощения при 228 нм и 276 нм и минимум поглощения при 257 нм.
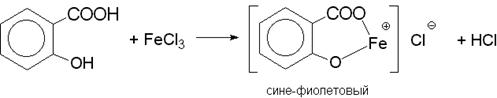
Качественная реакция. 0,5 г субстанции кипятят в течение 3 мин с 5 мл раствора натрия гидроксида, охлаждают, нейтрализуют серной кислотой разведенной 16 %; образуется белый кристаллический осадок. К осадку прибавляют 0,1 мл раствора железа(III) хлорида; должно появиться фиолетовое окрашивание.
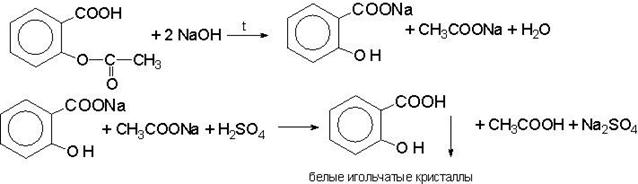
Качественная реакция. К 0,2 г субстанции прибавляют 0,5 мл серной кислоты концентрированной, перемешивают, прибавляют 0,1 мл воды; должен появиться запах уксусной кислоты. Прибавляют 0,1 мл формалина; должно появиться розовое окрашивание.
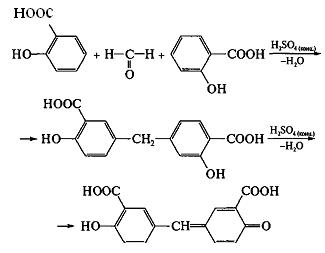
Количественное определение.
1) Метод алкалиметрии.
Точную навеску препарата растворяют в нейтрализованном по фенолфталеину (5—6 капель) спирте и охлаждают до 8 - 9°. Раствор титруют с тем же индикатором 0,1М раствором едкого натра до розового окрашивания.
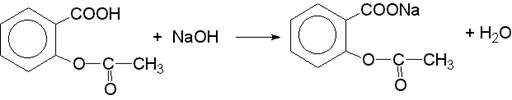
Э = М
Формула прямого титрования.
2) Метод ацидиметрии после гидролиза.
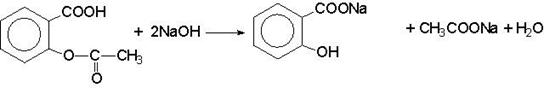
NaOH + HCl = NaCl + H2O
Э = М/2
Формула обратного титрования.
100Методы качественного и кол. определения перекиси водорода.
Описание
Бесцветная прозрачная жидкость.
Подлинность
1. Качественная реакция. К 1 мл субстанции прибавляют 0,2 мл серной кислоты разведенной 16 % и 0,25 мл 0,02 М раствора калия перманганата; раствор должен постепенно обесцветиться с выделением газа.
2. Качественная реакция. К 0,1 мл субстанции прибавляют 0,2 мл серной кислоты разведенной 16 %, 2 мл эфира, 0,2 мл 5 % раствора калия дихромата и взбалтывают; эфирный слой должен окраситься в синий цвет.
Реакции подлинности и количественное определение магния сульфат.
Фармакопейный анализ магния сульфата – MgSO4
Описание
Белый или почти белый кристаллический порошок или бесцветные призматические кристаллы.
Подлинность
Препарат дает характерные реакции на магний и сульфаты:
Mg 2+: 1) К 0,5 мл лекарственной формы прибавляют по 0,3 мл раствора аммония хлорида, натрия фосфата и 0,2 мл раствора аммиака. образуется белый кристаллический осадок, растворимый в разведенных минеральных кислотах и уксусной кислоте.
 Mg2+ + Na2HPO4 + NH4OH
Mg2+ + Na2HPO4 + NH4OH  MgNH4PO4¯ + 2Na+ + H2O
MgNH4PO4¯ + 2Na+ + H2O
2) 8–оксихинолин в аммиачной среде при рН 9,5–12,7 образует с ионами магния зеленовато-желтый кристаллический осадок внутрикомплексной соли оксихинолята магния Mg(C9H6NO)2·2H2O (нефармакоп):

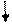 SO 4 2-: К 2 мл раствора сульфата (5 – 50 мг сульфат-иона) прибавляют 0,5 мл бария хлорида раствора 5 %; образуется белый осадок, нерастворимый в разведенных минеральных кислотах.
SO 4 2-: К 2 мл раствора сульфата (5 – 50 мг сульфат-иона) прибавляют 0,5 мл бария хлорида раствора 5 %; образуется белый осадок, нерастворимый в разведенных минеральных кислотах.
MgSO4 + BaCl2 → BaSO4¯ + MgCl2
Количественное определение:
1. Комплексонометрический метод. Вариант прямого титрования. Метод основан на свойстве ионов магния количественно вступать в реакцию с комплексоном (трилоном Б) с образованием прочных, растворимых в воде, бесцветных внутрикомплексных соединений.
Титрант: раствор трилона Б – динатриевая соль этилендиаминотетрауксусной кислоты (сокращенно – Na2H2ТrБ).
Индикаторы: металлоиндикаторы – органические красители, имеющие различную окраску в свободном виде и виде комплекса с металлом, который менее прочный, чем комплекс трилона Б с металлом. Изменение окраски металлоиндикаторов зависит от pH среды.
Определение солей магния проводят в среде аммиачного буфера при рН 9,5-10,0. Индикатор – кислотный хром черный специальный (эриохром черный Т). Переход окраски от красно-фиолетовой к синей.
Магния оксид предварительно растворяют в кислоте хлороводородной разведенной.
Mg2+ + H2Ind ® MgInd + 2H+
Окраска раствора за счет
комплекса металла с индикатором
В точке эквивалентности:
MgInd + Na2H2ТrБ ® MgNa2ТrБ + H2Ind
Окраска раствора за счет
свободного индикатора
fэкв (ЛВ) = 1
2. Ацидиметрический метод нейтрализации (вариант обратного титрования). Используется для количественного определения магния оксида. Метод основан на свойстве магния оксида количественно взаимодействовать с кислотой хлороводородной с образованием соли:
MgO + 2HCI → MgCI2 + 2H2O
Избыток
HCI + NaOH → NaCI + H2O
Остаток
fэкв (магния оксида) = Ѕ
Применение
Магния оксид – антацидное средство с легким послабляющим эффектом.
Магния сульфат – спазмолитическое, противосудорожное, успокаивающее, желчегонное и слабительное средство.



 Mg2+ + Na2HPO4 + NH4OH
Mg2+ + Na2HPO4 + NH4OH  MgNH4PO4¯ + 2Na+ + H2O
MgNH4PO4¯ + 2Na+ + H2O
 SO 4 2-: К 2 мл раствора сульфата (5 – 50 мг сульфат-иона) прибавляют 0,5 мл бария хлорида раствора 5 %; образуется белый осадок, нерастворимый в разведенных минеральных кислотах.
SO 4 2-: К 2 мл раствора сульфата (5 – 50 мг сульфат-иона) прибавляют 0,5 мл бария хлорида раствора 5 %; образуется белый осадок, нерастворимый в разведенных минеральных кислотах.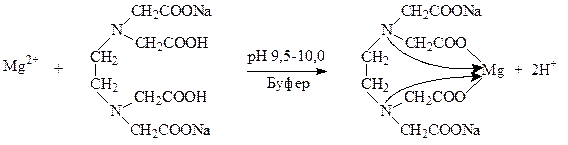
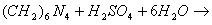
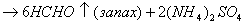
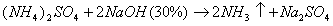
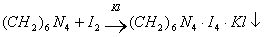
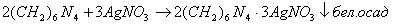

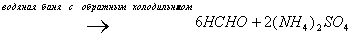

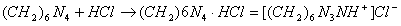
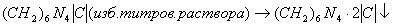
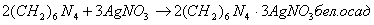
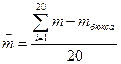 , где
, где 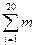 - суммарная масса 20 таблеток, г.
- суммарная масса 20 таблеток, г.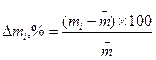
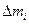 - отклонение отдельной испытуемой таблетки от средней массы, %;
- отклонение отдельной испытуемой таблетки от средней массы, %; 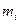 - масса таблетки, г;
- масса таблетки, г; 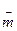 - средняя масса таблеток.
- средняя масса таблеток.