

Состав сооружений: решетки и песколовки: Решетки – это первое устройство в схеме очистных сооружений. Они представляют...

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...

Состав сооружений: решетки и песколовки: Решетки – это первое устройство в схеме очистных сооружений. Они представляют...

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...
Топ:
Процедура выполнения команд. Рабочий цикл процессора: Функционирование процессора в основном состоит из повторяющихся рабочих циклов, каждый из которых соответствует...
Комплексной системы оценки состояния охраны труда на производственном объекте (КСОТ-П): Цели и задачи Комплексной системы оценки состояния охраны труда и определению факторов рисков по охране труда...
Интересное:
Мероприятия для защиты от морозного пучения грунтов: Инженерная защита от морозного (криогенного) пучения грунтов необходима для легких малоэтажных зданий и других сооружений...
Национальное богатство страны и его составляющие: для оценки элементов национального богатства используются...
Что нужно делать при лейкемии: Прежде всего, необходимо выяснить, не страдаете ли вы каким-либо душевным недугом...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Ход работы. В калориметрический стакан массой 45 г поместить
25 мл 1 н. раствора щелочи и записать показание термометра. В отдельный стакан отмерить 25 мл 1 н. раствора кислоты и измерить температуру. Затем через воронку влить кислоту в калориметр. Отметить самую высокую температуру, которую покажет термометр после сливания растворов.
Опыты проделать по два раза с сильными кислотами и основаниями
NaOH + HCl = NaCl + Н2O
+ 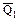 ;
;
Результаты опытов записать в таблицу:
| Измеряемые величины | NaOH+HCl | ||
| Масса калориметрического стакана m1, г | |||
| Концентрация растворов, н. | |||
| Объем каждого раствора V, мл | |||
| Температура щелочи tщ | |||
| Температура кислоты tK | |||
| Начальная температура t = 0,5(tщ +tK) | |||
| Температура после нейтрализации t2 | |||
Общая масса растворов m2 = 2V 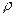
|
По результатам опытов вычислить теплоты нейтрализации, используя формулы:
 = Δt ٠ C/VN,
= Δt ٠ C/VN,
Δt = t2–t1; C = m1с1 + m2c2; с1 = 0,753 Дж/г град;
с2 = 4,184 Дж/г град; 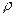 = 1 г/мл,
= 1 г/мл,
где С – общая теплоёмкость стекла и раствора; с1 – удельная теплоёмкость стекла; с2 – удельная теплоёмкость раствора.
Занятие 4
Лабораторная работа
Влияние различных факторов
на положение равновесия химической реакции
Влияние концентрации
К 20 мл воды в небольшом стакане прибавить по 1–2 капли насыщенных растворов FeCl3 и KCSN (или NH4CSN). Полученный раствор разлить в
4 пробирки. В 1-ю добавить несколько капель концентрированного раствора FeCl3, во 2-ю – несколько капель концентрированного раствора KCSN (или NH4CNS), в 3-ю – немного кристаллического КСl (или NH4Cl), 4-ю оставить для сравнения. Пользуясь законом действия масс, объяснить изменение окраски в первых трех пробирках. Результаты записать в таблицу:
|
|
| Добавленный раствор | Изменение интенсивности окраски | Направление смещения равновесия |
| FeCl3 | ||
| KCNS | ||
| КС1 |
Уравнение реакции образования роданида железа (Ш):
FeCl3 + 3KCNS ↔ Fe(CNS)3 + 3KCI.
Роданид железа (Ш) окрашен в красный цвет, FeCl3 – в желтый, а KCNS и КCl – бесцветны.
Влияние температуры
При взаимодействии йода с крахмалом образуется синее вещество сложного состава (соединение включения):
йод + крахмал ↔ соединения включения
В две пробирки налить по 4–5 мл крахмала и добавить 3–4 капли 0,1 н. раствора I2. Нагреть одну из пробирок, а затем снова охладить. Вторую оставить для сравнения. Что происходит? Экзо- или эндотермической является реакция образования йодкрахмала?
Каталитические реакции
1. Сравнение каталитического эффекта фермента каталазы крови, ионов I- и Fe3+ на реакцию разложения перекиси водорода
В четыре пробирки налить по 0,5 мл раствора Н2O2. Затем в каждую пробирку с интервалом 3 мин внести катализаторы. В одну из пробирок добавить 0,2 мл крови (0,1 мл крови разводят в 50 раз).
В остальные две пробирки внести по одной капле поверхностно-активного вещества (сыворотку крови, разведенную в 30 раз) и по 0,2 мл 10 % растворов KI и FeCl3. Перекись водорода и растворы катализаторов перемешать, отметить начало реакции и через 1 мин определить высоту столба пены.
На основании полученных данных сравнить скорость разложения перекиси водорода под действием каталазы и ионов Fe3+ и I-.
Занятие №5
ТЕМА:Кислотно-основные свойства химических соединений
Лабораторная работа
|
|
|

Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций...

Биохимия спиртового брожения: Основу технологии получения пива составляет спиртовое брожение, - при котором сахар превращается...

История развития хранилищ для нефти: Первые склады нефти появились в XVII веке. Они представляли собой землянные ямы-амбара глубиной 4…5 м...

История развития пистолетов-пулеметов: Предпосылкой для возникновения пистолетов-пулеметов послужила давняя тенденция тяготения винтовок...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!