

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...

Эмиссия газов от очистных сооружений канализации: В последние годы внимание мирового сообщества сосредоточено на экологических проблемах...

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...

Эмиссия газов от очистных сооружений канализации: В последние годы внимание мирового сообщества сосредоточено на экологических проблемах...
Топ:
Установка замедленного коксования: Чем выше температура и ниже давление, тем место разрыва углеродной цепи всё больше смещается к её концу и значительно возрастает...
Выпускная квалификационная работа: Основная часть ВКР, как правило, состоит из двух-трех глав, каждая из которых, в свою очередь...
Интересное:
Как мы говорим и как мы слушаем: общение можно сравнить с огромным зонтиком, под которым скрыто все...
Финансовый рынок и его значение в управлении денежными потоками на современном этапе: любому предприятию для расширения производства и увеличения прибыли нужны...
Отражение на счетах бухгалтерского учета процесса приобретения: Процесс заготовления представляет систему экономических событий, включающих приобретение организацией у поставщиков сырья...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Кислоты и их свойства.
Кислоты – это сложные вещества, состоящие из атомов водорода и кислотного остатка.
| HF | Фтороводородная кислота (плавиковая) |
| HCl | Хлороводородная кислота (соляная) |
| HBr | Бромоводородная кислота |
| HI | Йодоводородная кислота |
| H2S | Сероводородная кислота |
| H2SO3 | Сернистая кислота |
| H2SO4 | Серная кислота |
| HNO3 | Азотная кислота |
| HNO2 | Азотистая кислота |
| H3PO4 | Фосфорная (ортофосфорная) кислота |
| H2CO3 | Угольная кислота |
| H2SiO3 | Кремниевая кислота |
Все кислоты обязательно содержат водород, который записывается в формуле на первом месте. Вся остальная часть формулы называется кислотным остатком.
Например, у НСl кислотным остатком является Сl-, а у Н3РО4 кислоьный остаток РО43-.
Классификация кислот.
1) По содержанию кислорода:
Кислоты
По количеству водорода
Кислоты
По растворимости в воде
Кислоты
По стабильности
Кислоты
Физические свойства кислот.
1. Агрегатное состояние: жидкие или твердые (H3PO4, H2SiO3).
2. Кислые на вкус.

 3. Не имеют окраски: растворы HCl, HNO3, H2SO4, H3PO4 и др.
3. Не имеют окраски: растворы HCl, HNO3, H2SO4, H3PO4 и др.
Окрашенные растворы: H2CrO4 , HMnO4 .
H 2 SO 4 - серная кислота - бесцветная жидкость, вязкая, как масло, не имеющая запаха, почти вдвое тяжелее воды. Серная кислота поглощает влагу из вождуха и других газов. Это свойство серной кислоты используют для осушения некоторых газов.
|
|
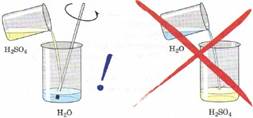
При смешивании серной кислоты с водой выделяется большое количество количество теплоты. Если воду вливать в серную кислоту, то вода, не успев смешаться с кислотой, может закипеть и выбросить брызги серной кислоты на лицо и руки работающего.
Правило разбавления серной кислоты:
При растворении серной кислоты нужно вливать ее тонкой струей в воду и перемешивать.
Серная кислота обугливает древесину, кожу, ткани. Если в пробирку с H2SO4 опустить лучинку, то происходит химическая реакция - лучинка обугливается.
Угольная и сернистая кислоты - H 2 CO 3 и H 2 SO 3 - в свободном виде не существуют, т.к. они легко разлагаются на воду и соответствующий оксид:
H2CO3 → СО2 + Н2О
H2SO3 → SО2 + Н2О
Действие их на индикаторы.
Индикаторы - вещества, изменяющие окраску в зависимости от среды – кислотной или щелочной (лакмус, метилоранж, фенолфталеин).
В кислотах:
| Лакмус | Метилоранж | Фенолфталеин |
| красный | красно-розовый | бесцветный |
Кремниевую кислоту распознать с помощью индикаторов распознать нельзя, т.к. она нерастворима в воде.
Диссоциация кислот.
1) HCl ↔ Н+ + Cl-
2)
|
3) H3PO4 ↔ 3 Н + + PO43-
Химические свойства.
Химические свойства кислот.
Кислоты взаимодействуют с металлами, оксидами металлов, основаниями и солями. Во всех случаях основным продуктом реакции будет соль.
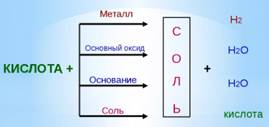
Кислоты и их свойства.
Кислоты – это сложные вещества, состоящие из атомов водорода и кислотного остатка.
| HF | Фтороводородная кислота (плавиковая) |
| HCl | Хлороводородная кислота (соляная) |
| HBr | Бромоводородная кислота |
| HI | Йодоводородная кислота |
| H2S | Сероводородная кислота |
| H2SO3 | Сернистая кислота |
| H2SO4 | Серная кислота |
| HNO3 | Азотная кислота |
| HNO2 | Азотистая кислота |
| H3PO4 | Фосфорная (ортофосфорная) кислота |
| H2CO3 | Угольная кислота |
| H2SiO3 | Кремниевая кислота |
|
|
Все кислоты обязательно содержат водород, который записывается в формуле на первом месте. Вся остальная часть формулы называется кислотным остатком.
Например, у НСl кислотным остатком является Сl-, а у Н3РО4 кислоьный остаток РО43-.
Классификация кислот.
1) По содержанию кислорода:
Кислоты
По количеству водорода
Кислоты
По растворимости в воде
Кислоты
По стабильности
Кислоты
Физические свойства кислот.
1. Агрегатное состояние: жидкие или твердые (H3PO4, H2SiO3).
2. Кислые на вкус.

 3. Не имеют окраски: растворы HCl, HNO3, H2SO4, H3PO4 и др.
3. Не имеют окраски: растворы HCl, HNO3, H2SO4, H3PO4 и др.
Окрашенные растворы: H2CrO4 , HMnO4 .
H 2 SO 4 - серная кислота - бесцветная жидкость, вязкая, как масло, не имеющая запаха, почти вдвое тяжелее воды. Серная кислота поглощает влагу из вождуха и других газов. Это свойство серной кислоты используют для осушения некоторых газов.
При смешивании серной кислоты с водой выделяется большое количество количество теплоты. Если воду вливать в серную кислоту, то вода, не успев смешаться с кислотой, может закипеть и выбросить брызги серной кислоты на лицо и руки работающего.
Правило разбавления серной кислоты:
При растворении серной кислоты нужно вливать ее тонкой струей в воду и перемешивать.

Серная кислота обугливает древесину, кожу, ткани. Если в пробирку с H2SO4 опустить лучинку, то происходит химическая реакция - лучинка обугливается.
Угольная и сернистая кислоты - H 2 CO 3 и H 2 SO 3 - в свободном виде не существуют, т.к. они легко разлагаются на воду и соответствующий оксид:
H2CO3 → СО2 + Н2О
H2SO3 → SО2 + Н2О
Действие их на индикаторы.
Индикаторы - вещества, изменяющие окраску в зависимости от среды – кислотной или щелочной (лакмус, метилоранж, фенолфталеин).
В кислотах:
| Лакмус | Метилоранж | Фенолфталеин |
| красный | красно-розовый | бесцветный |
|
|
|

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций...

Типы сооружений для обработки осадков: Септиками называются сооружения, в которых одновременно происходят осветление сточной жидкости...

Поперечные профили набережных и береговой полосы: На городских территориях берегоукрепление проектируют с учетом технических и экономических требований, но особое значение придают эстетическим...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!