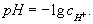Чистая вода, хоть и плохо (по сравнению с растворами электролитов), но может проводить электрический ток. Это вызвано способностью молекулы воды распадаться (диссоциировать) на два иона которые и являются проводниками электрического тока в чистой воде (ниже под диссоциацией подразумевается электролитическая диссоциация - распад на ионы):
H2O ↔ H+ + OH-
Примерно на 556 000 000 не диссоциированных молекул воды диссоциирует только 1 молекула, однако это 60 000 000 000 диссоциированных молекул в 1мм3. Диссоциация обратима, то есть ионы H+ и OH- могут снова образовать молекулу воды. В итоге наступает динамическое равновесие при котором количество распавшихся молекул равно количеству образовавшихся из H+ и OH- ионов. Другими словами скорости обоих процессов будут равны. Для нашего случая, уравнение скорости химической реакции можно написать так:
υ1 = κ1 • [H2O] (для диссоциации воды)
υ2 = κ2 • [H+] • [HO-] (для обратного процесса)
где υ - скорость реакции; κ - константа скорости реакции (зависящая от природы реагирующих веществ и температуры); [H2O], [H+] и [HO-] - концентрации (моль/л).
В состоянии равновесия υ1 = υ2, следовательно:
κ1 • [H2O] = κ2 • [H+] • [HO-]
Проведем нехитрые математические действия и получим:
κ1/κ2 = [H+] • [HO-]/[H2O]
κ1/κ2 = K
K - константа равновесия, а в нашем случаи константа диссоциации, которая зависит от температуры и природы веществ, и не зависящая от концентраций (также как κ1 и κ2). K для воды 1,8•10-16 при 25 °C (справочная величина).
Вследствие очень малого количества продиссоциированных молекул концентрацию [H2O] можно принять равной общей концентрации воды, а общую концентрацию воды в разбавленных растворах как величину постоянную:
[H2O]=1000(г/л)/18(г/моль)=55,6 моль/л.
Заменяя κ1/κ2 на K и используя величину [H2O], определяем чему равно произведение концентраций [H+] и [HO-], которое называется - ионное произведение воды:
K = [H+] • [HO-]/55,6 моль/л
1,8•10-16 • 55,6 моль/л = [H+] • [HO-]
10-14 = [H+] • [HO-]
Так как, при определенной температуре, величины используемые в расчете ионного произведения воды (K, [H2O]) постоянны, значение ионного произведения воды [H+] • [HO-] так же постоянно. А поскольку при диссоциации молекулы воды образуется одинаковое количество ионов [H+] и [HO-], получается что для чистой воды концентрации [H+] и [HO-] будут равны 10-7 моль/л. Из постоянства ионного произведения воды следует, что если количество ионов H+ становится больше, то количество ионов HO- становится меньше. Например, если к чистой воде добавить сильную кислоту HCl, она как сильный электролит вся продиссоциирует на H+ и Cl-, в результате концентрация ионов H+ резко увеличится, и это приведет к увеличению скорости процесса противоположного диссоциации, так как она зависит от концентраций ионов H+ и OH-:
υ2 = κ2 • [H+] • [HO-]
В ходе ускорившегося процесса противоположного диссоциации, концентрация ионов HO- уменьшится до величины соответствующей новому равновесию, при котором их будет так мало, что скорости диссоциации воды и обратного процесса снова будут равны. Если концентрация получившегося раствора HCl равна 0,1моль/л, равновесная концентрация [HO-] будет равна:
[HO-] = 10-14/0,1 = 10-13 моль/л
При добавлении сильного основания NaOH сдвиг будет в сторону уменьшения концентрации H+.
PH воды
Для удобства, концентрации [H+] и [HO-] выражают в виде водородного показателя pH и гидроксильного показателя pOH. pH и pOH - это отрицательные десятичные логарифмы концентраций [H+] и [HO-] (правильнее использовать не концентрацию, а активность) соответственно:
pH = -lg[H+]
pOH = -lg[OH-]
Прологарифмируя уравнение [H+] • [HO-] = 10-14 получим:
lg[H+] + lg[OH-] = -14
-lg[H+] - lg[OH-] = 14
pH + pOH = 14
Получившаяся сумма pH и pOH, также как и произведение, которое логарифмировали, является постоянной и равна 14, так если pH=3 то pOH=11 (pH и pOH могут быть и отрицательными, и если pH=-1 тогда pOH=15).
В зависимости от pH растворы делят на нейтральные, кислые и щелочные. При pH=7 раствор нейтральный, при pH<7 - кислый, при pH>7 - щелочной.
От pH раствора очень сильно зависит протекание многих химических реакций, как на уровне процессов проводящихся в лаборатории и на производстве, так и на уровне реакций в живых организмах, поэтому химикам и биологам с водородным показателем иметь дело приходится очень часто. Все обитатели природных вод и почв адаптированы к определенному водородному показателю, и в случаи его изменения могут погибнуть. Большинство живых организмов могут существовать лишь в средах, близких к нейтральным. Отчасти это связано с тем, что под действием ионов H+ и OH- многие белки, содержащие кислотные или основные группы, изменяют свою конфигурацию и заряд. А в сильнокислой и сильнощелочной средах рвётся пептидная связь, которая соединяет отдельные аминокислотные остатки в длинные белковые цепи. Из-за этого ультраосновные (сильнощелочные) растворы вызывают щелочные ожоги кожи и разрушают шёлк и шерсть, состоящие из белка. Все живые организмы вынуждены поддерживать во внутриклеточных жидкостях определённое значение рН. От величины водородного показателя почвенного раствора зависит урожайность различных культурных растений. На кислых почвах с pH=5-5,5 не развиваются проростки ячменя, но хорошо развивается картофель.
И о нное произвед е ние вод ы, произведение концентраций (точнее активностей) ионов водорода Н+ и ионов гидроксила OH— в воде или в водных растворах: KB = [Н+] [ОН—]
Водор о дный показ а тель, pH, отрицательный десятичный логарифм концентрации (точнее, активности) ионов водорода (в г-ион/л) в данном растворе: