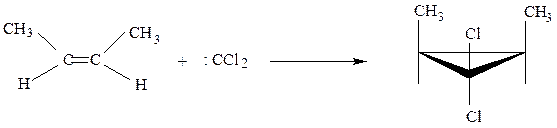С реакциями замещения галогена конкурируют реакции отщепления, которые преобладают при действии сильных оснований (спиртовой раствор щелочи, третичные ароматические амины и др.)
Отщепление галогеноводородов обычно протекает так, что атомы водорода и галогена отщепляется от соседних углеродных атомов (правило Зайцева). Такой процесс называется β-элиминированием.


β-Элиминирование обычно протекает по одному из механизмов: E1 или Е2.
Механизм Е1. Скорость реакции зависит только от концентрации галогенопроизводного v = k • [RHa1]. Медленная стадия, определяющая скорость реакции

Эта стадия совпадает с первой стадией реакции замещения SN 1. Вторая (быстрая) стадия реакции отщепления заключается в отрыве протона

Реакция может протекать и в нейтральной, и в кислой среде. Тогда вторая стадия выглядит так:

Как правило, реакции SN 1 и Е1 протекают одновременно, и образуется смесь продуктов замещения и отщепления.
Механизм Е2. Скорость реакции пропорциональна концентрации галогена и основания. Например, v = k • [RHa1] • [ -ОR ]. Атакующее основание отрывает протон от β-углеродного атома, одновременно с образованием двойной связи и уходом иона галогена


При этом конкурирующей реакцией также является замещение галогена. Элиминирование протекает тем легче, чем сильнее используемое основание

Повышение температуры также способствует преобладанию реакции отщепления над замещением.
Скорость элиминирования производных различных галогенов соответствует связи энергии C–Hal и возрастает в ряду: R–F → R–Сl → R–Br → RI.
В большинстве случаев в результате реакции элиминирования возможно образование двух или даже трех различных алкенов в зависимости от того, какой из β-водородных атомов отщепляется на стадии, определяющей скорость

Направленность реакции подчиняется правилу Зайцева: отщепление галогеноводородов от галогенопроизводного происходит таким образом, что с атомом галогена преимущественно отщепляется водород от соседнего наименее гидрогенизированного атома углерода. Образующийся наиболее полно замещенный этилен термодинамически более стабилен. При механизме Е2 главную роль в такой направленности играет стабильность переходного состояния

Первое переходное состояние стабилизировано эффектом сверхсопряжения трех метильных групп.
В отличие от SN2 в случае Е2 отсутствуют стерические препятствия отщеплению галогена от третичного углеродного атома. Поэтому в большинстве случаев элиминирование протекает именно по Е2. Однако для осуществления этого механизма необходимо, чтобы атомы галогена, отщепляющегося водорода, а также α- и β-углеродные атомы могли расположиться в одной плоскости, причем отщепляющиеся атомы должны в переходном состоянии находиться в транс -положении друг к другу

Освобождающаяся пара электронов связи Сβ–Н атакует «с тыла» атом Сα, вытесняя пару электронов связи Сα–Н на атом хлора.
В случае производных циклогексана отщепляющиеся атомы должны находиться в транс -диаксиальном положении

При невозможности принятия такой конформации протекает элиминирование против правила Зайцева

Дигалогенопроизводные, содержащие атомы галогена при одном и том же (геминальные) или при соседних (вицинальные) атомах углерода, подвергаясь дегидрогалогенированию образуют алкины или диены.


Реакции дегалогенирования. Дегалогенирование (отщепление двух атомов галогена) происходит при действии на дигалогенопроизводное цинка (или магния) в ацетоне или уксусной кислоте. Вицинальные соединения при этом образуют алкены

Реакция протекает по механизму Е2 и подчиняется всем его закономерностям.

При действии цинка на 1,3-; 1,4- и 1,5-дигалогенпроизводные происходит образование циклических соединений. Реакция служит удобным способом получения малых циклов.

α-Элиминирование – отщепление двух заместителей от одного атома углерода. В классе галогенопроизводных реакция распространена для производных метана. При действии сильных оснований от молекулы хлороформа может отщепляться хлороводород

Дихлоркарбен представляет собой бирадикал, имеющий два неспаренных электрона при одном атоме углерода. Он крайне реакционноспособен. Легко присоединяется по двойной связи, образуя производные циклопропана
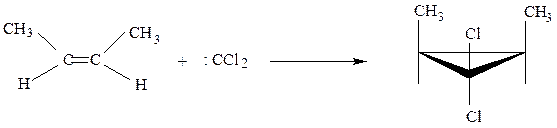
цис -бутен-2 цис -3,3-дихлор-1,2-диметилциклопропан
По-видимому образование обеих связей происходит одновременно, ибо образуется стереоспецифичный продукт

транс -бутен-2 транс -3,3-дихлор-1,2-диметил циклопропан
Незамещенный карбен образуется при α-элиминировании йодистого метилена действием цинка, имеющего омедненную поверхность (цинк-медная пара)

Присоединение карбена к двойной связи (реакция Симмонса-Смта) рассматривалась при изучении свойств алкенов

циклогексен бицикло(4,1,0)гептан