

Археология об основании Рима: Новые раскопки проясняют и такой острый дискуссионный вопрос, как дата самого возникновения Рима...

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

Археология об основании Рима: Новые раскопки проясняют и такой острый дискуссионный вопрос, как дата самого возникновения Рима...

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...
Топ:
Марксистская теория происхождения государства: По мнению Маркса и Энгельса, в основе развития общества, происходящих в нем изменений лежит...
Установка замедленного коксования: Чем выше температура и ниже давление, тем место разрыва углеродной цепи всё больше смещается к её концу и значительно возрастает...
Интересное:
Подходы к решению темы фильма: Существует три основных типа исторического фильма, имеющих между собой много общего...
Финансовый рынок и его значение в управлении денежными потоками на современном этапе: любому предприятию для расширения производства и увеличения прибыли нужны...
Принципы управления денежными потоками: одним из методов контроля за состоянием денежной наличности является...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Для определения ЭДС гальванического элемента необходимо составить этот элемент из двух разных металлических электродов по схеме (рис. 3). Для этого в один стакан налить 50 мл раствора соли, соответствующей помещаемому в этот стакан металлу (например, для цинкового электрода налить раствор ZnSO4 или ZnCl2). В другой стакан налить такой же раствора соли, соответствующей второму из исследуемых металлов. После этого поместить в стаканы электроды, предварительно очистив их наждачной бумагой, промыв дистиллированной водой и просушив фильтровальной бумагой.
Соединить электроды проводником с токоизмеряющим прибором (вольтметром). Для замыкания цепи соединить агар-агаровой трубкой два стакана с растворами. Наличие контакта регистрируется вольтметром. Если ток отсутствует, необходимо проверить надежность контактов. Через 10 минут необходимо замерить величину напряжения в этой системе, то есть экспериментальное значение ЭДС гальванического элемента eэксп.
После этого следует рассчитать теоретическое значение ЭДС изучаемого гальванического элемента, которое будет равно разности потенциалов положительного и отрицательного электродов. Например, для медного и цинкового электродов можно записать
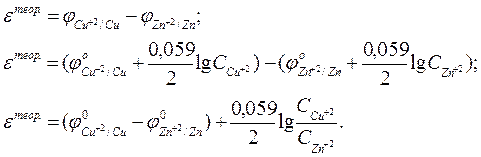
Так как 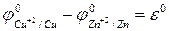 , то уравнение принимает вид
, то уравнение принимает вид 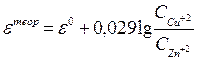 (в числителе дается окисленная, а в знаменателе - восстановленная форма), где e 0 – стандартная величина ЭДС гальванического элемента (eо=jко-jао). Для расчета e 0 используют данные табл. 2.
(в числителе дается окисленная, а в знаменателе - восстановленная форма), где e 0 – стандартная величина ЭДС гальванического элемента (eо=jко-jао). Для расчета e 0 используют данные табл. 2.
Относительную ошибку измерений (П, %) вычисляют по формуле
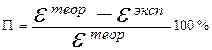 . (14)
. (14)
При оформлении работы студент должен написать уравнения электрохимических реакций, приводящих к возникновению электрического тока в системе, и указать какой из металлов выполняет роль окислителя, а какой – восстановителя.
|
|
Вопросы для самоконтроля и повторения
1. Дать определение электрохимическим процессам.
2. Дать определение электрохимическому или гальваническому элементу.
3. Какие энергетические превращения происходят в гальваническом элементе?
4. Дать определение электродного потенциала. Уравнение Нернста.
5. Какие из окислительно-восстановительных процессов происходят на катоде и аноде?
Лабораторная работа № 14
Электролиз растворов
Цель работы
1. Ознакомиться с явлением электролиза и составить схему установки для его проведения.
2. Написать схему процесса электролиза исследуемого раствора электролита.
3. Рассчитать количество веществ, образующихся в результате электролиза на электродах согласно законам Фарадея.
Теоретическая часть
Электролиз и работу гальванического элемента можно рассматривать как один и тот же процесс, направление которого изменяется под действием внешнего потенциала. Таким образом, электролиз – это окислительно-восстановительный процесс, протекающий в электролизере под действием электрического тока, подводимого от внешнего источника. При электролизе происходит превращение электрической энергии в химическую. Схема установки для проведения электролиза приведена на рис. 1.
|
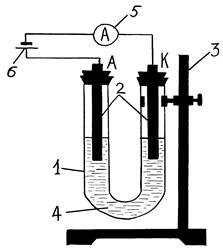
Электролиз широко используется в различных областях народного хозяйства: в гальваностегии, для нанесения металлических покрытий на металлы и пластмассы (гальванические покрытия); для рафинирования металлов, а также для получения большого спектра ценных продуктов: металлов, водорода, кислорода, хлора, щелочей и др. В частности, в мебельной промышленности – для хромирования и никелирования фурнитуры, в лесном и автомобильном хозяйствах, в лесоинженерном деле с помощью электролиза получают противокоррозионные гальванические покрытия, защищающие оборудование, механизмы и транспорт от коррозионных разрушений.
|
|
Пример электролиза расплава гидроксида калия
В расплаве происходит обратимый процесс диссоциации
 ⇄
⇄ 
Катионы (К+) перемещаются к катоду, а анионы (ОН–) к аноду
Катод 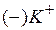 Анод
Анод 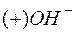
На катоде происходит На аноде происходит окисление
реакция восстановления гидроксильной группы (ОН-)


атомарный кислород объединяется в молекулярный
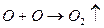
суммарный процесс электролиза выражается следующим уравнением:
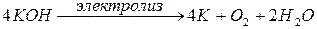 .
.
Пример электролиза раствора гидроксида калия
В растворе молекул КОН происходит диссоциация КОН
 ⇄
⇄ 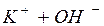
и молекул воды 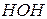 ⇄
⇄ 
Катионы К+ и Н+ подходят к катоду Анионы ОН– подходят к аноду
Катод 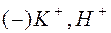 Анод
Анод 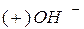
На катоде происходит
восстановление ионов Н+ На аноде окисляются ионы ОН-

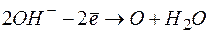
и молекул воды и молекулы воды
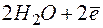 ⇄
⇄ 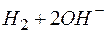
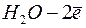 ® О + 2 Н +
® О + 2 Н + 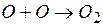
 Ионы К+ не восстанавливаются на катоде, так как
Ионы К+ не восстанавливаются на катоде, так как 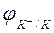 имеет более отрицательное значение, чем
имеет более отрицательное значение, чем 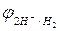 (см. табл. 2 стр. 114)
(см. табл. 2 стр. 114)


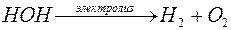 .
.
Гидроксид калия выполняет в данном случае функцию электропроводящей среды.
Количественные соотношения при электролизе были установлены Фарадеем в 1833 г. в виде следующих законов.
I закон Фарадея
|
|
|

Адаптации растений и животных к жизни в горах: Большое значение для жизни организмов в горах имеют степень расчленения, крутизна и экспозиционные различия склонов...

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...

Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов (88‰)...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!