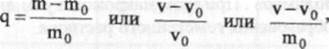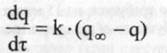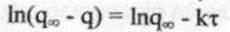Цель работы: получить фенолформальлегидные олигомеры новолачного и резольного типов, провести их отвердение и определить растворимость олигомеров до и после отвердения.
Реактивы: фенол, формалин, 1 Н раствор соляной кислоты, аммиак (30 %-й раствор) или раствор NaOH. уротропин (отвердитель), спирт, ацетон, гептан.
Приборы и посуда: колба круглодонная вместимостью 50 см3, обратный холодильник, термометр, фарфоровая чашка, шпатель, предметное стекло, пипетка, ступка, песчаная баня, металлическая пластинка.
Порядок работы:
1) получение фенолформальдегидного олигомера;
2)проведение его отвердения уротропином;
3)определение времени отвердения олигомера;
4)определение растворимости олигомера до и после отвердения.
1.Получение фенолформальдегидных олигомеров новолачного типа.
Методика работы. В круглодонную колбу емкостью 50 см3, снабженную обратным холодильником и термометром, помешают 2 г фенола и добавляют 1,8 см3 формалина (36 % раствор). После перемешивания добавляют 1 см3 1 Н раствора соляной кислоты. Затем смесь в течение 10-15 минут нагревают с обратным холодильником до 80°С. Через 10-20 мин после начала кипения смесь начинает мутнеть и затем расслаивается. С момента помутнения ее дополнительно нагревают при слабом кипении еще 30 минут. После этого смесь оставляют на 30 мин, затем выливают в фарфоровую чашку, промывают водой до нейтральной реакции, подсушивают и определяют растворимость полученного олигомера в спирте, ацетоне, гептане.
Далее проводят отвердение олигомера уротропином и определяют время его отвердения. Для этого навеску олигомера смешивают в ступке с уротропином (10:I). На металлическую пластину, нагретую по 150 °С, насыпают 1,0 г смеси и с помощью плоской металлической лопатки распределяют ее как можно более равномерно на площадке 4,5 х 4,5 см. Период от момента помещения олигомера на плитку до момента, когда он перестает тянуться в виде нитей и приклеиваться к лопатке, считают временем отвердения, затем проверяют растворимость отвержденного олигомера в спирте, ацетоне, углеводороде.
Задание. Написать схему реакций получения и отвердения новолачного фенолформальдегидного олигомера, оценить растворимость олигомера до и после отвердения.
Получение фенолформальдегидных олигомеров резольного типа
Методика работы. В круглодонную колбу помешают 2 г фенола, наливают 3 см3 формалина и после тщательного перемешивания массы добавляют пипеткой 0,1 см3 30 % раствора аммиака или NaOH. После этого колбу на песчаной бане нагревают до кипения, которое поддерживают в течение 40 мин, т.е. на протяжении всего времени поликонденсации (за начало конденсации принимают момент начала кипения). В процессе поликонденсации реакционная смесь мутнеет и разделяется на два слоя. Сразу же по окончании конденсации содержимое колбы переливают в фарфоровую чашку, промывают водой до нейтральной реакции, высушивают.
Полученный резол можно использовать для лакировки металлических изделий, для склеивания дерева с деревом, дерева с металлом. Для этого готовят раствор резола в спирте, покрывают лакируемый предмет лаком и нагревают до 160 °С для отвердения. Лак (резит) надежно пристает к металлу, он стоек по отношению к кислотам и щелочам, тверд, прочен на изгиб и к удару. Для склеивания деревянных дощечек одну из них смазывают полученной смолой, а на другую наносят концентрированную соляную кислоту. Зажимами плотно прижимают дощечки друг к другу, нагревают несколько минут и дают остыть. Соляная кислота служит отвердителем и превращает смолу в резит.
Задание: написать схему реакций, протекающих на первой и второй стадиях процесса.
ТЕМА 2. РАСТВОРЫ ПОЛИМЕРОВ
Теоретическая часть
Изучение поведения макромолекул в растворе имеет особое значение в связи с тем, что высокомолекулярные соединения не существуют в газообразном состоянии и всю основную информацию о свойствах индивидуальных макромолекул, их конформациях и размерах, молекулярных массах и распределении по молекулярным массам можно получить только при изучении растворов. Кроме того, для использования полимерных материалов в растворенном состоянии, а также для их переработки из растворов необходимо знание свойств полимерных растворов.
Размеры макромолекул соизмеримы с размерами коллоидных частиц. Поэтому растворы полимеров обнаруживают ряд свойств, характерных для коллоидных золей (эффект Тиндаля, замедленная диффузия, тиксотропия и др.). Однако в отличие от коллоидных золей растворы полимеров являются молекулярно-дисперсными системами и удовлетворяют основным критериям истинных растворов: 1) самопроизвольность образования, термодинамическая устойчивость, равновесие и обратимость; 2) постоянство концентрации во времени; 3) однофазность, гомогенность. Равновесие в системах полимер-растворитель из-за большого размера молекул полимера устанавливается значительно медленнее, чем в растворах низкомолекулярных веществ (иногда в течение недель и месяцев). Скорость установления равновесия определяется скоростью взаимной диффузии и сильно зависит от природы полимера и растворителя, молекулярной массы и концентрации полимера, а также от его исходного физического состояния и исходной степени дисперсности полимерных частиц.
Первой стадией растворения любого полимера является его набухание. Набухание - это процесс поглощения полимером низкомолекулярной жидкости, сопровождающийся увеличением объема полимера и изменением конформации его макромолекул. Большие молекулы полимера характеризуются низкими значениями коэффициентов диффузии. Поэтому смешение осуществляется медленно, и его промежуточные стадии легко фиксируются. При этом, благодаря способности макромолекул изменять свою форму растворитель на промежуточных стадиях растворения не только заполняет пустоты между отдельными звеньями (процесс, аналогичный капиллярной конденсации в твердых пористых телах), но и увеличивает эффективные радиусы полимерных клубков и расстояния между их центрами масс, не нарушая при этом сплошности полимерного тела. Последнее приводит к значительному увеличению объема полимерной фазы по сравнению с исходным. Набухший полимер фактически представляет собой раствор низкомолекулярной жидкости в полимере.
Если процесс растворения самопроизвольно прекращается на стадии набухания, то говорят об ограниченном набухании. Так, полимеры пространственно-сетчатого строения не могут полностью раствориться без разрыва химических связей. Они способны лишь ограниченно набухать, образуя гели. Состояние набухания характеризуют степенью набухания q, которую определяют как количество поглощенной полимером жидкости, отнесенное к единице массы или объема:
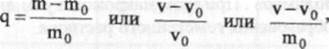
где m0, v0 - масса и объем исходного полимера;
m, v - масса и объем набухшего полимера.
На рис. 1.1. приведена типичная зависимость степени набухания от времени

Рис. 1. Зависимость степени набухания полимера от времени t.
1 - неограниченное; 2 - ограниченное набухание.
Максимальная или равновесная степень набухания определяется природой полимера и растворителя (сродством между ними) и густотой пространственной сетки полимера (при ее наличии).
Скорость набухания лимитируется скоростью взаимной диффузии компонентов системы и для полимеров, находящихся в исходном высокоэластическом состоянии, обычно удовлетворительно описывается кинетическим уравнением первого порядка:
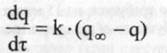
где k - постоянная набухания;
q∞ - максимальная степень набухания;
q - степень набухания в момент времени t.
После интегрирования этого уравнения получим:
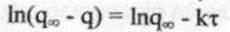
По тангенсу угла наклона прямолинейной зависимости ln(q∞ - q) от времени можно определить постоянную набухания k.
В случае линейных полимеров при изменении условий (температуры, концентрации и др.) ограниченное набухание может перейти в неограниченное, т.е. произойти растворение полимера. При этом макромолекулы диффундируют в растворитель вплоть до образования гомогенного раствора.
Методические указания
При подготовке к занятию повторите по курсу «Высокомолекулярные соединения» раздел, посвященный растворам полимеров.
Подготовьте ответы на приведенный ниже перечень вопросов.
Вопросы для самостоятельной подготовки
1. Особенности растворения полимеров. Набухание.
2. Электрические свойства полимеров. Полимерные диэлектрики, полупроводники.
3. Полиэлектролиты, ионообменные полимеры (иониты).
Занесите в тетрадь следующие работы, оставляя место для выводов и проведения расчетов