

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

История развития пистолетов-пулеметов: Предпосылкой для возникновения пистолетов-пулеметов послужила давняя тенденция тяготения винтовок...

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

История развития пистолетов-пулеметов: Предпосылкой для возникновения пистолетов-пулеметов послужила давняя тенденция тяготения винтовок...
Топ:
Особенности труда и отдыха в условиях низких температур: К работам при низких температурах на открытом воздухе и в не отапливаемых помещениях допускаются лица не моложе 18 лет, прошедшие...
Характеристика АТП и сварочно-жестяницкого участка: Транспорт в настоящее время является одной из важнейших отраслей народного...
Интересное:
Как мы говорим и как мы слушаем: общение можно сравнить с огромным зонтиком, под которым скрыто все...
Берегоукрепление оползневых склонов: На прибрежных склонах основной причиной развития оползневых процессов является подмыв водами рек естественных склонов...
Уполаживание и террасирование склонов: Если глубина оврага более 5 м необходимо устройство берм. Варианты использования оврагов для градостроительных целей...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Пути внутриклеточного превращения амино кислот.
1направление по аминогруппе дезаминирование аланин+Н2О(-2Н-NН3)=ПВК
переаминирование ПВК+ацетоуксусная кис-та=аспаргиновая к-та+СН3-С=О-СООН
аминировние ПВК+Н2+NН3=аланин СН3-С=NН2-СООН
2 направление по радикалуфенил-аланин+О2+Н2О=тирозин
3 По гидроксильной группе
СООН-СНNН2-СООН-СО2=СН2NН2-СООН
29.Обезвреживание аммиака.синтез мочевины Аммиак является ядовитым веществом для живых клеток. Основной путь обезвреживания аммиака в организме связан с синтезом мочевины. доказано, что синтез мочевины в основном происходит митохондриях клеток печени в результате кругового процесса, требующего небольшого количества орнитина, получившего название орнитинового цикла. Промежуточным продуктом этого цикла является карбамилфосфат, на синтез которого требуется две молекулы АТФ. С карбамилфосфата на орнитин, в результате образуется цитруллин. Последний вступает в реакцию с аспарагиновой кислотой и образует аргинин. Аргинин гидролизуется ферментом аргиназой с образованием мочевины и орнитина. Немаловажное значение в нейтрализации аммиака отводится образованию амидов - прежде всего, глютамина из глютаминовой кислоты, а также аспарагина из аспарагиновой кислоты. Синтез амидов сопряжен с распадом АТФ. По мере образования, аммиак во всех тканях связывается с глутаминовой кислотой с образованием глутамина. Это временное обезвреживание аммиака. С током крови глутамин поступает в печень, где распадается опять на глутаминовую кислоту и аммиак. Глутаминовая кислота с кровью снова поступает в органы для обезвреживания новых порций аммиака. Освободившийся аммиак, а также углекислый газ используются в печени для синтеза мочевины: Синтез мочевины – это циклический многостадийный процесс, идущий с большими затратами энергии. В синтезе мочевины важнейшую роль играет аминокислота орнитин. Синтез мочевины часто называют о рнитиновым циклом. В процессе синтезе к орнитину присоединяются две молекулы аммиака и молекула углекислого газа, и орнитин превращается в другую аминокислоту – аргинин. От аргинина отщепляется мочевина и вновь образуется орнитин. В сутки её образуется 20 – 35 г. выделение мочевины с мочой характеризует интенсивность распада белков в организме.
|
|
30. Химич ит.д Липиды -это класс органических соединений не растворимых в воде. Они растворяются в органических растворителях,таких как эфиры, хлороформ и бензол. Моллекула жира состоит из атомов углерода,водорода и кислорода. Жиры в организме выполняют разнообразные биологические функции: Энергетическая -при распаде 1 г жира освобождается 9,3 ккал энергии.В форме гликогена организм может запасать энергию для обеспечения основного обмена не более чем на сутки,тогда как в форме триглециридов-на несколько месяцев. Структурная -вместе с белками являются структурным компонентом всех клеточных мембран. Регуляторная -эту функцию выполняют гормоны стероидной породы, и тканевые гормоны. Терморегуляторная- предохраняют организм от переохлажления. Защитная -защищают внутренние органы о механических повреждений, а также нервные окончания и кровеносные сосуды от сдавливания и ушыбов. В качестве растворителя - в жирах растворяются многие органические соединения,благодаря чему они легко проникают через стенки сосудов,мембраны клеток, транспортируются в биолог.жидкостях. 1. Простые липиды представлены двухкомпонентными веществами - сложными эфирами высших жирных кислот с глицерином, высшими или полициклическими спиртами. Сюда относятся: жиры (триглицериды)-сложные эфиры высших жирных кислот и тpexaтомного спирта-глицерина; воски - сложные эфиры высших жирных кислот и высших спиртов; стериды - сложные эфиры высших жирных кислот и полициклических спиртов -стеролов. 2. Сложные липиды имеют многокомпонентные молекулы, компоненты которых соединены химическими связями различного типа. К ним принадлежат: фосфолипиды состоящие из остатков высших жирных кислот, глицерина или других многоатомных спиртов, фосфорной кислоты и азотистых оснований той или иной природы; гликолипиды, включающие в свой состав наряду с многоатомным спиртом и высшей жирной кислотой также углеводы.
|
|
Химические свойства аминокислот
В растворах они хорошо диссоциируют с образованием внутренней соли.
СН2-СООН = СН2СОО -
NН2 NН3+
Внутренняя соль
Основные свойства аминокислот проявляются в реакциях с кислотами.

Кислотные способности аминокислот можно видеть в реакциях с основаниями:
NН2–СН–СООН+NаОН→NН2–СН–СООNа+Н2О→NН2–СН–СОО–+Nа+ + ОН–
СН3 СН3 СН3
Являясь амфотерными электролитоми, они хорошо взаимодействуют между собой с образованием пептидов и белков.
СН3-СН-СООН + СН2-СООН СН3-СН- СО-NН -СН2-СООН+Н2О
NН2 NН2 NН2
аланин глицин аланилглицин
Связь (-СО - NН -) пептидной, а продукты
6. Общая хар-ка нуклеиновых…. Дезоксирибонуклеи́новая кислота́ (ДНК) — макромолекула (одна из трех основных, две другие — РНК и белки), обеспечивающая хранение, передачу из поколения в поколение и реализацию генетической программы развития и функционирования живых организмов. Основная роль ДНК вклетках — долговременное хранение информации о структуре РНК и белков. Рибонуклеи́новая кисло́та (РНК) — одна из трёх основных макромолекул (две другие — ДНК и белки), которые содержатся в клетках всех живых организмов.А-Т,Г-Ц—ДНК,Рнк---А-У,Т-Ц.Роль Днк-хранения и передача наследственной информации.Роль Рнк-синтез белков по программе зашифрованной в участках ДНК.
7.общая хар-ка липидов. Липиды-это сложные эфиры высших жирных кислот,разнообразных спиртов не растворимых в воде, а растворимых в неполярных растворитнелях.Нейтральные жиры-глицерин и три остатка жирных кислот,фосфолипиды-глицерин 2 остатка жирных кислот и остатка фосфорной кислоты,гликолипиды,стероидыжироподобные вещества в состав которых входит сложный цикл стерана. Молекулы простых липидов состоят из спирта, жирных кислот, сложные — из спирта, высокомолекулярных жирных кислот, возможны остатки фосфорной кислоты, углеводов, азотистых оснований и др. Строение липидов зависит в первую очередь от пути их биосинтеза. Для подробного ознакомления следует перейти по ссылкам, указанным в схеме классификации.Энергетическая,структурная,регуляторная,защитная,в качестве растворителя.
|
|
8. Триглециридов. По химическому строению триглицериды (или жиры) представляют собой сложные эфиры трехатомного спирта глицерина и высших жирных кислот. С15H33,COOH-трипальмитин. Физико-хим. С-ва жиров во многом определяются составом жирных к-т. Жиры, содержащие преимущественно ненасыщенные жирные жирные к-ты, при комнотной комнотной температуре твердые, а ненасыщенные жирные к-ты- жидкие.Твердые жиры-животного происхождения,за исключением рыбьего жира. Жидкие-это раст.масла. Среди триглицеридов различают простые и смешанные. Первые являются сложными эфирами глицерина и одной из высших кислот.Вторые построены из остатка глицерина и остатков разных высших жирных кислот
9. Фосфолипиды - сложные эфиры многоатомных спиртов с высшими жирными кислотами, содержащие остатки фосфорной кислоты и связанные с нею добавочные группировки (азотистые основания, аминокислоты, глицерин, инозит и др.). Биологич.роль-являются структурным компонентом всех клеточных мембран,поставщиком холина, необходимого для образования нейропередатчика-ацитилхолина. СТЕРОИДЫ - класс органических соединений; полициклические спирты, кетоны, кислоты и др. Широко распространены в живой природе. К стероидам относятся стерины, желчные кислоты, витамины группы D, половые гормоны, гормоны надпочечников (кортикостероиды). Биологич.роль -деление клеток, восстановление органов и тканей, обмен веществ углеводный, жировой, защитные реакции организма – иммунная функция, рост мышечных тканей, химические процессы в мембранах нервных клеток.Представители:желчные к-ты,муж. И жен. Половые гормоны,гормоны надпочечников. Стерины — группа биохимически важных веществ из группы стероидов. В основе структуры стеринов лежит насыщенный тетрациклический углеводород стеран. Основная биологическая роль стеринов состоит в том, что они являются предшественниками многих биологически активных соединений – стероидных гормонов, витаминов, желчных кислот, сапонинов, экдизонов. Важная роль стеринов в формировании клеточных структур, в частности, клеточных мембран.Представители:халестерин.
|
|
10. Предмет биохимии ….Биохи́мия — наука о химическом составе живых клеток и организмов и о химических процессах, лежащих в основе ихжизнедеятельности. Термин «биохимия» эпизодически употреблялся с середины XIX века, в классическом смысле он был предложен и введён в научную среду в 1903 году немецкимхимиком Карлом Нойбергом. Как самостоятельная наука биохимия сформировалась примерно 100 лет назад, однако биохимические процессы люди использовали ещё в глубокой древности, не подозревая, разумеется, об их истинной сущности. Биохимия стала первой биологической дисциплиной с развитым математическим аппаратом благодаря работам Холдейна, Михаэлиса, Ментен и других биохимиков, создавших ферментативную кинетику, основным законом которой является уравнение Михаэлиса-Ментен.Открытие ферментов позволило начать грандиозную работу по полному описанию всех процессов метаболизма, не завершённую до сих пор. Одними из первых значительных находок в этой области стали открытия витаминов, гликолиза и цикла трикарбоновых кислот.
11.метаболиз, катоболизм… Совокупность химических превращений веществ, которые происходят в организме начиная с момента поступления переваренных пищевых веществ в кровь и до момента выделения конечных продуктов обмена из организма – называют промежуточным метаболизмом (обменом веществ). Промежуточный метаболизм может быть разделён на два процесса: катаболизм (диссимиляция) и анаболизм (ассимиляция). Катаболизм – это ферментативное расщепление сравнительно крупных органических молекул осуществляемое у высших организмов, как правило, окислительным путём. Катаболизм сопровождается освобождением энергии, заключенной в сложных структурах крупных органических молекул и запасанием её в форме фосфатных связей АТФ. Анаболизм – это ферментативный синтез из более простых соединений крупномолекулярных клеточных компонентов, таких как полисахариды, нуклеиновые кислоты, белки, липиды, а также некоторых их предшественников. Анаболические процессы протекают с потреблением энергии. Катаболизм и анаболизм происходят в клетках одновременно и неразрывно связаны друг с другом. По существу их следует рассматривать не как два отдельных процесса, а как две стороны одного общего процесса – метаболизма, в котором превращение веществ теснейшим образом переплетены с превращением энергии.
|
|
Белки составляют до 45% массы тела. уникальность аминокислот заключается в том, что они могут соединяться с другими аминокислотами, образуя сложные структуры. Это ферменты, которые катализуют реакции; гормоны, такие, как инсулин и глюкагон; гемоглобин и миоглобин, которые являются переносчиками кислорода; все тканевые структуры, включая миозин и актин образующие белок мышц. Все они очень существенны для двигательной активности.
Исследования показывают, что белки вносят свой вклад как источники энергии во время голодания и интенсивной нагрузки, возможно, 15% всех килокалорий во время напряженных упражнений. Адекватность энергии и углеводов в диете имеют большое влияние на этот процесс.
Если диета неадекватна по калорийности или углеводам для поддержания энергии, расходуемой во время нагрузки, белки вносят свой вклад как источник энергии, отсюда углеводы можно рассматривать как «вещества, экономящие белок». Вклад белков как источника энергии уменьшается примерно до 50%, если энергия адекватна.
12. Особенности обменя вещ-в. Цереброзиды содержат спирт сфингозин,жирные кислоты и остатки различных сахаров.Содержатся в клетках белого вещества мозга,присутствуют в мембранах других клеток.Ганглиозиды-это наиболее сложные по строению сфинголипиды.В их состав входит несколько остатков сахаров.Они содержаться в сером веществе мозга.. Макроэргические соединения — группа природных веществ, молекулы которых содержат богатые энергией, или макроэргические, связи; присутствуют во всех живых клетках и участвуют в накоплении и превращении энергии. Разрыв макроэргических связей в молекулах М.с. сопровождается выделением энергии, используемой для биосинтеза и транспорта веществ, мышечного сокращения, пищеварения и других процессов жизнедеятельности организма. Все известные М.с. содержат фосфорильную (—РО3Н2) или ацильную группы и могут быть описаны формулой Х—Y, где Х — атом азота, кислорода, серы или углерода, а Y — атом фосфора или углерода. Реакционная способность М.с. связана с повышенным сродством к электрону атома Y, что обусловливает высокую свободную энергию гидролиза М.с., составляющую 6—14 ккал/моль. Аденозинтрифосфа́т — нуклеотид, играет исключительно важную роль в обмене энергии и веществ в организмах; в первую очередь соединение известно как универсальный источник энергии для всех биохимических процессов, протекающих в живых системах. Главная роль АТФ в организме связана с обеспечением энергией многочисленных биохимических реакций. Являясь носителем двух высокоэнергетических связей, АТФ служит непосредственным источником энергии для множества энергозатратных биохимических и физиологических процессов. Все это реакции синтеза сложных веществ в организме: осуществление активного переноса молекул через биологические мембраны, в том числе и для создания трансмембранного электрического потенциала; осуществления мышечного сокращения.
13.. Окисление биологическое - совокупность реакций окисления, протекающих во всех живых клетках. Основная функция О. б. — обеспечение организма энергией в доступной для использования форме. Реакции О. б. в клетках катализируют ферменты, объединяемые в класс оксидоредуктаз.
Процессы биологического окисления протекают в присутствии особых ферментов, принимающих участие в образовании промежуточных соединений. Чтобы фермент мог принять участие в реакции окисления - восстановления, он должен обладать определенным окислительно-восстановительным потенциалом, характеризующим его способность присоединять или отдавать электроны. Если окислительно-восстановительный потенциал фермента больше окислительно-восстановительного потенциала вещества А, с которым он реагирует, то фермент будет действовать как окислитель, присоединяя электроны, отдаваемые веществом А. В том случае, когда фермент обладает более низким окислительно-восстановительным потенциалом, чем вещество А, он будет проявлять свойства восстановителя, отдавая электроны веществу А
14. Ферме́нты — обычно белковые молекулы или молекулы РНК (рибозимы) или их комплексы, ускоряющие (катализирующие) химические реакции в живых системах. Реагенты в реакции, катализируемой ферментами, называются субстратами, а получающиеся вещества — продуктами. Ферменты специфичны к субстратам. Ферментативная активность может регулироваться активаторами и ингибиторами (активаторы — повышают, ингибиторы — понижают). Белковые ферменты синтезируются на рибосомах, а РНК — в ядре. Структура и механизм действия ферментов Как и все белки, ферменты синтезируются в виде линейной цепочки аминокислот, которая сворачивается определённым образом. Каждая последовательность аминокислот сворачивается особым образом, и получающаяся молекула (белковая глобула) обладает уникальными свойствами. Несколько белковых цепей могут объединяться в белковый комплекс. Третичная структура белков разрушается при нагревании или воздействии некоторых химических веществ.Чтобы катализировать реакцию, фермент должен связаться с одним или несколькими субстратами. Белковая цепь фермента сворачивается таким образом, что на поверхности глобулы образуется щель, или впадина, где связываются субстраты. Эта область называется сайтом связывания субстрата. Обычно он совпадает с активным центром фермента или находится вблизи него. Некоторые ферменты содержат также сайты связывания кофакторов или ионов металлов.Фермент, соединяясь с субстратом:очищает субстрат от водяной «шубы» располагает реагирующие молекулы субстратов в пространстве нужным для протекания реакции образом
подготавливает к реакции (например, поляризует) молекулы субстратов. Обычно присоединение фермента к субстрату происходит за счет ионных или водородных связей, редко – за счет ковалентных. В конце реакции её продукт (или продукты) отделяются от фермента.В результате фермент снижает энергию активации реакции. Это происходит потому, что в присутствии фермента реакция идет по другому пути (фактически происходит другая реакция), например:В отсутствии фермента:А+В = АВ В присутствии фермента:
А+Ф = АФ АФ+В = АВФ АВФ = АВ+Ф где А, В - субстраты, АВ - продукт реакции, Ф - фермент. Свойства: они остаются неизмененными после реакции, т.е. освобождаясь, могут вновь реагировать с новыми молекулами субстрата. Ферменты способны оказывать действие в ничтожно малых концентрациях
15. Гормо́ны — сигнальные химические вещества, выделяемые эндокринными железами непосредственно в кровь и оказывающие сложное и многогранное воздействие на организм в целом либо на определённые органы и ткани-мишени. Гормоны служат гуморальными (переносимыми с кровью) регуляторами определённых процессов в определённых органах и системах. Механизмы действияКогда гормон, находящийся в крови, достигает клетки-мишени, он вступает во взаимодействие со специфическими рецепторами; рецепторы "считывают послание" организма, и в клетке начинают происходить определенные перемены. Каждому конкретному гормону соответствуют исключительно "свои" рецепторы, находящиеся в конкретных органах и тканях - только при взаимодействии гормона с ними образуется гормон-рецепторный комплекс.Механизмы действия гормонов могут быть разными. Одну из групп составляют гормоны, которые соединяются с рецепторами, находящимися внутри клеток - как правило, в цитоплазме. К ним относятся гормоны с липофильными свойствами - например, стероидные гормоны (половые, глюко- и минералокортикоиды), а также гормоны щитовидной железы. Будучи жирорастворимыми, эти гормоны легко проникают через клеточную мембрану и начинают взаимодействовать с рецепторами в цитоплазме или ядре. Они слабо растворимы в воде, при транспорте по крови связываются с белками-носителями.Считается, что в этой группе гормонов гормон-рецепторный комплекс выполняет роль своеобразного внутриклеточного реле - образовавшись в клетке, он начинает взаимодействовать с хроматином, который находится в клеточных ядрах и состоит из ДНК и белка, и тем самым ускоряет или замедляет работу тех или иных генов. Избирательно влияя на конкретный ген, гормон изменяет концентрацию соответствующей РНК и белка, и вместе с тем корректирует процессы метаболизма.Биологический результат действия каждого гормона весьма специфичен. Хотя в клетке-мишени гормоны изменяют обычно менее 1% белков и РНК, этого оказывается вполне достаточно для получения соответствующего физиологического эффекта.Большинство других гормонов характеризуются тремя особенностями:1.они растворяются в воде; 2.не связываются с белками носителей; 3.начинают гормональный процесс, как только соединяются с рецептором, который может находиться в ядре клетки, ее цитоплазме или располагаться на поверхности плазматической мембраны. Классификация гормонов по химической структуре: Производные аминокислот:
производные тирозина: тироксин, трийодтиронин, дофамин, адреналин, норадреналин; производные триптофана: мелатонин, серотонин;производные гистидина: гистамин. Белково-пептидные гормоны:полипептиды: глюкагон, кортикотропин, меланотропин, впзопрессин, окситоцин, пептидные гормоны желудка и кишечника;простые белки (протеины): инсулин, соматотропин, пролактин, паратгормон, кальцитонин;сложные белки (гликопротеиды): тиреотропин, фоллитропин, лютропин. Стероидные гормоны: кортикостероиды (альдостерон, кортизол, кортикостерон);половые гормоны: андрогены (тестостерон), эстрогены и прогестерон.
Производные жирных кислот:арахидоновая кислота и ее производные: простагландинм: простациклины, тромбоксаны, лейкотриены.
Функциональная классификация гормонов: Эффекторные гормоны — гормоны, которые оказывают влияние непосредственно на орган-мишень. Тропные гормоны — гормоны, основной функцией которых является регуляция синтеза и выделения эффекторных гормонов. Выделяются аденогипофизом. Рилизинг-гормоны — гормоны, регулирующие синтез и выделение гормонов аденогипофиза, преимущественно тропных. Выделяются нервными клетками гипоталамуса.
16. .Общая хар-ка углеводов. Углево́ды(сахара, сахариды) —органические вещества, содержащиекарбонильную группуи несколькогидроксильных групп. Название класса соединений происходит от слов «гидраты углерода», оно было впервые предложено К. Шмидтом в1844 году. Появление такого названия связано с тем, что первые из известных науке углеводов описывались брутто-формулой Cx(H2O)y, формально являясь соединениямиуглеродаиводы.Моносахари́ды(от греческогоmonos — единственный,sacchar —сахар) — простейшие углеводы, не гидролизующиеся с образованием более простых углеводов — обычно представляют собой бесцветные, легко растворимые вводе, плохо — в спирте и совсем нерастворимые в эфире, твёрдые прозрачныеорганические соединения[2], одна из основных групп углеводов, самая простая форма сахара.Дисахари́ды— сложныеорганические соединения, одна из основных групп углеводов, пригидролизекаждая молекула распадается на две молекулы моносахаридов. О́лигосахари́ды — углеводы, молекулы которых синтезированы из 2 — 10 остатков моносахаридов, соединённых гликозидными связями. Структурная и опорная функции. Углеводы участвуют в построении различных опорных структур. Так целлюлоза является основным структурным компонентом клеточных стенокрастений, хитин выполняет аналогичную функцию у грибов, а также обеспечивает жёсткость экзоскелета членистоногих[1].Защитная роль у растений. У некоторых растений есть защитные образования (шипы, колючки и др.), состоящие из клеточных стенок мёртвых клеток.Пластическая функция. Углеводы входят в состав сложных молекул (например, пентозы (рибоза и дезоксирибоза) участвуют в построении АТФ, ДНК и РНК)..Энергетическая функция. Углеводы служат источником энергии: при окислении 1 грамма углеводов выделяются 4,1 ккал энергии и 0,4 г воды.Запасающая функция. Углеводы выступают в качестве запасных питательных веществ: гликоген у животных, крахмал и инулин — у растений.Осмотическая функция. Углеводы участвуют в регуляции осмотического давления в организме. Так, в крови содержится 100—110 мг/% глюкозы, от концентрации глюкозызависит осмотическое давление крови.Рецепторная функция. Олигосахариды входят в состав воспринимающей части многих клеточных рецепторов или молекул-лигандов.
17. Моносахариды, строение, изомерия, свойства
Моносахариды можно рассматривать как производные многоатомных спиртов, содержащие карбонильную группу

| и | 
|
Если карбонильная группа находится в конце цепи, то моносах альдегидоспирт и называется альдозой; при любом другом положении этой карбонильной группы моносахарид является кетоспиртом и называется кетозой.
По количеству атомов углерода различают триозы, тетрозы, пентозы, гексозы, гептозы.
Простейшим представителем моносахаридов являются триозы: глицериновый альдегид (альдоза) и дигидроксиацетон (кетоза).
При окислении первичной спиртовой группы трехатомного спирта – глицерина образуется глицериновый альдегид (глицеральдегид), а окисление вторичной спиртовой группы приводит к образованию дигидроксиацетона.

глицерин альдегидоглицерин дигидроксиацетон эритроза (тетроза) рибоза (пентоза) глюкоза (гексоза) фруктоза (гексоза)
Для моносахаридов характерна оптическая изомерия. Все моносахариды содержат один или более асимметрических атомов углерода: у альдозы - 1; у альдотетрозы - 2; у альдокетозы - 3; у альдогексозы - 4. 
Кетозы с тем же числом атомов углерода в молекуле содержат на один асимметричный атом меньше. Общее число стереоизомеров для любого моносахарида выражается формулой: N = 2n, где N - число стереоизомеров; n - число асимметричных атомов углерода. Глюкоза имеет 16 стереоизомеров.
Тот изомер, у которого при проекции молекулы на плоскость группа - ОН у асимметричного атома углерода расположена с правой стороны, принято считать D-изомером, а его зеркальное отражение - L-изомером. Например,

D-изомер L-изомер
Химические свойства моносахаридов (на примере глюкозы)
· Глюкоза способна подвергаться спиртовому брожению с образованием СО2 и спирта: С6Н12О6 2 С2Н5ОН + 2СО2
· Глюкоза в организме человека может окисляться:
а) В присутствии кислорода: С6Н12О6 +6О2 +36Н3РО4 +36АДФ → 6СО2 + 42 Н2О + 38АТФ;
б) В гипоксических условиях - с образованием молочной кислоты
С6Н12 О6 = 2СН3СНОНСООН + 2АТФ.
· Фосфорилирование глюкозы:

глюкоза фосфорная к-та глюкозо-1-фосфат
· Моносахариды легко окисляются, т. к. содержат карбонильную группу:
а) реакция серебряного зеркала

глюкоза глюконовая к-та
б) реакция Троммера:

глюкоза глюконовая кислотата
в) реакция с реактивом Фелинга:
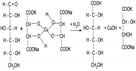
глюкоза + реактив Фелинга = глюконовая к-та + натрий-калиевая соль винной кислоты
5. Восстановление моносахаридов:

глюкоза (альдегидо-спирт) сорбит (шестиатомный спирт)
18. Дисахариды и полисахариды. Строение и свойства, биолог.родь. Представители. Дисахариды - типичные сахароподобные полисахариды. Это твердые вещества, или некристаллизующиеся сиропы, хорошо растворимые в воде. Как аморфные, так и кристаллические дисахариды обычно плавятся в некотором интервале температур и, как правило, с разложением. Дисахариды образуются в результате реакции конденсации между двумя моносахаридами, обычно гексозами. Связь между двумя моносахаридами называют гликозидной связью. Обычно она образуется между первым и четвертым углеродными атомами соседних моносахаридных единиц (1,4-гликозидная связь). Этот процесс может повторяться бессчетное число раз, в результате чего и возникают гигантские молекулы полисахаридов. После того как моносахаридные единицы соединятся друг с другом, их называют остатками. Таким образом мальтоза состоит из двух остатков глюкозы. Среди дисахаридов наиболее широко распространены мальтоза (глюкоза + глюкоза), лактоза (глюкоза + галактоза), сахароза (глюкоза + фруктоза).
ОТДЕЛЬНЫЕ ПРЕДСТАВИТЕЛИ ДИСАХАРИДОВ. Мальтоза (солодовый сахар) имеет формулу С12Н22О11. Название возникло в связи со способом получения мальтозы: ее получают из крахмала при воздействии солода (лат. maltum - солод). В результате гидролиза мальтоза расщепляется на две молекулы глюкозы: С12Н22О11 + Н2О = 2С6Н12О6)Лактоза (молочный сахар). Название этого дисахарида возникло в связи с его получением из молока (от лат. lactum - молоко). При гидролизе лактоза расщепляется на глюкозу и галактозу: С12Н22О11 + Н2О = С6Н12О6 + С6Н12О6) Сахароза (тростниковый или свекловичный сахара). Название возникло в связи с ее получением либо из сахарной свеклы, либо из сахарного тростника. Тростниковый сахар был известен за много столетий до нашей эры. Лишь в середине XVIII в. этот дисахарид был обнаружен в сахарной свекле и только в начале XIX в. он был получен в производственных условиях. Сахароза очень распространена в растительном мире. Листья и семена всегда содержат небольшое количество сахарозы. Она содержится также в плодах (абрикосах, персиках, грушах, ананасах). Ее много в кленовом и пальмовом соках, кукурузе. Это наиболее известный и широко применяемый сахар. При гидролизе из него образуются глюкоза и фруктоза: С12Н22О11 + Н2О = С6Н12О6 + С6Н12О6.
19. .Расщепление углеводного обмена. Норма глюкозы в крови. Понятие о гипо-гипергликимии, гликозурин. Регуляция углеводного обмена осуществляется при участии очень сложных механизмов, которые могут оказывать влияние на индуцирование или подавление синтеза различных ферментов У. о. либо способствовать активации или торможению их действия. Инсулин, катехоламины, глюкагон, соматотропный и стероидные гормоны оказывают различное, но очень выраженное влияние на разные процессы углеводного обмена. Так, например, инсулин способствует накоплению в печени и мышцах гликогена, активируя фермент гликогенсинтетазу, и подавляет гликогенолиз и глюконеогенез. Антагонист инсулина — глюкагон стимулирует гликогенолиз. Адреналин, стимулируя действие аденилатциклазы, оказывает влияние на весь каскад реакций фосфоролиза. Гонадотропные гормоны активируют гликогенолиз в плаценте. Глюкокортикоидные гормоны стимулируют процесс глюконеогенеза. Соматотропный гормон оказывает влияние на активность ферментов пентозофосфатного пути и снижает утилизацию глюкозы периферическими тканями. В регуляции глюконеогенеза принимают участие ацетил-КоА и восстановленный никотинамидадениндинуклеотид. Повышение содержания жирных кислот в плазме крови тормозит активность ключевых ферментов гликолиза. В регуляции ферментативных реакций У. о. важную цель играют ионы Са2+, непосредственно или при участии гормонов, часто в связи с особым Са2+-связывающим белком — калмодулином. В регуляции активности многих ферментов большое значение имеют процессы их фосфорилирования — дефосфорилирования. В организме существует прямая связь между У. о. и обменом белков, липидов (см. Жировой обмен) и минеральных веществ. Норма уровня глюкозы в крови. Содержание сахара в крови у взрослых и у детей одинаково. Оно регулируется эндокринной и нервной системами. Уровень сахара в крови считается нормальным, если он находится в диапазоне 3,3-5,5 ммоль/л. Однако, физиологические процессы, происходящие в организме при пищеварении, оказывают влияние на уровень глюкозы в крови, заставляя его колебаться более, чем в пределах нормы. После поступления пищи в желудочно-кишечный тракт происходит всасывание в кровь простых углеводов, сложные углеводы расщепляются ферментами до простых и тоже всасываются в кровь. В результате повышается уровень сахара в крови, его значение превышает 5,5 ммоль/л (обычно не поднимается выше 8,0 ммоль/л).В одной чайной ложке 5 грамм сахара – быстро усвояемого углевода, который при употреблении в пищу и всасывании в желудочно-кишечном тракте, попадает в кровь. Очевидно, что уровень «сахара» в крови в этом случае повысится.Избыточное количество глюкозы запасается клетками печени. В перерывах между приемами пищи, когда содержание глюкозы в крови понижается, она извлекается из «хранилища» для поддержания необходимого минимального уровня в крови.Исходя из того, что молярная масса глюкозы – 180 г/моль, а у взрослого человека количество крови находится в пределах 5-ти литров, можно определить, что у взрослого человека в крови 3-5 граммглюкозы. Гипогликемия- явл, вызываемое пониженным содерж. Глюкозы в крови(до 50-60 мг %). Гипергликемия- явл. Повышения концентрации глюкозы в крови (до 150-250 мг%). Глюкозурия- явл. Сопровождающее гипергликемию и выражающееся в присутствии сахара в моче.
20. .Биосинтез и ферментативный распад гликогена.
Гликоген - основная форма депонирования глюкозы в клетках животных. У растений эту же функцию выполняет крахмал. В структурном отношении гликоген, как и крахмал, представляет собой разветвленный полимер из глюкозы.Однако гликоген более разветвлен и компактен. Ветвление обеспечивает быстрое освобождение при распаде гликогена большого количества концевых мономеров. Синтез и распад гликогена не являются обращением друг в друга, эти процессы происходят разными путями. Биосинтез гликогена. Гликоген синтезируется в период пищеварения (в течение 1-2 ч после приема углеводной пищи). Гликогенез особенно интенсивно протекает в печени и скелетных мышцах. В начальных реакциях образуется UDF-глюкоза (реакция 3), которая является активированной формой глюкозы, непосредственно включающейся в реакцию полимеризации (реакция 4). Эта последняя реакция катализируется гликогенсинтазой, которая присоединяет глюкозу к олигосахариду или к уже имеющейся в клетке молекуле гликогена, наращивая цепь новыми мономерами. Для подготовки и включения в растущую полисахаридную цепь требуется энергия 1 моль АТР и 1 моль UTP. Ветвление полисахаридной цепи происходит при участии фермента амило - -1,4--1,6-гликозил-трансферазы путем разрыва одной -1,4-связи и переноса олигосахаридного остатка от конца растущей цепи к ее середине с образованием в этом месте -1,6-гликозидной связи. Молекула гликогена содержит до 1 млн остатков глюкозы, следовательно, на синтез расходуется значительное количество энергии. Необходимость превращения глюкозы в гликоген связана с тем, что накопление значительного количества глюкозы в клетке привело бы к повышению осмотического давления, так как глюкоза хорошо растворимое вещество. Напротив, гликоген содержится в клетке в виде гранул, и мало растворим. Распад гликогена - гликогенолиз - происходит в период между приемами пищи.
Распад гликогена. Освобождение глюкозы в виде глюкозо-1-фосфата (реакция 5) происходит в результате фосфоролиза, катализируемого фосфорилазой. Фермент отщепляет концевые остатки один за другим, укорачивая цепи гликогена. Однако этот фермент расщепляет только -1,4 гликозидные связи. Связи в точке ветвления гидролизуются ферментом амило--1,6-гликозидазой, который отщепляет мономер глюкозы в свободном виде.
21.регуляция углеводного обмена…..
.В регул угл обм.принимают участи ЦНС:пониж сахара=возбужд центры промеж мозга(мысль о предстоящ нагр, соревнования – усл раздражители)
Также принимает участие эндокр сис-ма.гормоны коры надпочечн. Адреналин и норадреналин повыш содерж сахара в крови. Горм поджел железы-усил рапад гликогена в печени и в мышцах.
Инсулин – усил синтез гликогена. Мышцы-место усил потребления угл., в нач работы или при интенсив упр. Созд анаэробные усл, когда О2 не поступил ещё в мышцы происх анаэробн окис(гликолиз и накопление мол.)
В состоянии покоя уровень сахара 70-100мг% (спорт-80-120)молоч к-та 10-20мг%
Повыш конц глк до 150-250-гипергликем(от пищевого проис или под физ нагр и эмоц)во вр гапергл –наблюд гюкозурия. Понижение глю до 60-50 мг гипогликемия.
|
|
|

История развития хранилищ для нефти: Первые склады нефти появились в XVII веке. Они представляли собой землянные ямы-амбара глубиной 4…5 м...

Папиллярные узоры пальцев рук - маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни...

Биохимия спиртового брожения: Основу технологии получения пива составляет спиртовое брожение, - при котором сахар превращается...

Археология об основании Рима: Новые раскопки проясняют и такой острый дискуссионный вопрос, как дата самого возникновения Рима...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!