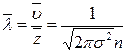 ,
,
где 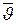 - средняя арифметическая скорость,
- средняя арифметическая скорость,  - среднее число столкновений каждой молекулы с остальными в единицу времени, σ – эффективный диаметр молекулы и n – число молекул в единице объема.
- среднее число столкновений каждой молекулы с остальными в единицу времени, σ – эффективный диаметр молекулы и n – число молекул в единице объема.
Общее число столкновений всех молекул в единице объема за единицу времени равно
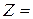
 .
.
Масса М, перенесенная за время ∆t при диффузии, определяется уравнением
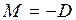
 ,
,
где  - градиент плотности в направлении, перпендикулярном к площадке ∆S и D – коэффициент диффузии, равный
- градиент плотности в направлении, перпендикулярном к площадке ∆S и D – коэффициент диффузии, равный
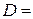
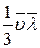 .
.
Здесь 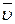 - средняя скорость,
- средняя скорость, 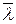 - средняя длина свободного пробега молекул.
- средняя длина свободного пробега молекул.
Количество движения, перенесенное газом за время ∆t, определяет силу внутреннего трения F в газе:
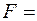
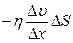 ,
,
где 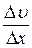 - градиент скорости течения газа в направлении, перпендикулярном к площадке ∆S,а η – коэффициент внутреннего трения (динамическая вязкость)
- градиент скорости течения газа в направлении, перпендикулярном к площадке ∆S,а η – коэффициент внутреннего трения (динамическая вязкость)

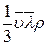 .
.
Количество тепла Q, перенесенное за время ∆t в результате теплопроводности, равно
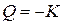
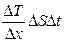 ,
,
где 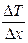 - градиент температуры в направлении, перпендикулярном к площадке ∆S, К – коэффициент теплопроводности, равный
- градиент температуры в направлении, перпендикулярном к площадке ∆S, К – коэффициент теплопроводности, равный

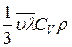 .
.
Первое начало термодинамики может быть записано в виде
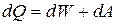 ,
,
где dQ – количество тепла, полученного газом; dW – изменение внутренней энергии газа и dA=pdV – работа, совершаемая газом при изменении его объема. Изменение внутренней энергии газа
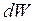
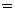
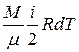 ,
,
где dT – изменение температуры.
Полная работа при изменении объема газа
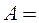
 .
.
Работа, совершаемая при изотермическом изменении объема газа,

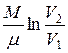 .
.
Давление газа и его объема связаны при адиабатическом процессе уравнением Пуассона
т.е. 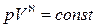 ,
,
где показатель адиабаты 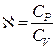 .
.
Уравнение Пуассона может быть записано еще в таком виде

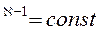 ,
,
т.е.
 ,
,
или 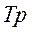
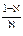
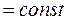 ,
,
т.е. 
Работа, совершаемая при адиабатическом изменении объема газа, может быть найдена по формуле
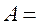
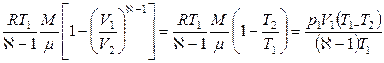 .
.
Где p1 и V1 давление и объем газа при температуре T1.
Уравнение политропического процесса имеет вид:
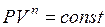 ,
,
или 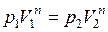 ,
,
где n – показатель политропы (1 ‹ n ‹  ).
).
Коэффициент полезного действия тепловой машины
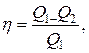
где Q1 – тепло, переданное рабочему телу, и Q2 – тепло, отданное холодильнику. Для идеального цикла Карно
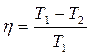 ,
,
где T1 – температура нагревателя, T2 – температура холодильника.
Разность энтропий 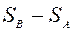 двух состояний В и А определяется формулой
двух состояний В и А определяется формулой
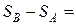
 .
.
Реальные газы.
Уравнение состояния реальных газов (уравнение Ван–дер– Ваальса) для одного киломоля имеет вид:
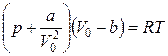 ,
,
где V0 – объем одного киломоля газа, а и b – постоянные, различные для разных газов, p – давление, T – абсолютная температура и R – газовая постоянная.
Уравнение Ван–дер–Ваальса, отнесенное к любой массе М газа, имеет вид:
 ,
,
где V – объем всего газа, µ - масса одного киломоля.
В этом уравнении  - давление, обусловленное силами взаимодействия молекул, и
- давление, обусловленное силами взаимодействия молекул, и 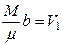 - объем, связанный с собственным объемом молекул.
- объем, связанный с собственным объемом молекул.
Постоянные а и b данного газа связаны с его критической температурой Tк, критическим давлением pk и критическим молярным объемом V0k следующими соотношениями:


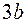 ,
, 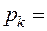
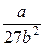 ,
, 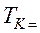
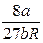 .
.
Эти уравнения можно решить относительно постоянных а и b:
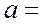
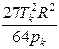 ,
, 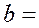
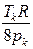 .
.



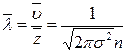 ,
,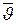 - средняя арифметическая скорость,
- средняя арифметическая скорость,  - среднее число столкновений каждой молекулы с остальными в единицу времени, σ – эффективный диаметр молекулы и n – число молекул в единице объема.
- среднее число столкновений каждой молекулы с остальными в единицу времени, σ – эффективный диаметр молекулы и n – число молекул в единице объема.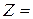
 .
.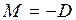
 ,
, - градиент плотности в направлении, перпендикулярном к площадке ∆S и D – коэффициент диффузии, равный
- градиент плотности в направлении, перпендикулярном к площадке ∆S и D – коэффициент диффузии, равный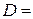
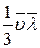 .
.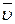 - средняя скорость,
- средняя скорость, 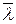 - средняя длина свободного пробега молекул.
- средняя длина свободного пробега молекул.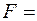
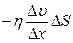 ,
,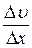 - градиент скорости течения газа в направлении, перпендикулярном к площадке ∆S,а η – коэффициент внутреннего трения (динамическая вязкость)
- градиент скорости течения газа в направлении, перпендикулярном к площадке ∆S,а η – коэффициент внутреннего трения (динамическая вязкость)
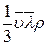 .
.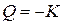
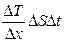 ,
,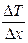 - градиент температуры в направлении, перпендикулярном к площадке ∆S, К – коэффициент теплопроводности, равный
- градиент температуры в направлении, перпендикулярном к площадке ∆S, К – коэффициент теплопроводности, равный
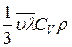 .
.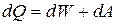 ,
,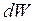
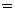
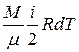 ,
,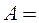
 .
.
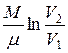 .
.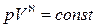 ,
,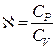 .
.
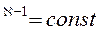 ,
, ,
,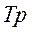
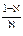
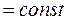 ,
,
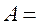
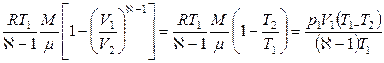 .
.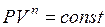 ,
,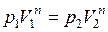 ,
, ).
).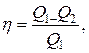
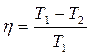 ,
,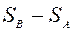 двух состояний В и А определяется формулой
двух состояний В и А определяется формулой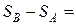
 .
.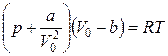 ,
, ,
, - давление, обусловленное силами взаимодействия молекул, и
- давление, обусловленное силами взаимодействия молекул, и 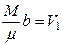 - объем, связанный с собственным объемом молекул.
- объем, связанный с собственным объемом молекул.

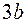 ,
, 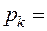
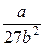 ,
, 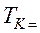
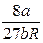 .
.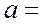
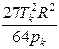 ,
, 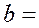
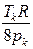 .
.


