Проведение режима
С разрешения учебно-вспомогательного персонала и в его присутствии начали подачу сырья в реактор.
Во время проведения режима:
1. Через каждые 5 минут в таблицу 2 записывали параметры режима: уровень по бюретке, температуру в реакторе, показания газового счетчика.
2. Через каждые 5 минут рассчитывали средний объем подачи сырья в единицу времени, поступившего в реактор за прошедшие 5 минут, и полученные значения заносили в таблицу 2.
3. Следили за температурой в реакторе и объемом подаваемого сырья в реактор, поддерживая их на заданном значении.
4. Отобрали пробу газа: в газовый пикнометр для определения плотности газа. Отбор газа выполнили через 30 минут режима при установившихся параметрах процесса: температуре в реакторе и скорости подачи сырья.
Порядок отбора пробы газа в газовый пикнометр
Взвесили пикнометр на аналитических весах. В таблицу 1 записали вес пикнометра с воздухом, его номер и водное число. Подсоединили пикнометр к байпасам (19 и 19а). Открыли краники (22 и 22а) на пикнометре и крайние зажимы (20 и 20а) на байпасах, а средний зажим (17) закрыли. Через пикнометр пропустили не менее одного литра углеводородного газа, чтобы вытеснить из него воздух. Во время отбора газа в пикнометр записали барометрическое давление и температуру в лаборатории: 751 мм рт. ст., 18,5°С. По окончании отбора газа открыли средний зажим (17), затем закрыли краники (22 и 22а) на пикнометре и крайние зажимы (20 и,20а) на байпасах. Отсоединили пикнометр и взвесили его на аналитических весах. Результат взвешивания занесли в таблицу 1.
Порядок окончания режима
После того, как истекло время процесса, и через реактор был пропущен рассчитанный объем сырья, прекратили подачу сырья в реактор: на сырьевой бюретке закрыли оба краника. Затем выполнили следующие требования:
1. Отключили все электрические приборы на установке.
2. Записали конечное показание газового счетчика.
3. Дали реактору остыть в течение 20 минут, за это время из него стечет оставшийся на насадке продукт.
Пока реактор остывал, рассчитали среднюю температуру режима и средний объем подачи сырья, а также объем полученного газа. Результаты расчетов представлены в таблице 2.
4. Прекратили подачу воды в холодильник, закрыв водяной кран.
5. Закрыли средний зажим.
6. Отсоединили приемную и промежуточную колбы и поместили их в вытяжной шкаф на 2 минуты для удаления газообразных продуктов. После чего указанные колбы и абсорбер взвесили. Результаты взвешиваний занесли в таблицу 1. Полученный жидкий продукт – катализат перелили в колбу для хранения и засыпали в нее хлористый для обезвоживания. Колбу с катализатом и хлористым кальцием закрыли пробкой.
Расчет плотности и молекулярной массы газа
Определение плотности газа
Вес пикнометра с воздухом (g1) — 70,5346 г;
Вес пикнометра с газом процесса (g2) — 70,5827 г;
Температура в лаборатории (t), — 18,5 °C;
Барометрическое давление (Р1), — 751 мм рт. ст.;
Водное число газового пикнометра (В.Ч.), — 0,13017 л.
1) масса воздуха в пикнометре (g3), г:
g3 = γ * В.Ч.,
где у - плотность воздуха, г/л;
Плотность воздуха (γ), г/л:
γ = М/V1
где М - молекулярная масса воздуха, равная 29;
V1 - объем 1 грамм-моля воздуха при температуре определения и барометрическом давлении, л.
По закону Бойля-Мариотта: P1 * V1 / T1 = Р0 * V0 / Т0,
отсюда находим: V1 = Р0 * V0 * Т1 / Р1 * Т0,
где Т0 - температура при нормальных условиях, равная 273° К;
Р0 - давление при нормальных условиях, равное 760 мм рт. ст.;
V0 - объем 1 грамм-моля воздуха при нормальных условиях, равный 22,4л;
T1 - температура в лаборатории в момент отбора газа, °К;
P1 - барометрическое давление в момент отбора газа, мм рт. ст.
V1 = (760 * 22,4 * 291,5) / (751 * 273) = 24,2045 л,
γ = 29/24,2045 = 1,1981 г/л,
g3 = 1,1981 * 0,13017 = 0,1559 г.
2) масса пустого (эвакуированного) пикнометра (go), г:
go = g1 – g3,
где g1 - масса пикнометра с воздухом, г;
g3 - масса воздуха в пикнометре, г.
3) масса газа в пикнометре (g4), г:
g4 = g2-go,
где g2 - масса пикнометра с газом процесса, г;
go - масса пустого (эвакуированного)пикнометра, г.
g4 = 70,5827-70,3784 = 0,2043 г.
4) плотность газа (γ1), г/л:
γ1 = g4/B.Ч.
γ1 = 0,2043/0,13017 = 1,5695 г/л.
5) количество газа, полученного при процессе (Q), г:
Q = γ1* V,
где γ1 - плотность газа при температуре определения и барометрическом давлении, г/л;
V - объем газа, полученный при процессе, л.
Q = 1,5695 * 17,31 = 27,17 г.
6) расчет молекулярной массы газа.
Молекулярная масса газа (МГ), г:
Mr=γo*V0,
где γ0 - плотность газа, приведенная к нормальным условиям, г/л;
V0 - объем газа при нормальных условиях, равный 22,4 л.
Из уравнений: Р1 * V1 / Т1 = Р0 * V0 /Т0,
P1 * M/T1 *γ1 = Р0 * М/Т0 * γ0,
Р1/Т1*γ1=Р0/Т0*γ0
получим γ0 = γ1*P0*T1 / P1 * T0,
где γ1 - плотность газа при температуре определения и барометрическом давлении, г/л.
γ0 = 1,5695 * 760 * 291,5/ 751 * 273 = 1,6959,
Mr = 1,6959 * 22,4 = 37,9890 г ≈ 38 г.
Подготовка фракции и аппарата к испытанию
На рисунке 3 показан аппарат Энглера для определения фракционного состава нефтепродуктов.

1 – термометр;
2 – колба для перегонки;
3 – асбестовая прокладка;
4 – электрический нагрев;
5 – подставка для колбы;
6 – регулятор положения нагревателя;
7 – регулятор напряжения;
8 – вольтметр;
9 – выключатель;
10 – лампочка контроля;
11 – подставка для цилиндра;
12 – цилиндр для сбора дистиллята;
13 – фильтровальная бумага;
14 – отводная трубка холодильника;
15 – водяная баня.
Рисунок 3 - Аппарат для определения фракционного состава
В сухой, чистый измерительный цилиндр отфильтровывали 100 мл предварительно обезвоженного катализата. Цилиндр с катализатом взвешивали на технических весах. Катализат осторожно переливали в колбу для перегонки так, чтобы жидкость не попала в отводную трубку колбы. Пустой цилиндр взвешивали на технических весах и по разнице результатов взвешиваний рассчитывали массу катализата, взятого для перегонки:
mк = mц+к + mц,
где mц+к - масса цилиндра, наполненного 100 мл катализата, г;
mц – масса пустого цилиндра, г.
mк = 219,5 – 140,0 = 59,5 г
В горловину колбы вставили термометр на плотно пригнанной пробке так, чтобы ось термометра совпадала с осью горловины колбы, а нижний конец капилляра находился на одном уровне с самой высокой точкой нижней внутренней стенки пароотводной трубки.
Отводную трубку колбы соединили с холодильником при помощи плотно пригнанной пробки. При этом отводная трубка колбы должна входить в холодильник на 25 - 40 мм и не касаться стенок последнего.
Сухой, чистый мерный цилиндр взвесили на технических весах и поставили так, чтобы нижний отвод трубки холодильника входил в цилиндр не менее чем на 25 мм, но не ниже метки 100 мл, и не касался стенок цилиндра. На время перегонки отверстие цилиндра закрыли ватой или бумагой. Подали воду в холодильник для охлаждения.
Проведение перегонки
Равномерно нагревали колбу с катализатом так, чтобы с момента включения аппарата до падения первой капли дистиллята с нижнего отвода трубки холодильника прошло 5-10 минут.
Температуру, показываемую термометром в момент падения первой капли конденсата в мерный цилиндр, записывали как температуру начала кипения. Затем мерный цилиндр установили так, чтобы конденсат стекал по стенке цилиндра. Далее перегонку вели равномерно со скоростью 20 - 25 капель за 10 секунд. В ходе перегонки отмечали температуры выкипания дистиллята через каждые 5 мл отгона, начиная от 10 мл до температуры конца кипения бензиновой фракции включительно. Результаты представлены в таблице 5.
Таблица 5 – Изменение температуры выкипания дистиллята через каждые 5 мл отгона
| Порядковый номер
| Температура выкипания дистиллята, °С
| Объем дистиллята, мл
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Средняя температура кипения бензиновой фракции составила 116,22°С
По достижении температуры 165 °С, то есть начала кипения дизельного топлива, нагрев колбы прекратили. Дали стечь конденсату в течение 10 минут, закрыли воду и взвесили цилиндр с бензиновой фракцией. По разности результатов взвешиваний рассчитать выход бензиновой фракции:
mб = mц+б + mц,
где mц+к - масса цилиндра, наполненного бензиновой фракцией, г;
mц – масса пустого цилиндра, г.
mб = 120,4 – 92,7 = 27,7 г.
Таблица материального баланса перегонки
По выходам фракций составили материальный баланс перегонки катализата, который представлен в таблице 6.
Таблица 6 – Материальный баланс перегонки
| Взято
| г
| %
| Получено фракции
| г
| % на катализат
|
| Катализат
| 59,5
|
| 1.Бензиновой (50 – 165°С)
2.Газойлевой (165°С +)
| 27,7
31,8
| 46,6
53,4
|
| Итого:
| 59,5
|
| Итого:
| 59,5
|
|
Таблица материального баланса крекинга
При составлении материального баланса по процессу крекинга использовали данные материальных балансов режима и перегонки. При этом учли, что для атмосферной перегонки было взято катализата меньше, чем было его получено на установке.
27,7 г (бензиновой фракции) – 59,5 г (катализата)
X г (бензиновой фракции) – 135,3 г (катализата)
mб = X = 135,3 * 27,7 / 59,5 = 62,99 г бензиновой фракции может быть получено из 142,8 г катализата.
При расчете массы бензиновой фракции учли привес абсорбера:
mбф = mб + mа,
где mб - масса бензиновой фракции, рассчитанная по пропорции, г;
mа – привес абсорбера, г.
mбф = 62,99 + 7,5 =70,49 г.
Таблица 7 – Материальный баланс процесса крекинга
| Взято
| г
| %
| Получено
| г
| % на сырье
|
| Сырья
| 176,3
|
| 1.Газа
2. Катализата
В т.ч.:
-бензиновой фракции (н.к. – к.к.)
-газойлевой фракции
(н.к.+)
3. Кокса + потерь
| 27,17
142,80
70,49
72,31
6,33
| 15,41
81,00
34,00
46,00
5,39
|
| Итого:
| 176,3
|
| Итого:
| 176,3
|
|
14 Методики и результаты определения свойств бензиновой фракции
Определение плотности
Для газойлевой фракции (165°С+) определили  =0,835 г/см3 при 23°С. Средняя температурная поправка принята по таблице 3.1 [1] и составляет 0,000725:
=0,835 г/см3 при 23°С. Средняя температурная поправка принята по таблице 3.1 [1] и составляет 0,000725:

Вывод
В ходе лабораторной работы проведен процесс каталитического крекинга дизельной фракции 165-348°С на катализаторе Цеокар–100 (свежий) при температуре 500°С. Процесс проводился с целью получения светлых продуктов: высокооктанового компонента бензина (бензиновой фракция), газов. Объемная скорость подачи сырья в процессе 1,3 ч-1 .
Далее составлена таблица для сравнения полученных результатов при разных объемных скоростях процесса 1,3 ч-1 , 1,5 ч-1 и 1,7 ч-1.
Таблица 8 – Сравнительная таблица результатов лабораторной работы
| Параметры
| I подгруппа
| II подгруппа
| III подгруппа
|
| Объемная скорость подачи сырья w, ч-1
| 1,3
| 1,5
| 1,7
|
| ОЧММ
| 78,8
| 81,2
| 78,2
|
| ОЧИМ
| 84,8
| 89,2
| 83,2
|
| По материальному балансу каталитического крекинга
|
| Газ, %
| 15,41
| 7,19
| 15,10
|
| Бензиновая фракция, %
| 34,00
| 30,47
| 38,63
|
| Газойлевая фракция, %
| 46,00
| 59,08
| 61,37
|
| Кокс+потери, %
| 5,39
| 3,26
| 0,13
|
По результатам работы I, II и III подгрупп построили графики зависимости октановых чисел бензиновой фракции ОЧММ и ОЧИМ от объемной скорости подачи сырья, представленные на рисунке 5. Из графиков следует, что максимальные значения октановых чисел достигаются при объемной скорости подачи сырья, равной 1,5 ч-1.

Рисунок 5 – Зависимость октановых чисел бензиновой фракции от объемной скорости подачи сырья
Также нами был построен график зависимости процентного содержания продуктов в конечной смеси от объемной скорости подачи сырья, представленный на рисунке 6.
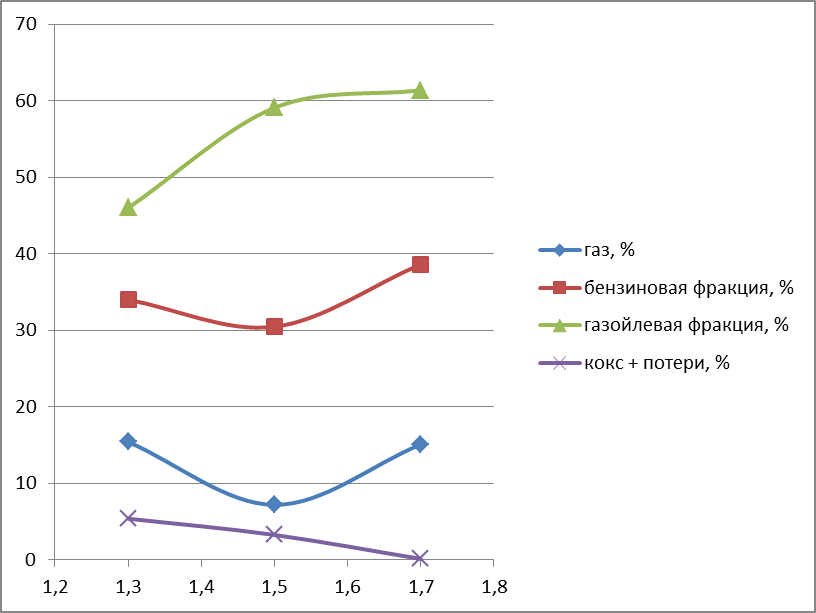
Рисунок 6 – Зависимость процентного содержания продуктов в конечной смеси от объемной скорости подачи сырья
Из рисунка 6 следует, что максимальный выход целевых продуктов, а именно газа и бензиновой фракции наблюдается при объемной скорости подачи сырья, равной 1,7 ч-1.
Несмотря на высокие октановые числа при объемной скорости, равной 1,5 ч-1, максимальный выход целевых продуктов достигается при объемной скорости, равной 1,7 ч-1.
Отсюда можно сделать вывод, что хороший выход газа и бензиновой фракции достигается при скорости подачи сырья в реактор 1,7 ч-1.
Проведение режима
С разрешения учебно-вспомогательного персонала и в его присутствии начали подачу сырья в реактор.
Во время проведения режима:
1. Через каждые 5 минут в таблицу 2 записывали параметры режима: уровень по бюретке, температуру в реакторе, показания газового счетчика.
2. Через каждые 5 минут рассчитывали средний объем подачи сырья в единицу времени, поступившего в реактор за прошедшие 5 минут, и полученные значения заносили в таблицу 2.
3. Следили за температурой в реакторе и объемом подаваемого сырья в реактор, поддерживая их на заданном значении.
4. Отобрали пробу газа: в газовый пикнометр для определения плотности газа. Отбор газа выполнили через 30 минут режима при установившихся параметрах процесса: температуре в реакторе и скорости подачи сырья.
Порядок отбора пробы газа в газовый пикнометр
Взвесили пикнометр на аналитических весах. В таблицу 1 записали вес пикнометра с воздухом, его номер и водное число. Подсоединили пикнометр к байпасам (19 и 19а). Открыли краники (22 и 22а) на пикнометре и крайние зажимы (20 и 20а) на байпасах, а средний зажим (17) закрыли. Через пикнометр пропустили не менее одного литра углеводородного газа, чтобы вытеснить из него воздух. Во время отбора газа в пикнометр записали барометрическое давление и температуру в лаборатории: 751 мм рт. ст., 18,5°С. По окончании отбора газа открыли средний зажим (17), затем закрыли краники (22 и 22а) на пикнометре и крайние зажимы (20 и,20а) на байпасах. Отсоединили пикнометр и взвесили его на аналитических весах. Результат взвешивания занесли в таблицу 1.
Порядок окончания режима
После того, как истекло время процесса, и через реактор был пропущен рассчитанный объем сырья, прекратили подачу сырья в реактор: на сырьевой бюретке закрыли оба краника. Затем выполнили следующие требования:
1. Отключили все электрические приборы на установке.
2. Записали конечное показание газового счетчика.
3. Дали реактору остыть в течение 20 минут, за это время из него стечет оставшийся на насадке продукт.
Пока реактор остывал, рассчитали среднюю температуру режима и средний объем подачи сырья, а также объем полученного газа. Результаты расчетов представлены в таблице 2.
4. Прекратили подачу воды в холодильник, закрыв водяной кран.
5. Закрыли средний зажим.
6. Отсоединили приемную и промежуточную колбы и поместили их в вытяжной шкаф на 2 минуты для удаления газообразных продуктов. После чего указанные колбы и абсорбер взвесили. Результаты взвешиваний занесли в таблицу 1. Полученный жидкий продукт – катализат перелили в колбу для хранения и засыпали в нее хлористый для обезвоживания. Колбу с катализатом и хлористым кальцием закрыли пробкой.
Расчет плотности и молекулярной массы газа
Определение плотности газа
Вес пикнометра с воздухом (g1) — 70,5346 г;
Вес пикнометра с газом процесса (g2) — 70,5827 г;
Температура в лаборатории (t), — 18,5 °C;
Барометрическое давление (Р1), — 751 мм рт. ст.;
Водное число газового пикнометра (В.Ч.), — 0,13017 л.
1) масса воздуха в пикнометре (g3), г:
g3 = γ * В.Ч.,
где у - плотность воздуха, г/л;
Плотность воздуха (γ), г/л:
γ = М/V1
где М - молекулярная масса воздуха, равная 29;
V1 - объем 1 грамм-моля воздуха при температуре определения и барометрическом давлении, л.
По закону Бойля-Мариотта: P1 * V1 / T1 = Р0 * V0 / Т0,
отсюда находим: V1 = Р0 * V0 * Т1 / Р1 * Т0,
где Т0 - температура при нормальных условиях, равная 273° К;
Р0 - давление при нормальных условиях, равное 760 мм рт. ст.;
V0 - объем 1 грамм-моля воздуха при нормальных условиях, равный 22,4л;
T1 - температура в лаборатории в момент отбора газа, °К;
P1 - барометрическое давление в момент отбора газа, мм рт. ст.
V1 = (760 * 22,4 * 291,5) / (751 * 273) = 24,2045 л,
γ = 29/24,2045 = 1,1981 г/л,
g3 = 1,1981 * 0,13017 = 0,1559 г.
2) масса пустого (эвакуированного) пикнометра (go), г:
go = g1 – g3,
где g1 - масса пикнометра с воздухом, г;
g3 - масса воздуха в пикнометре, г.
3) масса газа в пикнометре (g4), г:
g4 = g2-go,
где g2 - масса пикнометра с газом процесса, г;
go - масса пустого (эвакуированного)пикнометра, г.
g4 = 70,5827-70,3784 = 0,2043 г.
4) плотность газа (γ1), г/л:
γ1 = g4/B.Ч.
γ1 = 0,2043/0,13017 = 1,5695 г/л.
5) количество газа, полученного при процессе (Q), г:
Q = γ1* V,
где γ1 - плотность газа при температуре определения и барометрическом давлении, г/л;
V - объем газа, полученный при процессе, л.
Q = 1,5695 * 17,31 = 27,17 г.
6) расчет молекулярной массы газа.
Молекулярная масса газа (МГ), г:
Mr=γo*V0,
где γ0 - плотность газа, приведенная к нормальным условиям, г/л;
V0 - объем газа при нормальных условиях, равный 22,4 л.
Из уравнений: Р1 * V1 / Т1 = Р0 * V0 /Т0,
P1 * M/T1 *γ1 = Р0 * М/Т0 * γ0,
Р1/Т1*γ1=Р0/Т0*γ0
получим γ0 = γ1*P0*T1 / P1 * T0,
где γ1 - плотность газа при температуре определения и барометрическом давлении, г/л.
γ0 = 1,5695 * 760 * 291,5/ 751 * 273 = 1,6959,
Mr = 1,6959 * 22,4 = 37,9890 г ≈ 38 г.




 =0,835 г/см3 при 23°С. Средняя температурная поправка принята по таблице 3.1 [1] и составляет 0,000725:
=0,835 г/см3 при 23°С. Средняя температурная поправка принята по таблице 3.1 [1] и составляет 0,000725:




