Теплоемкость политропного процесса  можно определить из выражения
можно определить из выражения
 = n
= n

где k - показатель адиабаты.
Найдем значение  и n для изопроцессов определения сведем результаты в таблицу
и n для изопроцессов определения сведем результаты в таблицу
| процесс
| 
| n
|
| T=const
| 
|
|
| p=const
| 
|
|
| v=const
| 
| 
|
| q=const
|
| k
|
Изобразим зависимость  (n) графически
(n) графически

В деапазоне 1< n < k теплоемкость процессов отрицательная, т.е. с подводом теплоты температура системы уменьшается, а с отводом теплоты - увеличивается.
Смысл отрицательной теплоемкости заключается в том, что вся подведенная теплота расходуется на работу и, кроме этого, на работу затрачивается еще и часть внутренней энергии системы

dq=du+dl подвод тепла


 dq=du+dl отвод тепла
dq=du+dl отвод тепла
Энергетические характеристики политропных процессов
Изменение энтропии
По аналогии с интегралом работы было получено выражение для подсчета количества теплоты в ТДП. Для этого был введен параметр состояния системы – энтропия.
Энтропия является функцией состояния. Ее изменение в пределах процесса определяется как разность конечного и начального значений. Также как внутренняя энергия она определяется с точностью до произвольной постоянной. В ТДП нужно знать только ее изменение. Энтропия, и ее изменение не поддается физическому определению и измерению, а является расчетной величиной.




Работа расширения /сжатия в политропном процессе.
Работа расширения /сжатия в политропном процессе.
 ;
; 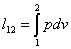
Используя связь параметров, можно найти значение интеграла работы.
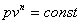
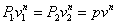

Параметры состояния в граничных точках известны, известен показатель политропы n
Подставляем полученную функцию  в уравнение для работы и интегрируем
в уравнение для работы и интегрируем

Можно получить и другие формулы для расчета работы.
Применяя уравнение состояния идеального газа  , получаем
, получаем

Располагаемая работа
Располагаемая работа: 

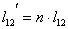
Количество теплоты
Теплота является формой обмена энергией между системой и ОС. При этом обмен энергией происходит на микроуровне.
Q = 
 T
T

 =
=  =
= 
 T,
T,  – удельное количество теплоты.
– удельное количество теплоты.


Изменение внутренней энергии
Внутренняя энергия ТДС зависит от температуры рабочего тела. В ТДС абсолютное значение внутренней энергии не определяют. Имеет смысл только ее изменение в термодинамическом процессе. Для идеального газа:
∆u12 =  ;
; 

Изменение энтальпии
Одной из энергетических характеристик ТДС является тепловая функция или энтальпия.
Если термомеханическую систему рассматривать как состоящую из макротела (газа) и поршня с грузом P =  , уравновешивающего давление газа
, уравновешивающего давление газа 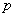 внутри сосуда, то такая система называется расширенной. Энтальпия или энергия такой системы E равна внутренней энергии газа U плюс потенциальная энергия поршня с грузом
внутри сосуда, то такая система называется расширенной. Энтальпия или энергия такой системы E равна внутренней энергии газа U плюс потенциальная энергия поршня с грузом 
I = E = U + 
Энтальпия в данном состоянии представляет собой сумму внутренней энергии тела и работы, которую необходимо затратить, чтобы тело объемом V ввести в окружающую среду, имеющую давление p и находящуюся c телом в равновесном состоянии. Энтальпия системы I аналогично внутренней энергии имеет вполне определенное значение для каждого состояния, т.е. является функцией состояния. В процессе изменения состояния

I закон термодинамики
Для политропного процесса уравнение I закона термодинамики можно записать в виде:

 =
=  +
+  уравнение Майера.
уравнение Майера.
При p=const  n=0
n=0 



 можно определить из выражения
можно определить из выражения = n
= n
 и n для изопроцессов определения сведем результаты в таблицу
и n для изопроцессов определения сведем результаты в таблицу







 dq=du+dl отвод тепла
dq=du+dl отвод тепла



 ;
; 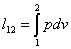
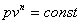
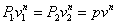

 в уравнение для работы и интегрируем
в уравнение для работы и интегрируем
 , получаем
, получаем


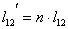

 T
T
 =
=  =
= 
 ;
; 

 , уравновешивающего давление газа
, уравновешивающего давление газа 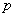 внутри сосуда, то такая система называется расширенной. Энтальпия или энергия такой системы E равна внутренней энергии газа U плюс потенциальная энергия поршня с грузом
внутри сосуда, то такая система называется расширенной. Энтальпия или энергия такой системы E равна внутренней энергии газа U плюс потенциальная энергия поршня с грузом 



 уравнение Майера.
уравнение Майера. n=0
n=0 

