Рассматривалось влияние основности шлака на активность оксида марганца в шлаке /11/. В целом повышение основности шлака от 0,2 до 1,1-1,3 повышает активность aMnO примерно в 25-30 раз. Но условия восстановления (MnO) из основного шлака по его активности в 6-7 раз хуже, чем из чистой MnOтв. Поэтому, принимая меры к повышению aMnO в шлаке, необходимо одновременно принимать меры к уменьшению его количества, усилению восстановления (MnO) из твердой руды.
Влияние температуры на активность (MnO) в шлаке невелико. В кислых шлаках повышение температуры на 400 0С увеличивает aMnO в 1,1-1,3 раза. В основных шлаках, наоборот, повышение температуры несколько понижает aMnO.
Были проведены расчеты, по результатам которых сделан вывод о том, что высокое извлечение марганца из бедной руды может быть получено только при 1650-1700 0С и шлаках основностью (CaO+MgO)/SiO2»1.6.
Восстановление оксида марганца
Элементы, имеющие при данной температуре сродство к кислороду больше, чем марганец, могут восстанавливать марганец из оксида. При температурах сталеплавильных процессов восстановителями для марганца могут являться углерод, алюминий, кремний.
7.1. Восстановление оксида марганца углеродом
Восстановление закиси марганца углеродом происходит по следующим реакциям
MnO + Cгр= Mnж + СО, dG0=272740-160.35T Дж/моль, (5)
MnO +10/7Cгр= 1/7Mn7C3 +CO, dG0=265550-168.0T Дж/моль. (6)
Эти реакции начинаются (рсо=98 кПа) соответственно при 1428 и 1307 0С.
Активность марганца в его расплаве, насыщенном углеродом, может быть описана уравнением
Lg aMn = -  + 1,95. (7)
+ 1,95. (7)
В реальных условиях восстановление марганца из руды по реакции (5) осложняется взаимодействием оксида марганца с кремнеземом по реакции
m MnO + n SiO2 = m MnO×n SiO2. (8)
Эта реакция начинается в твердых фазах при температурах около 900 0С. Она приводит к образованию легкоплавкого шлака с температурой плавления 1230-1250 0С. Поэтому полнота восстановления марганца из руды определяется не только температурными факторами и активностью марганца в металле, но и активностью марганца в образующемся шлаке. Значительную роль играют и кинетические факторы.
Потери марганца в шлаке (bMn) связаны c содержанием кремнезема в руде уравнением
bMn = m(SiO2)p  , (9)
, (9)
где (Mn)p и (SiO2)р – концентрации марганца и кремнезема в руде,
(Mn)шл - концентрация марганца в отвальном шлаке.
Численный коэффициент m связан с составом шлака. В системе CaO-MgO- SiO2 он равен» 3,3, в системе CaO-MgO-MnO-SiO2 при MgO» 10 % этот коэффициент снижается до 3,0, а при MgO=26-28 % - до 2,7 /12/.
Образующийся легкоплавкий первичный шлак, согласно диаграмме MnO-SiO2, содержит SiO2»37 % и MnO»63 %. При подобном составе первичного двухкомпонентного шлака в нем растворяется 1,3 кг марганца на 1 кг кремнезема.
Это означает, что при восстановлении марганца из богатой руды
(SiO2 £ 10-12 %) в шлак переходит около трети марганца, вносимого шихтой, а при использовании бедной руды (SiO2 ³ 20 %, MnO ~ 44 %) – не менее 60 %.
Далее в первичном шлаке растворяются и другие окислы пустой породы руды (Al2O3, CaO, MgO), флюсы и закись марганца. И если не обеспечивается высокая скорость реакций (5) и (8), в шлак может переходить от 30 до 70 % марганца из богатой руды и весь марганец, вносимый бедной рудой. Поэтому особенно важно обеспечение оптимальных условий восстановления закиси марганца из шлака.
7.2 Восстановление оксидов марганца кремнием
Восстановление оксидов марганца кремнием – экзотермический процесс, идущий с выделением тепла, поэтому реакции могут протекать при любых температурах, однако с заметной скоростью восстановление марганца кремнием протекает при появлении жидких фаз.
Была проанализирована /12/ возможность восстановления оксидов марганца чистым кремнием и его сплавами. При использовании в качестве восстановителя чистого кремния наиболее легкоплавкой фазой будет кремний в системе чистый оксид-восстановитель, поэтому процесс восстановления начнется при температурах выше температур плавления кремния, т.е. выше 1700 К.
При использовании в качестве восстановителя сплавов кремния температура плавления жидкой фазы понижается до 1520-1560 К в случае использования сплавов систем Mn – Si – Fe и до 1490-1570 К при использовании стандартных сплавов ферросилиция. В этом случае восстановление может идти как оксида Mn2O3, так и MnO. Оба эти оксида термически устойчивы.
Процессы восстановления могут быть описаны уравнениями
1/2(Mn3O4)+Siж= 3/2Mnж + SiO2(т), dG0T= -237075+11.56T, (17)
2(Mn3O4)+Siж = 6MnO + SiO2(т), dG0T=-558240+14.69T, (18)
2(MnO) + Siж = 2Mnж + SiO2(т), dG0T=-130020+20.3T. (19)
Константа равновесия реакции (18) значительно больше, чем реакции (17). При температуре 2200 К константа равновесия реакции (17) составляет 1.055×105, тогда как для реакции (18) она равна 1,04×1014. Еще больше различие между величинами констант при 1600-1800 К. Это означает, что Mn3O4 реагирует только по реакции (18), а конечные показатели процесса могут определяться только равновесием реакции (19).
Таким образом, процесс восстановления оксидов марганца кремнием можно описать схемой, которая позволяет проанализировать условия реального силикотермического процесса восстановления. Она включает:
- частичную диссоциацию высших оксидов марганца в процессе нагрева и плавления марганецсодержащего оксидного материала MnO2 – Mn2O3 – Mn3O4 – MnO;
- взаимодействие кремния восстановителя с высшими оксидами марганецсодержащего расплава
MnxOy + 0,5(y-x)Si = xMnO + 0,5(y-x)SiO2 ; (20)
- взаимодействие кремния восстановителя с кислородом атмосферы и кислородом, образующимся при диссоциации высших оксидов марганца
Si + O2 = SiO2; (21)
- взаимодействие кремния восстановителя с оксидом марганца в расплаве
2MnO + Si = 2Mn + SiO2. (22)
Проведенные эксперименты показывают, что при восстановлении оксидов MnO и Mn2O3 газовая фаза содержит свободный кислород. Это приводит к снижению полезного использования кремния. Избежать потерь восстановителя по реакциям (20) и (21) можно только в случае использования в качестве окислителя предварительно подготовленной марганцевой руды или при восстановлении марганца из оксидного расплава.
Равновесное распределение марганца при его восстановлении из оксида марганца кремнием по реакции
2MnOж + Siж = 2Mnж + SiO2ж.нас. (23)
может быть найдено из уравнения
lg 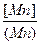 =
=  lgKp - lg
lgKp - lg  –
–  lg
lg  + lg1,37. (24)
+ lg1,37. (24)
Выражение для константы равновесия имеет вид
LgKp =  - 3,54. (25)
- 3,54. (25)
Равновесное распределение марганца тогда определится уравнением
lg 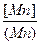 =
= 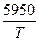 -1,629-lg
-1,629-lg  -
-  lg
lg 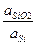 . (26)
. (26)
Для получения высокого распределения марганца необходимо понизить активность кремнезема, то есть его необходимо ошлаковать. Обычно снижают активность кремнезема введением в систему СаО.
7.3 Восстановление оксида марганца алюминием
Восстановление оксидов марганца алюминием идет по экзотермическим реакциям /12/. Высшие оксиды восстанавливаются с выделением большого количества тепла. Это приводит к тому, что процесс идет взрывообразно с выделением большого количества выбросов.
Восстановление оксидов Mn3O4 и MnO можно описать реакциями
1/2 Mn3O4 + 3/4Al = 3/2Mn + 2/3Al2O3, dG0T = -410820+28,23T, (10)
2MnO + 4/3Al = 2Mn +2/3Al2O3, dG0T = -303760+36,96T, (11)
2 Mn3O4 +4/3Al = 6MnO + 2/3Al2O3, dG = 730990+1,97T. (12)
Расчеты, проведенные авторами в работе /13/, показали, что все технико-экономические показатели восстановления оксидов марганца алюминием определяются процессом, который описывается реакцией (11).
Известно, что полнота протекания реакции определяется получением продуктов реакции в жидком виде. В результате протекания реакции (11) тугоплавким продуктом является глинозем с температурой плавления, превышающей 2300 К. Восстановление оксидов марганца при прямом легировании стали алюминием происходит в интервале температур 1800-2400 К. Равновесное распределение марганца можно найти, рассмотрев реакцию
2MnOж + 4/3Alж = 2Mnж + 2/3Al2O3 ж.нас. (13)
Константа этой реакции
Kp=  . (14)
. (14)
Константа реакции может быть также найдена по уравнению
LgKp=  -3,44. (15)
-3,44. (15)
Тогда
lg 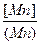 =
=  -1,584-lg gMn-1/3 lg
-1,584-lg gMn-1/3 lg  . (16)
. (16)
Снижение активности глинозема приводит к более полному восстановлению оксида марганца.1.5.3 Восстановление оксида марганца кремнием.



 + 1,95. (7)
+ 1,95. (7) , (9)
, (9)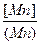 =
=  lgKp - lg
lgKp - lg  –
–  + lg1,37. (24)
+ lg1,37. (24) - 3,54. (25)
- 3,54. (25)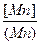 =
= 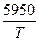 -1,629-lg
-1,629-lg  -
- 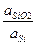 . (26)
. (26) . (14)
. (14) -3,44. (15)
-3,44. (15) -1,584-lg gMn-1/3 lg
-1,584-lg gMn-1/3 lg  . (16)
. (16)


