Цель: оценить качество знаний по теме «Теоретические основы органической химии»
Примерный вариант контрольной работы для самоподготовки
1. Назовите соединения по заместительной номенклатуре IUРАС

2. Напишите структурные формулы следующих соединений: 2-гидрокси-2-фенилэтановой кислоты, о-аминофенола.
3. Какие из приведенных соединений содержат сопряженные фрагменты? 
Укажите вид сопряжения. Укажите вид гибридизации орбиталей каждого атома углерода. Изобразите электронное и пространственное строение атома углерода в sр2-гибридизации.
4.Выберите из приведенных структур ароматические: анилин, циклопентадиенид-ион, циклогексанол. Приведите критерии ароматичности и обоснуйте принадлежность выбранных структур к ароматическим.
5. Укажите вид и знак электронных эффектов в следующих соединениях: толуол, нитробензол, анилин, бутен-2-овая кислота. Обозначьте эффекты графически.
6. Выберите соединение, молекула которого хиральна: 2,3 -дигидроксипропаналь или 3-гидроксипропаналь. Напишите формулы стереоизомеров. Назовите их по D,L- и R,S-номенклатуре (с использованием правил преобразования формул Фишера). Дайте определение энантио- и диастереомеров.
7. Дайте определение конформации. Напишите в виде проекций Ньюмена конформации 1,1-дихлорэтана. Приведите их энергетическую кривую.
8.Дайте определение понятия «кислота» по теории Брёнстеда. Сравните кислотность фенола, n-нитрофенола, n-аминофенола, основываясь на стабильности соответствующих анионов. Напишите уравнение реакции образования натриевой соли для наиболее сильной кислоты.
9. Дайте определение понятия «основание» по теории Брёнстеда. Сравните основность в растворе этиламина, диэтиламина, анилина. Напишите уравнение реакции солеобразования для наиболее сильного основания.

Глава 2. Углеводороды
Лабораторно-практическое занятие № 13. «Предельные углеводороды: строение и свойства» (2ч)
Цель: сформировать знания о строении и свойствах предельных углеводородов.
Вопросы для обсуждения:
1. Предельные углеводороды, их применение в фармации
2. Реакционные центры предельных углеводородов.
3. Физические свойства предельных углеводородов.
4. Реакции замещения, протекающие с разрывом С-Н связи (галогенирование, нитрование, сульфохлорирование, сульфоокисление).
5. Реакции, протекающие с разрывом С-С и С-Н связей (окисление, термические превращения алканов).
Материалы и примеры для самостоятельного изучения
Пример 1. Какой продукт преимущественно образуется в результате реакции бромирования изооктана?
Решение. Насыщенный углеводород изооктан (2,2,4-триметилпентан) принят за стандарт моторного топлива с октановым числом 100. Все атомы углерода в этом соединении находятся в состоянии sp3-гибридизации. В молекуле изооктана имеются только неполярные С—С и малополярные С—Н σ-связи. Это обусловливает участие их в реакциях радикального замещения SR. Реакционными центрами, как правило, служат пространственно более доступные связи С—Н. Атомы водорода в молекуле изооктана связаны с первичным, вторичным и третичным атомами углерода. Неравноценность этих связей определяет региоселективность процесса бромирования: при наличии первичных, вторичных и третичных атомов углерода бромирование проходит преимущественно у третичного атома.
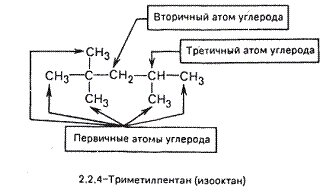
Взаимодействие изооктана с бромом по свободнорадикальному механизму можно представить в виде трех стадий:
Инициирование. Происходит гемолитическое расщепление молекулы брома (реагента) на два свободных радикала либо при высокой температуре (термолиз), либо облучении УФ-светом (фотолиз).

Рост цепи. Радикал брома атакует третичный атом углерода в молекуле изооктана (субстрата).

Образовавшийся алкильный свободный радикал взаимодействует с молекулой брома, что приводит к появлению продукта реакции замещения — 2-бромо-2,4,4-триметилпентана — и радикала брома.

Стадия роста цепи повторяется многократно. Процесс имеет цепной характер. Достаточно небольшого первоначального количества свободных радикалов, чтобы реакция замещения прошла полностью. В результате в реакционной смеси накапливаются свободнорадикальные частицы.
Обрыв цепи. Прекращается цепная реакция за счет соединения между собой любых свободнорадикальных частиц. Одна из реакций осуществляется между третичным алкильным радикалом и радикалом брома.

Таким образом, вследствие региоселективнести процесса бронирования преимущественным продуктом реакции является 2-бромо-2,4,4-триметилпентан.

Пример 2. В чем отличие химических свойств малых циклов от свойств линейных аналогов и больших циклов?
 Решение. Э лектронное строение циклопропанов во многом приближается к строению алкенов: кольцо плоское, а большая часть электронной плотности вынесена из межатомного пространства во внешнюю часть кольца. Естественно, как и в случае этиленов, это облегчает атаку атомов углерода кольца электрофильными агентами, обеспечивая возможность протекания реакций присоединения.
Решение. Э лектронное строение циклопропанов во многом приближается к строению алкенов: кольцо плоское, а большая часть электронной плотности вынесена из межатомного пространства во внешнюю часть кольца. Естественно, как и в случае этиленов, это облегчает атаку атомов углерода кольца электрофильными агентами, обеспечивая возможность протекания реакций присоединения.
Высокая напряженность цикла обусловливает легкость разрыва связи С—С, поэтому реакции циклопропанов с электрофилами завершаются, как правило, образованием линейных продуктов 1,3-присоединения в отличие от этиленов, дающих продукты 1,2-присоединения без разрыва 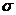 -связи С—С этиленового фрагмента исходного алкена. Однако степень ненасыщенности циклопропанов заметно ниже, чем у алкенов, и некоторые их реакции протекают так же, как и у алканов:
-связи С—С этиленового фрагмента исходного алкена. Однако степень ненасыщенности циклопропанов заметно ниже, чем у алкенов, и некоторые их реакции протекают так же, как и у алканов:

Четырехчленное кольцо циклобутанов напряжено меньше циклопропановых. Циклобутаны значительно более устойчивы, чем циклопропаны, и не вступают в реакции электрофильного присоединения, но, подобно алканам, для них характерны реакции радикального замещения. Раскрытие кольца происходит лишь при гидрировании:

Задачи для самостоятельного решения
Номенклатура и изомерия
Задача 13.1. Назовите по систематической (IUPAC) номенклатуре следующие алканы:

Укажите первичные, вторичные, третичные и четвертичные атомы углерода.
Задача 13.2. Составьте структурные формулы следующих алициклических соединений:
1) циклогексанола;
2) циклогексанона;
3) циклопентанкарбоновой кислоты;
4) циклогексен-3-карбальдегида,
5) 3,3-диметил-4-циклопентилбутанола-2.












 Решение. Э лектронное строение циклопропанов во многом приближается к строению алкенов: кольцо плоское, а большая часть электронной плотности вынесена из межатомного пространства во внешнюю часть кольца. Естественно, как и в случае этиленов, это облегчает атаку атомов углерода кольца электрофильными агентами, обеспечивая возможность протекания реакций присоединения.
Решение. Э лектронное строение циклопропанов во многом приближается к строению алкенов: кольцо плоское, а большая часть электронной плотности вынесена из межатомного пространства во внешнюю часть кольца. Естественно, как и в случае этиленов, это облегчает атаку атомов углерода кольца электрофильными агентами, обеспечивая возможность протекания реакций присоединения.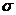 -связи С—С этиленового фрагмента исходного алкена. Однако степень ненасыщенности циклопропанов заметно ниже, чем у алкенов, и некоторые их реакции протекают так же, как и у алканов:
-связи С—С этиленового фрагмента исходного алкена. Однако степень ненасыщенности циклопропанов заметно ниже, чем у алкенов, и некоторые их реакции протекают так же, как и у алканов:





