Цель занятия:
Изучить механизм буферного действия буферных систем и приобрести практические навыки определения буферной ёмкости
Содержание занятия:
1. Обсуждение теоретических вопросов по теме.
2. Выполнение демонстрационных и лабораторных работ, обсуждение их результатов, оформление научного отчета.
Вопросы, предлагаемые для обсуждения на занятии:
1. Кислотность общая, активная, потенциальная. Влияние активной кислотности на биологические процессы.
2. Буферные системы. Механизм буферного действия.
3. Уравнение Гендерсона-Гассельбаха для расчета С(Н+) и С(ОНˉ) двух основных типов буферных систем. Факторы, влияющие на рН раствора.
4. Буферная ёмкость, её расчет. Факторы, влияющие на буферную ёмкость.
5. Буферные системы крови. Механизм действия буферных систем крови. Понятие о кислотно-щелочном равновесии и щелочном резерве крови.
Лабораторная работа 1. Приготовление буферных смесей.
В семи пробирках готовят ацетатные буферные смеси из растворов уксусной кислоты и ее соли с молярной концентрацией эквивалента 0.1 моль/л, объёмы которых указаны в таблице.
| №
пробирки
| Состав буферной смеси, мл
| рН смеси
(расчетн)
| Окраска после прибавления
индикатора (метилового красного 4.2–6.3)
|
| СН3СООН
0.1 моль
| СН3СООNa
0.1 моль/л
|
|
|
0.5
0.2
|
9.5
9.8
|
|
|
В каждую пробирку прибавляют по 3 капли индикатора метилового красного, перемешивают и сравнивают окраску буферных смесей при хорошем освещении, на белом фоне, глядя сверху вниз сквозь раствор. Окраску растворов отмечают в таблице.
Затем рассчитывают С(Н+) и рН одного из буферных растворов (по указанию преподавателя), результат расчета записывают в таблицу. Значения С(Н+) и рН для остальных шести растворов получают у преподавателя. Чертят на миллиметровой бумаге буферную кривую, показывающую связь рН буферного раствора с объёмом одного из его компонентов. По оси ординат откладывают 10 единиц масштаба (1 мл CH3COONa = 1 см), принимая начало координат за 0. По оси абсцисс, принимая начало координат равным 3, откладывают область значений рН от 3 до 7 (единица рН = 2 см).
Пример расчета рН буферной смеси.
Рассчитать рН буферной смеси, состоящей из раствора СН3СООН объёмом 4.5 мл и молярной концентрацией эквивалента С(СН3СООН) = 0.1 моль/л и раствора СН3СООNa объемом 5.5 мл с молярной концентрацией эквивалента С(СН3СООNa) = 0.1 моль/л
С(Н+) = Кд ∙ 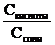 = Кд ∙
= Кд ∙ 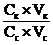
рН = -lg C(H+), откуда рН = -lg Кд + lg 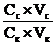
рН = -lg(1,8 ∙ 10-5) + lg  = -(lg1,8 – 5) + 0,0872 =
= -(lg1,8 – 5) + 0,0872 =
=4,8319»4,83
Оформление работы:
Привести таблицу и расчеты С(Н+) и рН указанного буферного раствора.
Вклеить график «Буферная кривая».
Лабораторная работа 2. Определение буферной емкости буферного раствора.
Получают у преподавателя исследуемый раствор с известным значением рН0 (записать в тетради).
В две чистые колбы отмеряют пипеткой по 10 мл исследуемого раствора. В одну колбу добавляют 2 капли фенолфталеина и титруют рабочим раствором NaОН с молярой концентрацией эквивалента С(1NaOH) = 0.1 моль/л до появления слабо-розовой окраски, рН раствора при этом станет равным 8.4 (рНщ). В другую колбу добавляют 1 каплю метилоранжа и титруют рабочим раствором HCl = 0.1 моль/л до появления оранжево-розовой окраски, рН раствора при этом станет равным 3.4 (рНк).
Вычисляют буферную емкость раствора по отношению к кислоте (Вк) и щелочи (Вщ) и результат проверяют у преподавателя. Вк и Вщ рассчитывают с точностью до трех значащих цифр и округляют до двух.
Вщ = 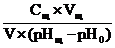 , моль/л; Вк =
, моль/л; Вк =  , моль/л
, моль/л
где Vщ, Vк – объемы (в мл) рабочего раствора щелочи или кислоты, затраченный на титрование V мл исследуемого буферного раствора;
Сщ, Ск – молярная концентрация эквивалента рабочего раствора щёлочи или кислоты.
Оформление работы:
Указать рН0 буферного раствора; Vщ, рНщ и индикатор; Vк, рНк и индикатор; привести расчет Вщ и Вк и вывод, указав, во сколько раз Вщ больше (или меньше), чем Вк.
Расчет общей, активной и потенциальной кислотности буферного раствора.
Для расчетов используют данные (рН0 и Vщ) для буферного раствора, полученного у преподавателя при определении буферной ёмкости.
Общая кислотность равна общей концентрации кислоты (С0), выраженной через молярную концентрацию эквивалента и определяемой титрованием рабочим раствором щелочи.
С0 =  , моль/л;
, моль/л;
Активная кислотность равна концентрации ионов водорода С(Н+) и рассчитывается из значений рН0 буферного раствора.
Пример расчета С(Н+).
Вычислить С(Н+) раствора с рН0 = 5,6.
рН = –lg C(H+) = 5,6; lgC(H+) = –5,6; C(H+) = 10-5,6 = 2,51 ∙ 10-6 моль/л.
Потенциальная кислотность равна концентрации недиссоциированных молекул кислоты, т.е. разности между общей и активной кислотностями.
Спот = Собщ – С(Н+)
Индикаторы
| Индикаторы
| рК
| Зона перехода
|
| Метиловый оранжевый
| 3,7
| 3,1–4,4
|
| Метиловый красный
| 5,1
| 4,2–6,3
|
| п -нитрофенол
| —
| 5,2–7,0
|
| Фенолфталеин
| 9,7
| 8,3–10,0
|
Контрольные вопросы и задачи
1. Вычислите рН ацетатного буферного раствора, составленного из 500 мл раствора соли с молярной концентрацией эквивалента
0.1 моль/л и 100 мл раствора кислоты с молярной концентрацией эквивалента 0.5 моль/л, если рК (СН3СООН) = 4.75.
2. Вычислите рН буферного раствора, составленного из равных объёмов растворов слабого основания и его соли одинаковой концентрации, если константа диссоциации основания равна 7.2 ∙ 10-6.
3. Какими процессами объясняется незначительное изменение значения рН буферного раствора при добавлении к нему растворов: а) сильной кислоты, б) щёлочи?
4. Рассчитайте в каких объёмах надо слить раствор слабой кислоты с молярной концентрацией эквивалента 0.6 моль/л и раствор её соли с молярной концентрацией эквивалента 0.2 моль/л, чтобы получить 200 мл ацетатного буферного раствора с рН = 5.2, если рК(СН3СООН) = 4.75.
5. Вычислить, на сколько единиц изменится рН аммиачного буферного раствора, содержащего по 0.1 моль эквивалента каждого из компонентов, если к 1 л его прибавить 0.05 моль эквивалента NаОН рК(NН 4ОН) = 4.74.
6. Рассчитайте, в каком соотношении должны находиться компоненты бикарбонатной буферной системы крови, если рК(Н2СО3) = 6.14.
7. К 20 мл фосфатного буферного раствора добавили 2 мл раствора НСl с молярной концентрацией эквивалента 0.02 моль/л. При этом рН изменился от 7.4 до 7.0. Рассчитайте буферную ёмкость буферной системы по кислоте.
8. Определите потенциальную кислотность буферного раствора с рН = 2.0, если на титрование 10 мл его потребовалось 8 мл раствора NаОН с молярной концентрацией эквивалента 0.1 моль/л.
9. Какие из ниже перечисленных систем обладают буферным действием: а) НСООН + НСООNа; б) NаОН + НNО3;
в) НNО3 + КNО3; г) НСl + НNО3; д) СН3СООН + СН3СООNа; е) NаНСО3 + НСl.
10. Какова биологическая роль буферных растворов в организме человека?
11. Какова роль гидрокарбонатного буферного раствора при поддержании постоянства рН крови, нарушаемого процессами дыхания?
Занятие 18. КОЛОРИМЕТРИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ рН
Цель занятия:
Изучить принципы колориметрического метода определения концентраций Н+-ионов в растворе.
Содержание занятия:
1. Обсуждение теоретических вопросов по теме.
2. Выполнение лабораторных работ, обсуждение их результатов, оформление отчёта.
Вопросы, предлагаемые для обсуждения на занятии:
1. Индикаторы. Механизм действия индикатора.
2. Точка перехода и зона перемены окраски индикатора. Универсальный индикатор.
3. Закон Ламберта–Бера. Принципы колориметрического метода определения концентрации растворов.
4. Буферный и безбуферный методы определения рН раствора.
Лабораторная работа 1. Колориметрический буферный метод определения рН.
а) Ориентировочное определение рН исследуемой жидкости по универсальному индикатору. Выбор буферной системы и индикаторов.
В чистую фарфоровую чешку наливают небольшое количество исследуемого раствора и с помощью универсальной индикаторной бумажки, пользуясь цветной шкалой, определяют приблизительное значение рН. Затем, пользуясь таблицей 1, выбирают индикатор и буферную смесь для приготовления растворов–эталонов и после этого занимают соответствующее рабочее место. Индикатор выбирают так, чтобы в зону перемены окраски его попадала ориентировочно найденная величина рН раствора.
Таблица 1. Значения рН буферных смесей – эталонов
| Индикатор
(зона перехода)
| Название
буферных систем
| Объем, мл
| рН
|
| соли
| кислоты
|
| Тимоловый синий
(1,1–2,8)
| Цитратная
(лимонная)
| 1,0
2,5
| 4,0
2,5
| 2,3
2,9
|
| Метилоранж
(3,0–4,4)
| 3,5
4,0
4,5
| 1,5
1,0
0,5
| 3,3
3,5
3,9
|
| Метиловый красный
(4,2–6,3)
| Ацетатная
| 1,0
2,5
3,5
4,0
4,5
| 4,0
2,5
1,5
1,0
0,5
| 4,1
4,7
5,1
5,3
5,7
|
| Бромтимоловый синий
(6,0–7,6) или
нейтральрот (6,5 – 8,0)
| Фосфатная
| 1,0
2,5
3,5
4,0
4,5
| 4,0
2,5
1,5
1,0
0,5
| 6,2
6,8
7,2
7,4
7,7
|
б) Приготовление эталонов и определение рН исследуемой жидкости.
В чистых пронумерованных пробирках из бесцветного стекла и одинакового диаметра, пользуясь таблицей 1, готовят пять соответствующих буферных растворов-эталонов, затем в каждую из пробирок добавляют по 3 капли выбранного индикатора и растворы-эталоны перемешивают. В отдельную пробирку отмеривают пипеткой 5 мл исследуемого раствора, добавляют 3 капли того же индикатора и после перемешивания сравнивают окраску с окраской растворов–эталонов.
Примечание. При работе с цитратным буфером исследуемый раствор отмеривают в две пробирки и добавляют в них различные индикаторы (см. табл. 1), чтобы затем сравнивать окраску в каждой из них с соответствующими эталонами. При сравнивании окраски растворов следует пробирки поставить на белый лист бумаги и смотреть на растворы сверху. Значение рН исследуемой жидкости равно значению рН раствора–эталона, если их окраска совпадает.
Работу оформите в виде таблицы 2.
Таблица 2
| Ориентировочная величина рН по универсальному индикатору
| Выбранный
индикатор
(указать зону
перехода)
| Буферные растворы – эталоны
| Точная величина
рН
|
| Название и формулы компонентов
| Состав (мл)
|
| соль
| кис-лота
| рН
|
|
|
|
|
|
|
|
|
Лабораторная работа 2. Определение рН раствора при помощи фотоколориметра КФК- 2МП.
а) Подготовка фотоколориметра КФК–2МП к работе в циклическом режиме.
Общий вид прибора:
|
|  7 6 4
1 – колориметр
2 – микропроцессорная система
3 – фотоприемник
4 – ручка смены кювет
5 – крышка кюветного отделения
6 – светофильтры
7 – сигнальная лампочка
8 – сеть
9 – пуск 7 6 4
1 – колориметр
2 – микропроцессорная система
3 – фотоприемник
4 – ручка смены кювет
5 – крышка кюветного отделения
6 – светофильтры
7 – сигнальная лампочка
8 – сеть
9 – пуск
|
|
1. Присоедините прибор к сети, откройте крышку кюветного отделения (5) и на задней панели прибора слева включите тумблер «сеть» (8), при этом должна загореться сигнальная лампа (7) (на цифровом табло могут появиться различные символы).
2. Нажмите клавишу «пуск» - на цифровом табло появляется мигающая запятая и горит индикатор «р». Если запятая не появилась, повторно нажмите клавишу «пуск».
3. Выдержите колориметр во включенном состоянии в течение 15 мин. при открытой крышке кюветного отделения.
4. Ручкой (6) установите светофильтр 440 нм, а ручкой (3) — фотоприемник 315–540. Выдержите прибор с закрытой крышкой 5 мин. Если положение ручек (3) и (б) уже было установлено, как указано, операции п.4 можно опустить.
5. Измерение и учет темнового тока «n0». Крышку кюветного отделения закройте и через несколько секунд откройте опять. Через 5 с. нажмите клавишу «Ш (0)». На цифровом табло справа от мигающей запятой высвечивается значение n0, а слева – символ «0». Значение n0 необходимо для внутренней калибровки прибора, для расчетов вам оно не потребуется. Однако, если оно выходит за пределы промежутка от 0.001 до 1.000, следует пригласить преподавателя. После выполнения пунктов 1–5 прибор готов к работе. Крышку кюветного отделения следует оставить открытой.
б) Выбор индикатора и подготовка растворов для фотоэлектроколориметрирования.
1. В чистый фарфоровый тигелек пипеткой (на 10 мл) отмеряют 1 мл исследуемого раствора, добавляют 1 капли раствора универсального индикатора и, сравнивая получившуюся окраску раствора с цветной шкалой для универсального индикатора (приколота к полке), находят примерную величину рН раствора с точностью до 0.5 и записывают в протокол (таблицу).
2. Выбирают один из одноцветных индикаторов ряда нитрофенола (см. таблицу 3). Индикатор выбирают так, чтобы ориентировочно найденная по универсальному индикатору величина рН оказалась в пределах (примерно в средней части) зоны перехода окраски индикатора.
Таблица 3
| № п/п
| Индикатор
| Точка перехода окраски индикатора рК
| Зона перехода окраски индикатора
|
| I.
| a-динитрофенол
| 4,05
| 2,8–4,5
|
| 2.
| γ-динитрофенол
| 5,15
| 4,0–5,5
|
| 3.
| п- нитрофенол
| 6,18
| 5,2–7,0
|
| 4.
| т -нитрофенол
| 8,31
| 6,7–8,4
|
3. В пробирку № 1 с помощью бюретки отмерьте 6 мл раствора карбоната натрия, а в пробирку № 2 — 6 мл исследуемого раствора (пипеткой). В обе пробирки добавляют пипеткой (на 1 мл) точно по 1 мл раствора выбранного индикатора. Содержимое пробирок хорошо перемешивают стеклянными палочками.
4. Одну из кювет прибора (с меткой "В" на дне кюветы) заполните растворителем (дист. водой), другую (с меткой "И") — щелочным раствором выбранного индикатора (проба № 1), а третью (с меткой "З") — исследуемым раствором (проба № 2),предварительно сполоснув эти кюветы небольшим объемом соответствующих растворов.
Примечание: Жидкости в кюветы наливают до метки по нижнему мениску. Рабочие поверхности кювет тщательно протирают сухой чистой марлей. При работе с кюветами нельзя касаться рабочих поверхностей кювет.
б) Измерение оптической плотности растворов в циклическом режиме (с периодом 5 с).
В дальнее гнездо кюветного отделения установите кювету с растворителем (дист. водой), а в ближнее — кювету со щелочным раствором выбранного индикатора (толщина поглощающего слоя кювет 1 см).
Закройте крышку кюветного отделения. Ручку (4) установите в положение "1" (в световой пучок вводится кювета с растворителем).
Нажмите клавишу "Пуск" и "Ц/Р". Вы выбрали циклический режим работы, о чем свидетельствует загорание индикатора "Ц" справа от табло. Прибор готов к выполнению измерений в цикле с интервалом в 5 с.
Нажмите клавишу "К(1)". На цифровом табло слева от мигающей запятой высвечивается символ "1". Это означает, что прибор измерил оптическую плотность раствора сравнения (дистиллированная вода).
Поверните ручку (4) из положения "1" в положение "2" (в световой пучок введена кювета с раствором индикатора).
Нажмите клавишу "Д(5)". На цифровом табло слева от мигающей запятой появляется символ "5", а справа — с интервалом 5 с. высвечивается значение измеренной величины оптической плотности раствора индикатора Динд.. Данные измерений заносят в таблицу 4.
Откройте крышку кюветного отделения. Вместо кюветы с раствором индикатора поставьте кювету с исследуемым раствором (из пробирки № 2) и произведите замеры оптической плотности Диссл., повторив операции по пунктам раздела б). Пригласите преподавателя для проверки результатов работы.
Окончание работы.
1. Отключить тумблер "сеть" на задней панели прибора, выключить прибор из сети.
2. Вымыть кюветы дистиллированной водой и протереть марлей досуха (снаружи) рабочие поверхности кювет.
3. Вымыть пробирки, тигелек и пипетки. Рабочее.место привести в порядок.
Оформление отчета по работе:
1. По формуле α =  рассчитать степень диссоциации индикатора в исследуемом растворе
рассчитать степень диссоциации индикатора в исследуемом растворе
2. По уравнению рН = рК + lg 
 рассчитайте рН исследуемого раствора, где рК — точка перехода окраски индикатора (см. табл. 3).
рассчитайте рН исследуемого раствора, где рК — точка перехода окраски индикатора (см. табл. 3).
3. Данные занесите в таблицу 4:
Таблица 4
| 1.
| Ориентировочное значение рН раствора
|
|
|
| Выбранный индикатор (название, зона перезода окраски, рК)
|
|
| 3.
| Оптическая плотность раствора индикатора Динд
| 1.
2.
3.
4.
5.
────
ср.=
|
| 4.
| Оптическая плотность исследуемого раствора Диссл
| 1.
2.
3.
4.
5.
────
ср.=
|
| 5.
| Степень диссоциации индикатора в растворе α
|
|
| 6.
| рН исследуемого раствора
|
|
Контрольные вопросы и задачи
1. рН Исследуемого раствора, определенного по шкале универсального индикатора, находится в пределах 4—5. Какой индикатор и какую буферную смесь для приготовления растворов — эталонов будете использовать для определения точного значения рН раствора? (см. табл.3).
2. рН Исследуемого раствора, определенного по шкале универсального индикатора, равен 3. Для точного определения рН раствора выбрали индикатор тимоловый синий и цитратную буферную смесь для приготовления растворов—эталонов. Почему окраска раствора не совпала с окраской растворов—эталонов?
3. Почему в качестве стандартных растворов с известным рН удобно брать буферные смеси?
4. рН раствора равен 8.41. Чему равна концентрация ионов водорода?
5. Константа диссоциации слабого однокислотного основания МОН равна Косн = 1 ∙ 10-6. Вычислите концентрацию гидроксид-ионов в растворе этого основания, концентрация которого С = 0.01 моль/л.
6. Смешивают равные объемы растворов серной кислоты с концентрацией С(H2SO4) = 0.2 моль/л и КОН с концентрацией С(КОН) = 0.6 моль/л. Вычислите рН полученного раствора.
7. В растворе слабой одноосновной кислоты с молярной концентрацией С = 10-2 моль/л концентрация ионов водорода составляет 1∙10-3 моль/л. Определите константу диссоциации кислоты.
8. Рассчитать соотношение кислоты и соли в буферной смеси, если готовится раствор объемом 5 мл и его рН = 5
(рКдис. к-ты = 4.73, молярная концентрация эквивалента кислоты и соли 0.2 моль/л).
9. Концентрация гидроксид-ионов в растворе составляет
6∙10-4 моль/л. Определить, будет ли активен в этом растворе пепсин, если зона его активности рН = 1.5–2.5.
10. рН мочи в норме колеблется от 6 до 7. Определить интервал концентраций гидроксид-ионов в этих областях рН.



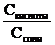 = Кд ∙
= Кд ∙ 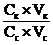
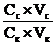
 = -(lg1,8 – 5) + 0,0872 =
= -(lg1,8 – 5) + 0,0872 =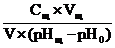 , моль/л; Вк =
, моль/л; Вк =  , моль/л
, моль/л , моль/л;
, моль/л; 7 6 4
1 – колориметр
2 – микропроцессорная система
3 – фотоприемник
4 – ручка смены кювет
5 – крышка кюветного отделения
6 – светофильтры
7 – сигнальная лампочка
8 – сеть
9 – пуск
7 6 4
1 – колориметр
2 – микропроцессорная система
3 – фотоприемник
4 – ручка смены кювет
5 – крышка кюветного отделения
6 – светофильтры
7 – сигнальная лампочка
8 – сеть
9 – пуск
 рассчитать степень диссоциации индикатора в исследуемом растворе
рассчитать степень диссоциации индикатора в исследуемом растворе
 рассчитайте рН исследуемого раствора, где рК — точка перехода окраски индикатора (см. табл. 3).
рассчитайте рН исследуемого раствора, где рК — точка перехода окраски индикатора (см. табл. 3).


