Среди различных химических веществ особую группу составляют кремнийорганийческие соединения. Их отчасти можно рассматривать как продукты замещения водорода в силанах на органические радикалы или на другие группы атомов, содержащие в своем составе углерод. В молекуле кремнииорганических соединений кроме атомов различных элементов обязательно должны быть атомы кремния и атомы углерода, связанные между собой. непосредственно или через.атомы кислорода, серы и азота.
Особенностью молекулярного строения кремнийорганических соединений является и то, что в них атомы кремния, связанные между собой непосредственно, образуют либо открытые цепи, на.т пример в этилметилтетрахлортрисилане
 снз
снз
 С2H5-SiH2 —Si —SlCI3
С2H5-SiH2 —Si —SlCI3
CI
либо замкнутые кольца, как в октафенилциклотетрасилане

 (C6H5)2Si- Si(C6H5)2
(C6H5)2Si- Si(C6H5)2
(C6H5)3Si - Si(C6H5)2



 Кроме этого, атомы кремния могут быть связаны между собой как в цепочки, так и в кольца через атомы кислорода при помощи так называемой силоксановои связи — Si — O-— Si—, например в гексаметилдисилоксане
Кроме этого, атомы кремния могут быть связаны между собой как в цепочки, так и в кольца через атомы кислорода при помощи так называемой силоксановои связи — Si — O-— Si—, например в гексаметилдисилоксане
Химическая связь между атомами кремния и атомами угле-
рода может быть непосредственной, как в приведенных примерах,
или может также осуществляться через кислород, как в диметил-
бутоксисилане (СНз)2Si(OC4H9)2, через азот, серу и атомы дру
гих элементов.
Различают низко- и высокомолекулярные кремнийорганиче-ские соединения. Первые обычно рассматриваются как производные силанов, в которых один или несколько атомов водорода замещены органическими радикалами, например диэтилсилан (C2H5)2SiH2, триметилфенилсилaн (CH3)3SiC6H5, тетрафеноксиси-лан (C6H5O)4Si и т. д. Высокомолекулярные (полимерные) крем-нийорганические соединения рассматриваются как продукты замещения атомов водорода и целых звеньев — Si — Si — Si — или
— Si — О — Si — на органические радикалы.
Получают кремнийорганические соединения преимущественно
из галогенидных соединений кремния путем полного или частичного замещения в них атомов галогена на соответствующие органические радикалы или их группы. Например,
H3SiCl + Zn(CH3)3 = CH3SiH3 + CH3ZnCI или
SiCI4 + 4C2H5OH = Si(OC3H5)4 + 4HC1
SiC14 + 4CH3MgCI = Si(CH3)4 + 4MgC33
по Вюрцу методом конденсации в присутствии металлического
натрия
SiCl4 + 4C6H5C1 +8Na = Si(C6H5)4 + 8NaCI
2[(С2Н5)3 SiBr] + 2Na = (C2H5)3Si - Si(C2H5)3 + 2NaBr
и некоторыми другими способами.
Промышленное производство исходных кремнийорганических соединений осуществляется преимущественно двумя методами: синтезом Гриньяра и прямым синтезом. Промышленный синтез Гриньяра может быть представлен по фазам в такой последовательности:
Si + 2Cl3 = SiC14
2CH3C1 + 2Mg = 2CH3MgCI
 2CH3MgCl + SiCl4 = (CH3)2SiCl2 + 2MgCl3
2CH3MgCl + SiCl4 = (CH3)2SiCl2 + 2MgCl3
2CH3C1 + 2Mg + Si + 2C12 = (CH3)2SiCl2 + 2MgCI2
Прямым синтезом называют реакцию образования кремнийорганического соединения из элементарного кремния и галогенопроизводного соответствующего углеводорода в присутствии катализатора (медь, серебро и др.), которые способны образовывать нестойкие металлорганические соединения. Реакция протекает в накаленной контактной массе, когда через нее пропускают соответствующие галогенопроизводные углеводородов. Контактная масса представляет собой порошок или гранулы, полученные измельчением спекшейся при 700—1060° С смеси, состоящей из элементарного кремния и катализатора.
В основной массе кремнийорганические соединения представляют собой подвижные и вязкие жидкости, пастообразные массы и замазки, смолы, лаки, и каучуки. Их используют для получения очень тонкодисперсного кремнезема.
Многие кремнийорганические соединения по сравнению с органическими обладают более высокой термостойкостью, гидрофобностью, антикоррозийностью, долговечностью, повышенной механической прочностью, более высокими электроизоляционными свойствами, повышенной смачиваемостью и адгезией по отношению к различным материалам и т. д. Это дает возможность широко применять и использовать кремнийорганические соединения в качестве гидрофобных, антикоррозийных, электроизоляционных, пропиточных масс, и замазок. Соответствующая прочность и термостойкость этих веществ, а также способность их уменьшать коэффициент трения дали возможность использовать их в качестве сухих смазок трущихся частей в различных механизмах. Благодаря антисептическим свойствам, многие кремнийорганические соединения широко применяются в медицине.
Под действием атмосферных реагентов поверхность оптических стекол в приборах часто портится, шлифованная поверхность ее становится матовой, шероховатой и покрывается трещинами. Обработка такой поверхности гидрофобными кремнийорга-ническими соединениями в виде 0,020/о-ного бензольного раствора октадецилтрихлорсилана: или октадецилтриэтоксисилана и полимера (C18H37SiO1,5)х создает на поверхности стекла тончайшую водоотталкивающую пленку. Гидрофобизация * стекла в аналитической химии упрощает работу с химической посудой и аппаратурой и способствует более высокой точности определений. Соответствующая обработка стекол самолетов, автомобилей и судов в значительной степени снижает их обледенение, а очков в противогазах предотвращает их запотевание. Удельное поверхностное электрическое сопротивление гидрофобизированного стекла возрастает и сохраняется даже при 100%-ной относительной влажности, в то время как поверхностное электрическое сопротивление негидрофобизированного стекла понижается в тысячи раз. Силоксановый слой на поверхности гидрофобизированного стекла обусловливает более высокую адгезию по отношению к органическим клеям при склеивании стекла со стеклом. Семи- и восьмикратная обработка поверхности стекол раствором четыреххлористого кремния в четыреххлористом углероде с последующей поли- ровной обработанной поверхности снижает отражательную способность ее до 1—2%, что имеет существенное значение для оптических приборов.
Гидрофобизация строительных материалов — цементного камня, бетона, строительных растворов, штукатурок, известняков, песчаников, кирпича и других видов керамики — производится для защиты их от сырости 3—5%-ным раствором метилтрихлорсилана, этилтрихлорсилана, диметилдихлорсилана или термореактивными силиконовыми лаками. Эти вещества проникают глубоко в поры материала, покрьвают поверхность их тонким невидимым химически стойким слоем, не изменяя ни внешнего вида, ни воздухопроницаемости строительного материала и существенным образом улучшая термоизоляционные свойства их.
Гидрофобизированная бумага сохраняет прочность при повышенной влажности, не пропускает воду, сохраняет написанный текст во влажных условиях, повышает долговечность документов, чертежей и плакатов.
Гидрофобизированный кремнийорганическими соединениями текстиль водой не смачивается не пропускает ее, а по внешнему виду он ничем не отличается от обычного необработанного текстиля. Водопоглощение гидрофобизированного текстиля снижается примерно в 20 раз. В качестве гидрофобизаторов используются эмульсии метилгидросилоксанов или смеси диметилсилоксанов с метилгидросилоксанами. Гидрофобизированная кожа лучше переносит смачивание водой, становится более долговечной, не гниет и не плесневеет. Для этого используют растворы и водные эмульсии метилгидросилоксана, некоторых легкоподвижных силиконовых лаков и растворы аминосиланов.
Кремнийорганические соединения, широко используются для смазки трущихся стальных частей различных механизмов и стеклянных волокон при изготовлении пряжи и тканей. В производстве люминесцентных, фосфоресцирующих и флуоресцирующих материалов, атакже для изготовления ряда изделий из спекшегося кварца требуется кремнезем в чрезвычайно тонкодисперсном состояний до 0,1 мкм. Такой продукт легче и дешевле получить сжиганием эфиров ортокремниевой кислоты или четыреххлористого кремния в водородном пламени, что и используется в технике.
Силиконовые соединения во многих случаях используются в качестве теплоносителей при температурах до 350° С. Они воспламеняются с большим трудом, горения не поддерживают, материал трубопроводных систем и изолирующих прокладок не корродируют. Гидролизованные и частично сконденсированные эфиры ортокремниевой кислоты обладают хорошими пеногасящими свойствами, поэтому используются в противопожарном деле.
Кремнийорганические эфиры при соответствующих условиях конденсируются в масла и смолы. Смолы отвердевают при 150— 200° С, обладают высокой адгезией, хорошими изоляционными свойствами, гладкой поверхностью и хорошей стойкостью по отношению к воде и кислотам. Эфиры ортркремниевой кислоты при- меняются в качестве пластификаторов в лаковом производстве, попользуются как смазки для приборов, работающих при высоких давлениях, и в ряде производств являются диспергаторами. При добавлении эфиров ортокремниевой кислоты к твердым полимерам увеличивается их водостойкость, твердость, адгезия к стеклу, керамике, металлам и дереву, долговечность и гладкость поверхности, ускоряется отверждение их, понижается горючесть и плавкость органического полимера, повышается термическая стойкость, а также устойчивость по отношению к щелочам, кислотам и органическим растворителям.
Кремнийорганические соединения широко используются при
литье изделий методом выплавляемых моделей, а также для обра-
зования на поверхности металла (стали) защитного слоя, предо-
храняющего ее от коррозии. Эти соединения применяются в ме-
дицине как для поверхностной обработки различных материалов
и лабораторной посуды, так и в лечебном деле.
СИЛИКАТЫ И АЛЮМОСИЛИКАТЫ
По общепринятой в химии терминологии силикатами следует
называть соли кремниевых кислот. Однако, поскольку кремниевые
кислоты в чистом виде не выделены, силикатами называют хими-
ческие соединения, в которых кремний присутствует в составе
иона [SiO4]4- или производных последнего.
Химический состав силикатов принято выражать формулами оксидов тех элементов, которые входят в рассматриваемое химическое вещество, например, формулу ортосиликата натрия Na4SiO4 записывают 2Na2O • SiO2, вместо CaSi03 пишут CaO . SiO2, вместо H4Al2Si2O9—Al203 . 2SiO2 . 2H2O и т. д. В основе пространственного строения кристаллических силикатов находится четырехзарядный ион [Si04]4- (см. рис. 1) и его различные сочетания. В зависимости от этого силикаты классифицируются на следующие группы:
1. Силикаты с изолированными, т. е. не связанными между собой непосредственно тетраэдрами [Si04]4-. В кристаллической структуре таких силикатов связь между ионами [SiO4]4- осуществляется ионами тех металлов, какие входят в состав соответствующего соединения. Примером такого кристаллического строения силикатов служит минерал форстерит 2MgO . Si02 (рис.2). Ионы [SiO4]4- изображены треугольниками, в вершинах которых находятся ионы кислорода (рис. 2), а в центре треугольника — ион кремния. Этот ион виден только тогда, когда весь тетраэдр [SiO4]4- повернут к нам кремнием и от нас кислородом, т. е. когда четвертая кислородная вершина тетраэдра [SiO4]4- находится по ту сторону от нас и от атома кремния. Атомы магния соединены с соседними тетраэдрами [SiO4]4- через ближайшие к нему ионы кислорода. Такое строение присуще ортосиликатам магния, кальция, железа (II), никеля, кобальта, марганца, цинка и других ме-таллов. 2. Силикаты с изолированными группами — [Si207]6-, [Si309]6-, [Si4О12]8- и [Si6O18]12- — кремнекислородных тетраэдров получаются в том случае, когда два, три или больше простейших тетраэдра-ионов [SiO4]4- соединяются между собой общими ионами кислорода (рис
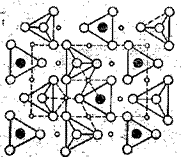
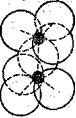

Рис. 2. Структура форстерита: Рис. 3. Условное обозначение иона [Si2O7]6-
ляется остальная часть воды, представленная гидроксильными группами. Этот процесс сопровождается разрушением кристаллической структуры каламина.
Представителем силикатов, состоящих из изолированных кольцевых радикалов [Si3O9]6-, [Si6018]12- и др., соединенных между собой и металлическими катионами, может служить минерал берилл Be3Ala[Si6018].
 3. Силикаты с непрерывными цепочечными радикалами [Si206l6- и ленточными радикалами [Si4O11]6-, а также радикалом [Si6017]10- представляют собой следующую группу силикатов. По цепочечной структуре кремнекислородные тетраэдры соединяются между собой в бесконечные цепочки при помощи общих атомов кислорода, принадлежащих одновременно двум смежным тетраэдрам (рис.6). При этом у каждого кремнекислородного тетраэдра [SiO4]4- два атома свободны, два других атома общие с соседними кремнекислородными тетраэдрами. Цепочечный радикал [Sl206]4- находится между
3. Силикаты с непрерывными цепочечными радикалами [Si206l6- и ленточными радикалами [Si4O11]6-, а также радикалом [Si6017]10- представляют собой следующую группу силикатов. По цепочечной структуре кремнекислородные тетраэдры соединяются между собой в бесконечные цепочки при помощи общих атомов кислорода, принадлежащих одновременно двум смежным тетраэдрам (рис.6). При этом у каждого кремнекислородного тетраэдра [SiO4]4- два атома свободны, два других атома общие с соседними кремнекислородными тетраэдрами. Цепочечный радикал [Sl206]4- находится между
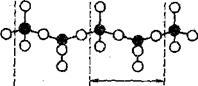
Рис. 6. Условное обозначение. Условное обозначение строения ленточной структуры радикала [S4O11]6-
строения, цепочечной структуры
радикала [Si2O6]4-
штриховыми линиями (рис. 6). Примером силикатов с одинарными анионными цепочками служат минералы — диопсид CaMg[Si2O6], геденбергит CaFe[Si2Oe], жадеит NaAI[Si2O6] и др,
4. Если две цепочки расположены параллельно друг другу в одной плоскости так, что одна из них представляет собой зеркальное отражение второй и обе они соединены между собой общими третьими в тетраэдрах атомами кислорода, то получается ленточная структура, состоящая из двух спаренных между собой цепочек кремнекислородных тетраэдров. Радикал такой структуры (рис. 7) содержит четыре атома кремния и одиннадцать атомов кислорода. Формула этого радикала записывается в виде [Si4O11]6-. Из природных силикатов такой структурой обладают, амфиболы, например антофиллит Mg7[Si4O11], термолит Ca2Mg5[Si4O11]2[OH]2 и др.
Подобная структура присуща силикатам с анионными лентами [Si6O17]10-. К минералам с такой структурой относится волластонит Ca6[Si6O17]О.
5. Более сложной структурой считают листовую, состоящую теоретически из сочетания бесконечно большого количества тетраэдров, соединенных друг с другом тремя общими атомами кислорода (рис. 8). Такое сочетание кремнекислородных тетраэдров
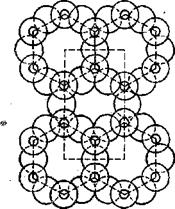
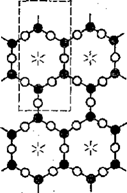
Рис. 8. Листовая структура радикала [S4O10]4-
образует плоский лист. В этой структуре четвертые атомы кислорода каждого из кремнекислородных тетраэдров валентны и могут располагаться либо по одну сторону листа, либо поочередно по обе стороны его. В первом случае они образуют химически активный слой всего листа, во втором два активных слоя, при помощи которых лист в целом может присоединять к себе различные катионы. Химическая формула силикатов листовой структуры выражается радикалом [Si2O5]2-∞. В природе к листовой структуре силикатов относят слюдообразиые минералы. Слоистое строение этих минералов обусловливает способность расщепления их на тонкие листочки. К этой группе минералов относится тальк Mg3tSi4O1o][OH]2 и пирофиллит Al2[Si4O10][OH]2. В слюдах один из атомов кремния в радикале из кремнекислородных тетраэдров замещается атомом А1, в результате радикал [Si4O10]4- записывается в таком виде: [Si3AlO10]5-. К таким минералам относятся флогопит KMg3[Si3A1010] [F, ОН]2 биотит K(Mg, Fe)3[Si3A1010] •[ОН, F]2! мусковит KAl2[Si3AlO10][OH]2, лепидолит KLi1,5A11,5 •[Si3AlO10][FeOH]2, гидрослюды — вермикулит и глауконит, минералы группы серпентина-калинита, среди которой выделяют-
ся минералы серпентин Mg6[Si4O10][OH]8, каолинит Al4[Si4O10] . [ОН]8 и его разновидности, диккит Al4[Si4O10][OHl8 и накрит
Al4[Si4O10][OH]8 и др.
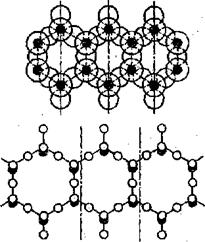
6. Если силикаты листовой структуры с валентными атомами кислорода, поочередно направленными в противоположные от листа стороны, наложить на другие такие же листы так, чтобы атомы кислорода одного листа вошли в соприкосновение с такими же атомами кислорода второго и т. д. листа, то каждая такая пара валентных атомов кислорода обоих листов может быть заменена одними общими для обоих листов атомами кислорода. В результате этого получается слоистая структура (рис. 9), 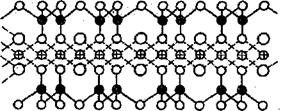
Рис. 9. Слоистаяструктура:
 О - ОН; О - О; Ø - Mg; • - Si
О - ОН; О - О; Ø - Mg; • - Si
в которой каждый отдельный кремнекислородный тетраэдр [SiO4]4- непосредственно связан с четырьмя такими же смежными тетраэдрами при помощи всех четырех атомов кислорода. Эта структура валентных атомов кислорода не имеет. Формула такой структуры записывается в виде [SiO2] 0 или / n [SiO2]°.
В перечисленных структурах силикатов кремнекислородные тетраэдры, обладающие четырьмя отрицательными зарядами, выступают в виде отрицательно заряженных ионов, способных присоединять к себе те или иные катионы, в результате чего образуются различного состава химические соединения, называемые силикатами. Многие силикаты наряду с кремнекислородными анионами содержат и другие анионы: 02-, [ОН]-, F-, Cl-, [СО2]2- и т.д. В результате получаются химические соединения, содержащие два или несколько анионов, соединенных при помощи тех или иных общих катионов. Например, андалузит и дистен, состав которых выражается формулой Al2[Si4O1o]2O, состоит из двух атомов алюминия (катионы), соединенных с двумя анионами [Si4O1o]4- и О2-. Это подтверждается структурой каолинита Al4[Si4O1o][OH]8, пирофиллита, Al2[Si4O1o][OH]2 и других минералов.
Если в составе силикатов присутствуют гидроксильные группы, их называют гидросиликатами соответствующих металлов. С этой точки зрения каолинит и пирофиллит рассматриваются как гидросиликаты алюминия.
Во время термической обработки многие силикаты, содержащие в своем составе элементы воды, выделяют ее при соответствующих температурах. Элементы воды в силикатах могут быть в четырех видах: структурной (конституционной), кристаллизациионной, цеолитной и в виде гигроскопической (адсорбционной влаги. Количество гигроскопической влаги не постоянно и изменяется в зависимости от влажности окружающей среды.
Цеолитная вода находится внутри (в его каналах) силикатов каркасного строения. Количество ее не постоянно. При нагревании она удаляется, не разрушая строения силикатов. Во влажной среде такой силикат опять поглощает цеолитную воду. Кроме воды могут быть поглощены аммиак, этиловый спирт, сероводород и другие вещества.
Кристаллизационная вода входит в молекулярном виде в структуру кристалла. При нагревании она постепенно удаляется, образуя сначала промежуточные кристаллогидраты, а затем полностью дегидратированное вещество. Это приводит к разрушению кристалла. Кристаллизационная вода записывается в кристаллохимических формулах справа в молекулярном виде, например минерал галлуазит Al4[Si4O10][OH]8 . 4H20 содержит четыре молекулы кристаллизационной воды.
При накаливании минералов, содержащих кристаллизацион-
ную и конституционную воду, вначале удаляется кристаллизаци-
онная, а затем при более высоких температурах гидроксильные
группы разлагаются и за счет их разложения выделяется консти-
туционная вода. При этом минерал распадается на смесь свобод-
ных оксидов и более простых силикатов. В кристаллохимических
формулах силикатов конституционная вода записывается справа
в виде гидроксильных групп. Например, в галлуазите [ОН]-8 обо-
значает конституционную воду.
Многие силикаты способны образовывать изоморфные смеси и твердые растворы за счет замены одних катионов другими. Катионы, способные замещать друг друга, заключаются в круглые скобки в убывающем порядке и записываются перед анионами. Так, в минерале нонтроните (Fe, Al)2[Si4O10][OH]2 . n H2O может быть одновременно некоторое количество катионов Fe3+ и А13+; анион [Si401o]4-, конституционная вода [ОН]-2 и кристаллизационная nH2O. При этом количественное соотношение между Fе3+ и- А13+ в различных видах минерала различно и может колебаться от Fe2[Si4O10][OH]2- n H2O до А12[514О10][ОН]2. гН2О.
СИЛИКАТЫ ЩЕЛОЧНЫХ МЕТАЛЛОВ
Большое промышленное значение имеют силикаты щелочных и щелочноземельных металлов, а также некоторые силикаты марганца, железа, титана, алюминия, меди, никеля, кобальта, свинца, цинка и некоторых других элементов. Из силикатов щелочных металлов рассмотрим силикаты лития, натрия и калия.
Из силикатов лития известны метасиликат Li2О .SiO2, ортосиликат 2Li2О •2 SiO2 и бисиликат Li2O . 2Si02. Искусственно получают их, расплавляя стехиометрически составленную смесь карбонатов лития с диоксидом кремния. Из природных силикатов лития практическое значение имеют минерал сподумен LiAl[Si2O6], литиевые слюды: лепидолит КLi 1,5Al 1,5[Si3AIO1o][F, OH]2 и цинвальдит KLiFeAl[Si3AlO10][F, OH]2, которые используются для получения различных химических препаратов лития, употребляемых в стеклоделии, медицине, пиротехнике, фотографии, рентгенографии, при изготовлении щелочных аккумуляторов, в синтезе органических соединений и т. д.
Из силикатов натрия наиболее исследованы метасиликат Na2O . SiO2, бисиликат NaaO . 2SiО2, ортосиликат 2Na2О . 2SiO2 и трехнатриевый бисиликат 3Na2O . 2Si02. Все они получаются сплавлением смесей едкого натра или натриевой соды с тонкоизмельченным кремнеземом, взятых в соответствующих количественных соотношениях. При медленном охлаждении расплава из него выкристаллизовываются силикаты натрия. Метасиликат натрия кристаллизуется в виде игольчатых кристаллов, плавящихся при 1089° С, двусиликат в виде пластинок ромбической системы, ортосиликат плавится при 1118° С и существует в виде двух кристаллических модификаций аи Вс температурой взаимного превращения 960° С и трехнатриевый бисиликат существует в виде остроугольных пластинок от 402 до 1123° С.
Метасиликат натрия можно получить также растворением тонкоизмельченного кремнезема в водном растворе едкого натра. Выпаривая этот раствор, получают игольчатые кристаллы ромбической системы, плавящиеся при 1089° С и состоящие из метасиликата натрия. Метасиликат натрия в холодной воде малорастворим, в кипящей растворяется лучше. Раствор его частично гидролизуется и обладает щелочной реакцией. В спирте Na2O . SiO2 не растворяется, но минеральные и некоторые орга-нические кислоты разлагают его, выделяя кремнезем:
Na2SiO3 + 2НС1 = 2NaCl + H2O + SiO2
Эта реакция используется в аналитической химии для количественного определения кремнезема.
Выделению кремнезема из водных растворов силикатов натрия способствуют соли аммония, натрия, калия, кальция, магния и других элементов. Эта реакция может быть представлена в таком виде:
Na2SiO3 + 2NH4C1 = 2NaCl + 2NH3 + H2O + SiO2
При выпаривании водных растворов силикатов натрия образуются кристаллогидраты с различным количеством кристаллизационной воды. Известны кристаллогидраты силиката натрия, содержащие на одну молекулу метасиликата 5, 6, 7, 8 и 9 молекул воды, т. е. Na2Si03 . 5H20, Na2Si03 . 6H2O и т. д. Они растворяются в воде и не растворяются в спирте.
Из калиевых силикатов изучены метасиликат калия K2O . SiO2 или K2SiO3, ортосиликат калия 2К2О . SiO2, или K4SiO4, бисиликат калия K2O . 2SiO2 или К2Si2О3 и тетрасиликат калия K2O . 4SiO2 или K2Si4O9. Химические свойства их подобны свойствам силикатов натрия, но температуры плавления их несколько ниже соответствующих температур плавления силикатов натрия и силикатов лития.
Силикаты калия получают подобно силикатам натрия сплавлением смеси, состоящей из эквивалентных количеств карбоната калия и мелкоизмельченного кварца, при температуре около 1100° С. Метасиликат калия при охлаждении расплава образует чрезвычайно гигроскопичные кристаллы ромбической системы, плавящиеся при 976° С, бисиликат калия кристаллизуется в таблетчатых кристаллах, плавящихся при 1045° С, тетрасиликат калия плавится при 770° С и ортосиликат калия — при 913° С, Водные растворы силикатов калия обладают щелочной реакцией.
РАСТВОРИМОЕ СТЕКЛО
Растворимое стекло — водный сиропообразный раствор силикатов калия или натрия. Состав натриевого растворимого стекла очень разнообразен. Обычно он характеризуется модулем М. Под модулем понимают количественное отношение кремнезема к оксиду натрия. Для нормальных растворимых стекол М=3, что соответствует трисиликату Na20 . 3SiO2. Однако этот модуль не всегда выдерживается и может изменяться. При выпаривании раствора стекла с модулем 3 наступает момент, когда выпадает в осадок SiO2, а в растворе остается бисиликат Na2О . 2SiO2, затем метасиликат Na2О . Si02.
Растворимое стекло широко используется в технике. Его добавляют в качестве наполнителя при изготовлении мыла; им пропитывают древесину, строительные камни, специальные ткани, перевязочный материал и т. д. Строительные материалы, пропитанные растворимым стеклом, приобретают большую прочность, огнестойкость, меньше выветриваются, повышается их устойчивость против разрушающего действия микроорганизмов.
Растворимое стекло используют в качестве клея и как прочный связывающий материал в химически стойких замазках и цементах. Наполняют такие замазки порошкообразными естественными и искусственными кремнийсодержащими веществами, например андезитом, молотым перекристаллизованным диабазом, фарфоровым боем, полевым шпатом и т. д. Из смеси наполнителя и растворимого стекла с небольшой добавкой Na2SiF6 изготовляют тестообразную пластическую массу, которой промазывают швы и склеивают отдельные строительные изделия.
Есть два способа получения калиевого и натриевого жидкого стекла — сухой и мокрый. По первому способу тонкоизмельченный кварц нагревают- с карбонатом щелочного металла. В качестве сырья, используют кварцевый песок, трепел, диатомит, соду или ее заменитель, сульфат натрия и угольный порошок. Накаливают сульфат натрия с кремнеземом в присутствии угля (восстановитель) до полного расплавления смеси:
2Na2SO4 + 2SiO2 + С = 2Na2SiO3 + 2SO2 + СО2
Для получения калиевого стекла вместо соды, или сульфата натрия употребляют карбонат калия. Стекло варят либо в огнеупорных горшках, либо в ванных печах при 1200—1300° С. Расплавленную стеклообразную массу гранулируют, а затем процесс ведут в автоклавах под давлением 0,3—0,8 МПа в течение 5—6ч для получения растворимого стекла.
Мокрый способ приготовления жидкого стекла основан на способности кремнезема переходить в раствор при кипячении его в водном растворе едкого натра или едкого кали:
Si02 + 2КОН = K2SiO3 + Н2О



 снз
снз С2H5-SiH2 —Si —SlCI3
С2H5-SiH2 —Si —SlCI3
 (C6H5)2Si- Si(C6H5)2
(C6H5)2Si- Si(C6H5)2
 2CH3MgCl + SiCl4 = (CH3)2SiCl2 + 2MgCl3
2CH3MgCl + SiCl4 = (CH3)2SiCl2 + 2MgCl3


 3. Силикаты с непрерывными цепочечными радикалами [Si206l6- и ленточными радикалами [Si4O11]6-, а также радикалом [Si6017]10- представляют собой следующую группу силикатов. По цепочечной структуре кремнекислородные тетраэдры соединяются между собой в бесконечные цепочки при помощи общих атомов кислорода, принадлежащих одновременно двум смежным тетраэдрам (рис.6). При этом у каждого кремнекислородного тетраэдра [SiO4]4- два атома свободны, два других атома общие с соседними кремнекислородными тетраэдрами. Цепочечный радикал [Sl206]4- находится между
3. Силикаты с непрерывными цепочечными радикалами [Si206l6- и ленточными радикалами [Si4O11]6-, а также радикалом [Si6017]10- представляют собой следующую группу силикатов. По цепочечной структуре кремнекислородные тетраэдры соединяются между собой в бесконечные цепочки при помощи общих атомов кислорода, принадлежащих одновременно двум смежным тетраэдрам (рис.6). При этом у каждого кремнекислородного тетраэдра [SiO4]4- два атома свободны, два других атома общие с соседними кремнекислородными тетраэдрами. Цепочечный радикал [Sl206]4- находится между



 О - ОН; О - О; Ø - Mg; • - Si
О - ОН; О - О; Ø - Mg; • - Si


