Выражение для средней энергии колебания с частотой ω дается выражением:

где  — постоянная Планка,
— постоянная Планка, 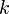 — постоянная Больцмана.
— постоянная Больцмана.
Количество стоячих волн в трёхмерном пространстве равно:

3. Квантовая теория фотоэффекта. Эффект Комптона.
Квантовая теория излучения. Фотоэффект
Фотоэффект - это явление, состоящее в возникновении электрического тока (фототока) через вакуумный зазор между двумя металлическими электродами, при освещении одного из них. Фотоэффект открыт Г. Герцем в 1877 г., а первое систематическое экспериментальное исследование проведено В.С. Столетовым в 1887 г.
Были установлены следующие закономерности: -Освещение металла светом приводит к испусканию электронов. -Cкорость выбитых электронов не зависит от интенсивности падающего света. -Фотоэффект возникает при освещении светом, частота которого больше некоторой характерной для каждого металла частоты кр, называемой пороговой частотой красной границей.
Эти экспериментальные данные полностью противоречат классическим представлениям. Согласно классической электродинамике увеличение освещенности сопровождается увеличением напряженности поля [(E)\vec] и, следовательно ростом силы eo [(E)\vec], действующей на каждый электрон, что должно приводить к увеличению его кинетической энергии. Напротив, увеличение частоты при постоянной освещенности должно было бы вести к уменьшению энергии электронов и к подавлению их выбивания из металла.
А. Эйнштейн (1905 г.), используя введенную им модель фотонов, сформулировал следующие предположения: -Поток света описывается моделью фотонов. -Поглощение металлом одного фотона может привести к вырыванию из металла только одного электрона. -Для удаления любого электрона из металла (на макроскопически большое расстояние) необходимо совершить работу, по величине не меньшую работы A, которая называется работой выхода.
Величина работы выхода зависит от вещества электрода, но не от свойств излучения, и определяется высотой потенциального барьера на границе "металл - вакуум".
| Используя закон сохранения энергии можем написать h ν = A +
| m v 2
| .
| | (5)
|
Это соотношение называется законом Эйнштейна для фотоэффекта.
| Пороговая частота определяется условием h νкр = A. Или νкр =
| c h
A
| ,
| |
где c - скорость света в вакууме.
Закон Эйнштейна для фотоэффекта был использован Р. Милликеном (1916 г.) для экспериментального определения величины постоянной Планка, независимого от законов теплового излучения. Он нашел, что h = 6,57·10-34Дж· c.
А. Комптон на опыте подтвердил квантовую теорию света. С точки зрения волновой теории световые волны должны рассеиваться на малых частицах без какого-либо изменения частоты излучения, что опытом не подтверждается.
При исследовании законов рассеяния рентгеновских лучей А. Комптон установил, что при прохождении рентгеновских лучей через вещество происходит увеличение длины волны рассеянного излучения по сравнению с длиной волны падающего излучения. Чем больше угол рассеяния, тем больше потери энергии, а следовательно, и уменьшение частоты (увеличение длины волны). Если считать, что пучок рентгеновских лучей состоит из фотонов, которые летят со скоростью света, то результаты опытов А. Комптона можно объяснить следующим образом.
Законы сохранения энергии и импульса для системы фотон - электрон: 

где m0c2- энергия неподвижного электрона; hv - энергия фотона до столкновения; hv' - энергия фотона после столкновения, p иp' - импульсы фотона до и после столкновения; mv - импульс электрона после столкновения с фотоном.
Решение системы уравнений для энергии и импульса с учетом того, что  дает формулу для измерения длины волны при рассеянии фотона на (неподвижных) электронах:
дает формулу для измерения длины волны при рассеянии фотона на (неподвижных) электронах:
 где
где  - так называемая комптоновская длина волны.
- так называемая комптоновская длина волны.
4. Давление света. Опыты, подтверждающие давление света. Корпускулярно-волновой дуализм излучения.
ДАВЛЕНИЕ СВЕТА - давление, оказываемое светом на отражающие и поглощающие тела, частицы, а также отдельные молекулы и атомы; одно из пондеромоторных действий света, связанное с передачей импульса эл--магн. поля веществу.
В 1873 г. Дж. Максвелл, исходя из представлений об электромагнитной природе света, пришел к выводу: свет должен оказывать давление на препятствие (благодаря действию силы Лоренца; на рисунке v - направление скорости электронов под действием электрической составляющей электромагнитной волны).

Квантовая теория света объясняет световое давление как результат передачи фотонами своего импульса атомам или молекулам вещества. Пусть на поверхность абсолютно черного тела площадью S перпендикулярно к ней ежесекундно падает N фотонов:  . Каждый фотон обладает импульсом
. Каждый фотон обладает импульсом  . Полный импульс, получаемый поверхностью тела, равен
. Полный импульс, получаемый поверхностью тела, равен  . Световое давление:
. Световое давление: 
При падении света на зеркальную поверхность удар фотона считают абсолютно упругим, поэтому изменение импульса и давление в 2 раза больше, чем при падении на черную поверхность (удар неупругий).

Это давление оказалось ~4.10-6 Па. Предсказание Дж. Максвеллом существования светового давления было экспериментально подтверждено П. Н. Лебедевым, который в 1900 г. измерил давление света на твердые тела, используя чувствительные крутильные весы. Теория и эксперимент совпали.
Опыты П. Н. Лебедева — экспериментальное доказательство факта: фотоны обладают импульсом


Корпускуля́рно-волново́й дуали́зм — принцип, согласно которому любой объект может проявлять как волновые, так и корпускулярные свойства. Был введён при разработке квантовой механики для интерпретации явлений, наблюдаемых в микромире, с точки зрения классических концепций. Дальнейшим развитием принципа корпускулярно-волнового дуализма стала концепция квантованных полей в квантовой теории поля.
Как классический пример, свет можно трактовать как поток корпускул (фотонов), которые во многих физических эффектах проявляют свойства электромагнитных волн. Свет демонстрирует свойства волны в явлениях дифракции и интерференции при масштабах, сравнимых с длиной световой волны. Например, даже одиночные фотоны, проходящие через двойную щель, создают на экране интерференционную картину, определяемую уравнениями Максвелла[1].
Тем не менее, эксперимент показывает, что фотон не есть короткий импульс электромагнитного излучения, например, он не может быть разделён на несколько пучков оптическими делителями лучей, что наглядно показал эксперимент, проведённый французскими физиками Гранжье, Роже и Аспэ в 1986 году[2]. Корпускулярные свойства света проявляются при фотоэффекте и в эффекте Комптона. Фотон ведет себя и как частица, которая излучается или поглощается целиком объектами, размеры которых много меньше его длины волны (например, атомными ядрами), или вообще могут считаться точечными (например, электрон).
5. Свойства волн де Бройля и их статистическая интерпретация. Опыты, подтверждающие волновые свойства микрочастиц.
Волны де Бройля — волны, связанные с любой микрочастицей и отражающие их квантовую природу. Любая движущаяся частица (например, электрон) ведёт себя не только как локализованный в пространстве перемещающийся объект - корпускула, но и как волна, причём длина этой волны даётся формулой  = h/р, где h = 6.6.10-34 Дж.сек – постоянная Планка, а р – импульс частицы. Эта волна и получила название волны де Бройля.
= h/р, где h = 6.6.10-34 Дж.сек – постоянная Планка, а р – импульс частицы. Эта волна и получила название волны де Бройля.
Согласно статистической интерпретации волны де Бройля следует рассматривать как волны вероятности. Более определенно: интенсивность волны де Бройля в каком-либо месте пространства пропорциональна вероятности обнаружить частицу в этом месте.
Свойства волн де Бройля:
1) Фазовая скорость волны де Бройля вычисляется в результате дифференцирования этого уравнения по времени: E – p dx/dt = 0,. υф = dx/dt = E/ p = mc2/mυ = c c/υ, где υ -скорость частицы. Т.к. υ<c, то фазовая скорость волн де Бройля всегда больше скорости света в вакууме, т.е. υф > c.
Это соотношение отражает особое специфическое свойство волн де Бройля.
2) Групповая скорость волн де Бройля равна скорости движения частиц: υr = ds/dt = υ.
3) Длинам боровских орбит соответствуют стоячие волны де Бройля, т.е. в длину боровской орбиты укладывается целое число стоячих волн де Бройля: 2πrn = nλ.
Гипотеза де Бройля объясняет ряд экспериментов, необъяснимых в рамках классической физики[2]: - Опыт Дэвиссона — Джермера по дифракции электронов на кристаллахникеля. - Опыт Дж. П. Томсона по дифракции электронов на металлической фольге. - Эффект Рамзауэра аномального уменьшения сечения рассеяния электронов малых энергий атомамиаргона. -Дифракция нейтронов на кристаллах (опыты Г. Хальбана, П. Прайсверка и Д. Митчелла).
6. Волновой пакет микрочастицы. Соотношение неопределенностей Гейзенберга.
Волновой пакет — определённая совокупность волн, обладающих разными частотами, которые описывают обладающую волновыми свойствами формацию, в общем случае ограниченную во времени и пространстве. Так, в квантовой механике описание частицы в виде волновых пакетов способствовало принятию статистической интерпретации квадрата модуля волновой функции.[1]
Произвольная отдельная волна  как функция радиус-вектора
как функция радиус-вектора 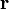 и времени
и времени  описывается выражением
описывается выражением

где  — мнимая единица,
— мнимая единица,  — энергия, переносимая волной,
— энергия, переносимая волной,  — редуцированная постоянная Планка,
— редуцированная постоянная Планка,  — импульс, переносимый волной,
— импульс, переносимый волной,  — её «круговая» частота (обычная частота, умноженная на
— её «круговая» частота (обычная частота, умноженная на  ),
), 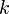 — волновое число (определяемое как
— волновое число (определяемое как  ; здесь
; здесь  скорость света).
скорость света).
Для волнового описания отдельной частицы, обладающей массой покоя, необходимо просуммировать некоторое количество волн, обладающих близкими частотами,— и в таком случае волновая функция 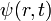 будет заметно отлична от нуля лишь в некоторой, сравнительно небольшой области пространства. Получится волновой пакет.
будет заметно отлична от нуля лишь в некоторой, сравнительно небольшой области пространства. Получится волновой пакет.
Образуем волновой пакет из суперпозиции (набора) плоских волн, для которых волновое число 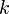 изменяется от
изменяется от  до
до  (для простоты предположим, что на имеющем основное значение интервале амплитуды остаются постоянными и равными
(для простоты предположим, что на имеющем основное значение интервале амплитуды остаются постоянными и равными 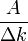 ):
):

где теперь 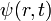 обозначает результирующую волновую функцию, а величины
обозначает результирующую волновую функцию, а величины  обозначают вклады волн
обозначают вклады волн  , из которых образован пакет, в результирующую волну, причем
, из которых образован пакет, в результирующую волну, причем  .
.
Принцип неопределённости Гейзенберга - в квантовой механике так называют принцип, дающий нижний (ненулевой) предел для произведения дисперсий величин, характеризующих состояние системы.
Соотношения неопределённости Гейзенберга — это теоретический предел точности любых измерений. Они справедливы для так называемых идеальных измерений, иногда называемых измерениями фон Неймана. Они тем более справедливы для неидеальных измерений или измерений Ландау.
Соответственно, любая частица (в общем смысле, например несущая дискретный электрический заряд) не может быть описана одновременно как «классическая точечная частица» и как волна. (Сам факт того, что какое-либо из этих описаний может быть справедливо, по крайней мере в отдельных случаях, называют корпускулярно-волновым дуализмом). Принцип неопределённости, в виде, первоначально предложенном Гейзенбергом, верен в случае, когда ни одно из этих двух описаний не является полностью и исключительно подходящим, например частица в коробке с определённым значением энергии; то есть для систем, которые не характеризуются ни каким-либо определённым «положением» (какое-либо определённое значение расстояния от потенциальной стенки), ни каким-либо определённым значением импульса (включая его направление).
Соотношение неопределенности Гейзенберга показывает, что “между точностью, с которой одновременно может быть установлено положение частицы, и точностью ее импульса существует определенное соотношение”: 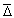 q
q 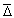 p ≥ h,
p ≥ h,
где 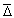 - среднеквадратичное отклонение.
- среднеквадратичное отклонение.
7. Опыты Резерфорда по рассеянию a-частиц. Формула Резерфорда. Модель атома Резерфорда-Бора.

 В отсутствие фольги на экране возникал светлый кружок, состоящий из сцинтилляций, вызванных тонким пучком альфа-частиц. Но когда на пути движения альфа-частиц помещали тонкую золотую фольгу толщиной примерно 0,1 мк (микрон), то наблюдаемая на экране картинка сильно менялась: отдельные вспышки появлялись не только за пределами прежнего кружка, но их можно было даже наблюдать с противоположной стороны золотой фольги.
В отсутствие фольги на экране возникал светлый кружок, состоящий из сцинтилляций, вызванных тонким пучком альфа-частиц. Но когда на пути движения альфа-частиц помещали тонкую золотую фольгу толщиной примерно 0,1 мк (микрон), то наблюдаемая на экране картинка сильно менялась: отдельные вспышки появлялись не только за пределами прежнего кружка, но их можно было даже наблюдать с противоположной стороны золотой фольги.
Подсчитывая число сцинтилляций в единицу времени в разных местах экрана, можно установить распределение в пространстве рассеянных альфа-частиц. Число альфа-частиц быстро убывает с увеличением угла рассеяния.
Наблюдаемая на экране картина позволила заключить, что большинство альфа-частиц проходит сквозь золотую фольгу без заметного изменения направления их движения. Однако некоторые частицы отклонялись на большие углы от первоначального направления альфа-частиц (порядка 135о…150о) и даже отбрасывались назад. Исследования показали, что при прохождении альфа-частиц сквозь фольгу примерно на каждые 10000 падающих частиц только одна отклоняется на угол более 10о от первоначального направления движения. Лишь в виде редкого исключения одна из огромного числа альфа-частиц отклоняется от своего первоначального направления.
Тот факт, что многие альфа-частицы проходили сквозь фольгу, не отклоняясь от своего направления движения, говорит о том, что атом не является сплошным образованием. Так как масса альфа-частицы почти в 8000 раз превосходит массу электрона, то электроны, входящие в состав атомов фольги, не могут заметно изменить траекторию альфа-частиц. Рассеяние альфа-частиц может вызывать положительно заряженная частица атома – атомное ядро.
Атомное ядро – это тело малых размеров, в котором сконцентрированы почти вся масса и почти весь положительный заряд атома.
Чем ближе альфа-частица подходила к ядру, тем больше была сила электрического взаимодействия и тем на больший угол частица отклонялась. На малых расстояниях от ядра положительно-заряженная альфа-частица испытывает значительную силу отталкивания F от ядра, которую определяют по закону Кулона:
отталкивания F от ядра, которую определяют по закону Кулона:

где r – расстояние от ядра до альфа-частицы; ε0 – электрическая постоянная в единицах измерения СИ; p – число протонов в ядре; е = 1,6*10-19 Кл – абсолютное значение элементарного электрического заряда (заряда электрона); 2e – заряд альфа-частицы
На рисунке 1.2 показаны траектории альфа-частиц, пролетающих на различных расстояниях от ядра.
Резерфорд смог ввести формулу, связывающую количество рассеянных на определённый угол альфа-частиц с энергией альфа-частиц и протонов р в ядре атома. Опытная проверка формулы подтвердила её справедливость и показала, что количество протонов в ядре равно числу внутриатомных электронов Z и определяется атомным номером химического элемента (то есть порядковым номером элемента в периодической системе Д.И.Менделеева):
p = Z

Рис. 1.2. Траектории альфа-частиц. Подсчитывая количество альфа-частиц, рассеянных на различные углы, Резерфорд смог оценить линейные размеры ядра. Чтобы положительное ядро могло отбросить альфа-частицу назад, потенциальная энергия электростатического (кулоновского) отталкивания у границ ядра атома должна равняться кинетической энергии альфа-частицы:
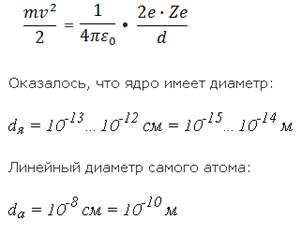
Фо́рмула Резерфóрда — формула для дифференциального эффективного поперечного сечения рассеяния нерелятивистских заряженных частиц в телесный угол Ω в кулоновском поле другой неподвижной заряженной частицы или ядра (мишени). Подтверждена эмпирически Э. Резерфордом в 1911 году в опытах по рассеянию α-частиц на тонкой золотой фольге субмикронной толщины. В системе центра инерции налетающей и рассеивающей частиц записывается следующим образом:

где  и
и  — заряды налетающей частицы и мишени,
— заряды налетающей частицы и мишени, 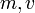 — масса и скорость налетающей частицы,
— масса и скорость налетающей частицы,  — двумерный угол рассеяния,
— двумерный угол рассеяния,  — элементарный заряд,
— элементарный заряд,  — дифференциальное сечение,
— дифференциальное сечение,  — телесный угол.
— телесный угол.
Планетарная модель атома Бора-Резерфорда. В 1911 году[3] Эрнест Резерфорд, проделав ряд экспериментов, пришёл к выводу, что атом представляет собой подобие планетной системы, в которой электроны движутся по орбитам вокруг расположенного в центре атома тяжёлого положительно заряженного ядра («модель атома Резерфорда»). Однако такое описание атома вошло в противоречие с классической электродинамикой. Дело в том, что, согласно классической электродинамике, электрон при движении с центростремительным ускорением должен излучать электромагнитные волны, а, следовательно, терять энергию. Расчёты показывали, что время, за которое электрон в таком атоме упадёт на ядро, совершенно ничтожно. Для объяснения стабильности атомов Нильсу Бору пришлось ввести постулаты, которые сводились к тому, что электрон в атоме, находясь в некоторых специальных энергетических состояниях, не излучает энергию («модель атома Бора-Резерфорда»). Постулаты Бора показали, что для описания атома классическая механика неприменима. Дальнейшее изучение излучения атома привело к созданию квантовой механики, которая позволила объяснить подавляющее большинство наблюдаемых фактов.
8. Закономерности в спектрах атома водорода. Серии Лаймана, Бальмера, Пашена. Комбинационный принцип Ритца.
Спектральные закономерности
В середине XVIII в. Г. Кирхгоф обнаружил: свечение газов дает четко выраженные дискретные линии.
Швейцарский преподаватель И. Бальмер эмпирически вывел формулу для спектра водорода (1885):  , где п— любое целое число >2, т. е. п= 3, 4, 5 и т.д.
, где п— любое целое число >2, т. е. п= 3, 4, 5 и т.д.
Величина R носит название "постоянная Ридберга"
Для инфракрасной области спектра аналогичную формулу вывел Ф. Пашен:
 ,
,
где п— любое целое число >3, т. е. п=, 4, 5 и т.д.
 А для ультрафиолетовой - Т. Лайман
А для ультрафиолетовой - Т. Лайман 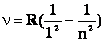 , где п— любое целое число >1, т. е. п=2, 3, 4, 5 и т.д.
, где п— любое целое число >1, т. е. п=2, 3, 4, 5 и т.д.
Значения длин волн спектральных линий, вычисленных по этим формулам, совпадали с исключительной точностью со значениями длин волн этих линий, измеренных экспериментально. В конце XIX в. ученые обнаружили фундаментальную закономерность в микромире, которую в то время объяснить не смогли.
Только через 30 лет Н. Бор дал физическую интерпретацию этой формулы.
Он предположил, что два члена в формуле Бальмера представляют собой полные энергии разрешенных орбит электрона в атоме водорода.
Преобразовав формулу Бальмера (умножив обе части на h), получим: 
Учитывая, что согласно гипотезе Планка энергия кванта D  , получим:
, получим: 
Свои постулаты Н. Бор применил для построения теории атома водорода.
Комбинацио́нный при́нцип Ри́тца — основной закон спектроскопии, установленный эмпирически Вальтером Ритцем в 1908 году. Согласно этому принципу всё многообразие спектральных линий какого-либо элемента может быть представлено через комбинации неких величин, получивших название термы. Спектроскопическое волновое число (не путать с волновым вектором k) каждой спектральной линии можно выразить через разность двух термов:
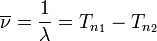 ;
;
Если зафиксировать  и перебирать все возможные значения
и перебирать все возможные значения  , то получится набор линий, именуемый спектральной серией. Из комбинационного принципа следует, что разность волновых чисел двух спектральных линий одной и той же серии атома даёт волновое число спектральной линии какой-то другой серии того же атома.
, то получится набор линий, именуемый спектральной серией. Из комбинационного принципа следует, что разность волновых чисел двух спектральных линий одной и той же серии атома даёт волновое число спектральной линии какой-то другой серии того же атома.
Следствие комбинационного принципа: Разность волновых чисел двух спектральных линий одной и той же серии атома даёт волновое число спектральной линии какой-то другой серии того же атома. Доказательство: Рассмотрим две спектральные линии одной серии:
 ,
, 
Пусть  , тогда
, тогда 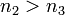 . Вычитая второе равенство из первого получаем
. Вычитая второе равенство из первого получаем
 .
.
9. Дискретность квантовых состояний атома. Постулаты Бора. Опыты Франка-Герца.
Модель Бора выявила истинное значение спектральных законов и позволила установить, как эти законы отражают квантовый характер внутренней структуры атома - устойчивость структуры атома оказалась неразрывно связанной с существованием квантов. В модели Бора каждый атом обладает некоторой последовательностью квантовых (стационарных) состояний. Каждый вид атома имеет свою последовательность квантовых значений энергии, соответствующих различным возможным стационарным состояниям.
Постулаты Бора:
1) В атоме существует ряд дискретных стационарных состояний, которым соответствуют определенные значения энергии атома E1, E2 и т.д. В стационарном состоянии атом не излучает и не поглощает энергии.
2) Переходя из одного стационарного состояния в другое, атом излучает и поглощает квант энергии ε = hv, равный разности энергий En и En' двух стационарных состояний: hv = En' - En.
Атом водорода (Z = 1) имеет наиболее простой линейчатый спектр излучения. Частоты спектральных линий для атома водорода и водородоподобных атомов определяются по формуле: v = Rv(1/n2 – 1/n'2), где Rv = Z2me4/8ε02h3 = 3,29 · 1015 с-1 – постоянная Ридберга.
Также эта формула может быть записана через длину волны λ: 1/λ = Rλ(1/n2 – 1/n'2), где Rλ = 1,097 · 107 м-1.
Недостатки теории Бора:
- не смогла объяснить интенсивность спектральных линий.
- справедлива только для водородоподобных атомов и не работает для атомов, следующих за ним в таблице Менделеева.
- теория Бора логически противоречива: не является ни классической, ни квантовой. В системе двух уравнений, лежащих в её основе, одно - уравнение движения электрона - классическое, другое - уравнение квантования орбит - квантовое.
Опыт Франка - Герца - опыт, явившийся экспериментальным доказательством дискретности внутренней энергии атома.
В опыте наблюдался монотонный рост I при увеличении ускоряющего потенциала вплоть до 4,9 в, то есть электроны с энергией Е < 4,9 эв испытывали упругие соударения с атомами Hg и внутренняя энергия атомов не менялась. При значении V = 4,9 в (и кратных ему значениях 9,8 в, 14,7 в) появлялись резкие спады тока. Это определённым образом указывало на то, что при этих значениях V соударения электронов с атомами носят неупругий характер, т. е. энергия электронов достаточна для возбуждения атомов Hg. При кратных 4,9 эв значениях энергии электроны могут испытывать неупругие столкновения несколько раз.
Таким образом, опыт Франка - Герца показал, что спектр поглощаемой атомом энергии не непрерывен, а дискретен, минимальная порция (квант электромагнитного поля), которую может поглотить атом Hg, равна 4,9 эВ. Значение длины волны λ = 253,7 нм свечения паров Hg, возникавшее при V > 4,9 В, оказалось в соответствии со вторым постулатом Бора.
10. Спонтанные и вынужденные переходы. Коэффициенты Эйнштейна. Спектральная плотность излучения.
Переходы, которые совершаются в системах микрочастиц, классифицируются по различным признакам. Основными видами переходов являются спонтанные, вынужденные и релаксационные.
 Спонтанные переходы - самопроизвольные излучательные квантовые переходы из верхнего энергетического состояния в нижнее. Электромагнитное поле спонтанного излучения характеризуется тремя параметрами: центральной частотой спектральной линии νπ, спектральной плотностью излучения S(v) и мощностью излучения. Центральная частота излучения называется также частотой квантового перехода и частотой спектральной линии и определяется постулатом Бора:
Спонтанные переходы - самопроизвольные излучательные квантовые переходы из верхнего энергетического состояния в нижнее. Электромагнитное поле спонтанного излучения характеризуется тремя параметрами: центральной частотой спектральной линии νπ, спектральной плотностью излучения S(v) и мощностью излучения. Центральная частота излучения называется также частотой квантового перехода и частотой спектральной линии и определяется постулатом Бора:
где W2 и W1 - энергии верхнего и нижнего уровней соответственно; h -постоянная Планка.
Определим теперь мощность спонтанного излучения. Здесь и в дальнейшем будем рассматривать процессы в единице объема вещества.
Пусть в рассматриваемом объеме содержится N2 частиц с энергией W2 и N1 частиц с энергией W1. Число частиц в единице объема с данной энергией называется населенностью уровня. Спонтанные переходы носят случайный характер и оцениваются вероятностью перехода в единицу времени A21, которая называется коэффициентом Эйнштейна для спонтанных переходов. Если населенность уровня Ν2 остается неизменной во времени (или изменяется незначительно), то число переходов в единицу времени с уровня W2 на уровень W1 составит
n21(в)=W21N2=B21uνN2
n12(в)=W12N1=B12uνN1
При каждом переходе выделяется энергия W2-W1= hv21 поэтому мощность излучения
Р21 =n21 (W2 -W1)=N2 A21 h v21
Между коэффициентом Эйнштейна и средним временем жизни частицы на уровне (время, за которое при отсутствии внешнего возбуждения населенность уровня падает в е раз) существует простая связь:
A21= 1/B2. (10.4)
В системе частиц, имеющих несколько энергетических уровней, возможны спонтанные переходы частиц с данного уровня на нижние (рис. 10.2). Полная вероятность Aj спонтанного перехода с уровня j на все нижние уровни i равна сумме вероятностей отдельных спонтанных переходов Аji:
 . (10.5)
. (10.5)
Уровни, для которых вероятность спонтанных переходов очень мала, называют метастабильными.
Время жизни на уровне j в многоуровневой системе определяется аналогично (10.4) с учетом (10.5):
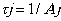 (10.6)
(10.6)
Среднее время жизни на уровне составляет величину в пределах от единицы до сотен наносекунд. На метастабильных уровнях время жизни составляет миллисекунды.

Рис. 10.2 Спонтанные переходы частиц с одного уровня на другой
Вынужденные переходы - этоквантовые переходы частиц под действием внешнего электромагнитного поля, частота которого совпадает или близка к частоте перехода. При этом возможны переходы с верхнего уровня 2 на нижний 1 и с нижнего на верхний. В первом случае под действием внешнего электромагнитного поля с частотой v21 происходит вынужденное испускание кванта энергии. Особенность вынужденного испускания состоит в том, что появившийся фотон полностью идентичен фотону внешнего поля. Вынужденное излучение имеет такие же частоту, фазу, направление распространения и поляризацию, как и вынуждающее излучение. Поэтому вынужденное излучение увеличивает энергию электромагнитного поля с частотой перехода v2 1. Это служит предпосылкой для создания квантовых усилителей и генераторов.
При каждом вынужденном переходе снизу вверх затрачивается квант энергии внешнего поля hv21.
Вынужденные переходы (как и спонтанные) имеют статистический характер. Поэтому вводятся вероятностные коэффициенты: W21 - вероятность вынужденного перехода сверху вниз и W12 - снизу вверх в 1с. Эти вероятности пропорциональны объемной плотности энергии внешнего поля uv в единичном спектральном интервале на частоте перехода и определяются соотношениями
W21=B21 uv,
W12=B12 uv, (10.7)
где B21 и B12 - коэффициенты Эйнштейна для вынужденных переходов с излучением и поглощением энергии соответственно.
Коэффициенты B21 и Β12 имеют смысл вероятностей вынужденных переходов в 1 с при единичной объемной плотности энергии внешнего поля (uv = 1 Дж см -3c -1).
Число вынужденных переходов сверху вниз с излучением энергии в единицу времени в единице объема пропорционально вероятности W21 и населенности верхнего уровня N2, т.е. с учетом (10.7)
n 21=W21 N2=B21 uv N2 . (10.8)
Аналогично при тех же условиях число вынужденных переходов снизу вверх с поглощением энергии
n 12=W12 N1=B12 uv N2 . (10.9)
В приборах СВЧ-диапазона, работающих на «низкой» частоте, вероятность спонтанных переходов мала по сравнению с вероятностью вынужденных переходов и их роль невелика. В лазерах же, работающих на оптических частотах, пренебрегать спонтанными переходами нельзя.
Спектральная плотность излучения — характеристика спектра излучения, равная отношению интенсивности (плотности потока) излучения в узком частотном интервале к величине этого интервала. Является применением понятия спектральной плотности мощности к электромагнитному излучению.
Энергия светового пучка неравномерно распределена по волнам различных длин. Зависимость частоты от длины волны описывается как λv=c
Для характеристики распределения излучения по частотам используют интенсивность, приходящуюся на единичный интервал частот. Эта величина называется спектральной плотностью интенсивности излучения и обозначается как I(v).
Различным видимым цветам соответствуют различные спектральные плотности видимого света.




 — постоянная Планка,
— постоянная Планка, 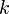 — постоянная Больцмана.
— постоянная Больцмана.


 дает формулу для измерения длины волны при рассеянии фотона на (неподвижных) электронах:
дает формулу для измерения длины волны при рассеянии фотона на (неподвижных) электронах: где
где  - так называемая комптоновская длина волны.
- так называемая комптоновская длина волны.
 . Каждый фотон обладает импульсом
. Каждый фотон обладает импульсом  . Полный импульс, получаемый поверхностью тела, равен
. Полный импульс, получаемый поверхностью тела, равен  . Световое давление:
. Световое давление: 



 = h/р, где h = 6.6.10-34 Дж.сек – постоянная Планка, а р – импульс частицы. Эта волна и получила название волны де Бройля.
= h/р, где h = 6.6.10-34 Дж.сек – постоянная Планка, а р – импульс частицы. Эта волна и получила название волны де Бройля. как функция радиус-вектора
как функция радиус-вектора 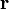 и времени
и времени  описывается выражением
описывается выражением
 — мнимая единица,
— мнимая единица,  — энергия, переносимая волной,
— энергия, переносимая волной,  — импульс, переносимый волной,
— импульс, переносимый волной,  — её «круговая» частота (обычная частота, умноженная на
— её «круговая» частота (обычная частота, умноженная на  ),
),  ; здесь
; здесь  скорость света).
скорость света).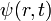 будет заметно отлична от нуля лишь в некоторой, сравнительно небольшой области пространства. Получится волновой пакет.
будет заметно отлична от нуля лишь в некоторой, сравнительно небольшой области пространства. Получится волновой пакет. до
до  (для простоты предположим, что на имеющем основное значение интервале амплитуды остаются постоянными и равными
(для простоты предположим, что на имеющем основное значение интервале амплитуды остаются постоянными и равными 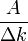 ):
):
 обозначают вклады волн
обозначают вклады волн  , из которых образован пакет, в результирующую волну, причем
, из которых образован пакет, в результирующую волну, причем  .
. q
q 
 В отсутствие фольги на экране возникал светлый кружок, состоящий из сцинтилляций, вызванных тонким пучком альфа-частиц. Но когда на пути движения альфа-частиц помещали тонкую золотую фольгу толщиной примерно 0,1 мк (микрон), то наблюдаемая на экране картинка сильно менялась: отдельные вспышки появлялись не только за пределами прежнего кружка, но их можно было даже наблюдать с противоположной стороны золотой фольги.
В отсутствие фольги на экране возникал светлый кружок, состоящий из сцинтилляций, вызванных тонким пучком альфа-частиц. Но когда на пути движения альфа-частиц помещали тонкую золотую фольгу толщиной примерно 0,1 мк (микрон), то наблюдаемая на экране картинка сильно менялась: отдельные вспышки появлялись не только за пределами прежнего кружка, но их можно было даже наблюдать с противоположной стороны золотой фольги.

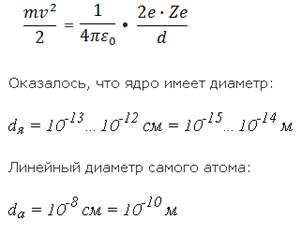

 и
и  — заряды налетающей частицы и мишени,
— заряды налетающей частицы и мишени, 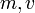 — масса и скорость налетающей частицы,
— масса и скорость налетающей частицы,  — двумерный угол рассеяния,
— двумерный угол рассеяния,  — элементарный заряд,
— элементарный заряд,  — дифференциальное сечение,
— дифференциальное сечение,  — телесный угол.
— телесный угол. , где п— любое целое число >2, т. е. п= 3, 4, 5 и т.д.
, где п— любое целое число >2, т. е. п= 3, 4, 5 и т.д. ,
, А для ультрафиолетовой - Т. Лайман
А для ультрафиолетовой - Т. Лайман 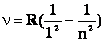 , где п— любое целое число >1, т. е. п=2, 3, 4, 5 и т.д.
, где п— любое целое число >1, т. е. п=2, 3, 4, 5 и т.д.
 , получим:
, получим: 
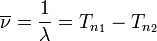 ;
; и перебирать все возможные значения
и перебирать все возможные значения  , то получится набор линий, именуемый спектральной серией. Из комбинационного принципа следует, что разность волновых чисел двух спектральных линий одной и той же серии атома даёт волновое число спектральной линии какой-то другой серии того же атома.
, то получится набор линий, именуемый спектральной серией. Из комбинационного принципа следует, что разность волновых чисел двух спектральных линий одной и той же серии атома даёт волновое число спектральной линии какой-то другой серии того же атома. ,
, 
 , тогда
, тогда 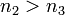 . Вычитая второе равенство из первого получаем
. Вычитая второе равенство из первого получаем .
. Спонтанные переходы - самопроизвольные излучательные квантовые переходы из верхнего энергетического состояния в нижнее. Электромагнитное поле спонтанного излучения характеризуется тремя параметрами: центральной частотой спектральной линии νπ, спектральной плотностью излучения S(v) и мощностью излучения. Центральная частота излучения называется также частотой квантового перехода и частотой спектральной линии и определяется постулатом Бора:
Спонтанные переходы - самопроизвольные излучательные квантовые переходы из верхнего энергетического состояния в нижнее. Электромагнитное поле спонтанного излучения характеризуется тремя параметрами: центральной частотой спектральной линии νπ, спектральной плотностью излучения S(v) и мощностью излучения. Центральная частота излучения называется также частотой квантового перехода и частотой спектральной линии и определяется постулатом Бора: . (10.5)
. (10.5)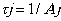 (10.6)
(10.6)



