

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

История создания датчика движения: Первый прибор для обнаружения движения был изобретен немецким физиком Генрихом Герцем...

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

История создания датчика движения: Первый прибор для обнаружения движения был изобретен немецким физиком Генрихом Герцем...
Топ:
Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов...
Эволюция кровеносной системы позвоночных животных: Биологическая эволюция – необратимый процесс исторического развития живой природы...
Выпускная квалификационная работа: Основная часть ВКР, как правило, состоит из двух-трех глав, каждая из которых, в свою очередь...
Интересное:
Уполаживание и террасирование склонов: Если глубина оврага более 5 м необходимо устройство берм. Варианты использования оврагов для градостроительных целей...
Что нужно делать при лейкемии: Прежде всего, необходимо выяснить, не страдаете ли вы каким-либо душевным недугом...
Подходы к решению темы фильма: Существует три основных типа исторического фильма, имеющих между собой много общего...
Дисциплины:
|
из
5.00
|
Заказать работу |
ЛЕКЦИЯ 1
Биоорганическая химия (БОХ), ее значение в медицине
БОХ – это наука, изучающая биологическую функцию органических веществ в организме.
БОХ возникла во 2-ой половине ХХ века. Объектами ее изучения служат биополимеры, биорегуляторы и отдельные метаболиты.
Биополимеры – высокомолекулярные природные соединения, которые являются основой всех организмов. Это пептиды, белки, полисахариды, нуклеиновые кислоты (НК), липиды и др.
Биорегуляторы – соединения, которые химически регулируют обмен веществ. Это витамины, гормоны, антибиотики, алкалоиды, лекарственные препараты и др.
Знание строения и свойств биополимеров и биорегуляторов позволяет познать сущность биологических процессов. Так, установление строения белков и НК позволило развить представления о матричном биосинтезе белка и роли НК в сохранении и передаче генетической информации.
БОХ играет большую роль в установлении механизма действия ферментов, лекарств, процессов зрения, дыхания, памяти, нервной проводимости, мышечного сокращения и др.
Основная проблема БОХ – это выяснение взаимосвязи структуры и механизма действия соединений.
БОХ основана на материале органической химии.
ОРГАНИЧЕСКАЯ ХИМИЯ
Это наука, изучающая соединения углерода. В настоящее время насчитывается ~ 16 млн. органических веществ.
Причины многообразия органических веществ.
1. Соединения атомов С друг с другом и др. элементами периодической системы Д. Менделеева. При этом образуются цепи и циклы:

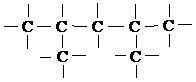
Прямая цепь Разветвленная цепь

Атом С может находиться в трех гибридных состояниях:
 | 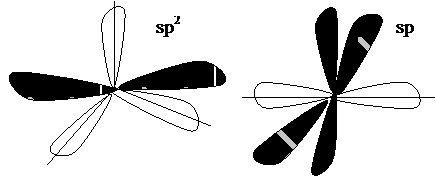 | ||
Тетраэдрическая Плоскостная конфигурация
конфигурация атома С атома С
2. Гомология – это существование веществ с близкими свойствами, где каждый член гомологического ряда отличается от предыдущего на группу
–СН2–. Например, гомологический ряд предельных углеводородов:
| СН4 | С2Н6 | С3Н8 | С4Н10 | С5Н12 | С6Н14 | и так |
| Метан | Этан | Пропан | Бутан | Пентан | Гексан | далее. |
3. Изомерия – это существование веществ, имеющих одинаковый качественный и количественный состав, но различное строение.
А.М. Бутлеров (1861) создал теорию строения органических соединений, которая и по сей день служит научной основой органической химии.
Основные положения теории строения органических соединений:
1) атомы в молекулах соединены друг с другом химическими связями в соответствии с их валентностью;
2) атомы в молекулах органических соединений соединяются между собой в определенной последовательности, что обусловливает химическое строение молекулы;
3) свойства органических соединений зависят не только от числа и природы входящих в их состав атомов, но и от химического строения молекул;
4) в молекулах существует взаимное влияние атомов как связанных, так и непосредственно друг с другом не связанных;
5) химическое строение вещества можно определить в результате изучения его химических превращений и, наоборот, по строению вещества можно охарактеризовать его свойства.
Рассмотрим некоторые положения теории строения органических соединений.
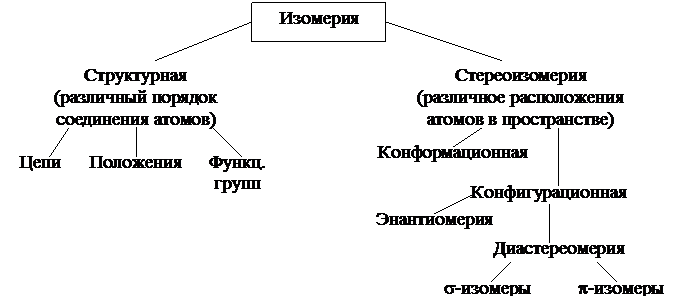
Структурная изомерия
Она делится:
1) Изомерия цепи
| С4Н10 | СН3 – СН2 – СН2 – СН3 | 
|
| Бутан | 2-Метилпропан |
2) Изомерия положения кратной связи и функциональных групп
| С4Н8 | СН2 = СН – СН2 – СН3 | СН3 – СН = СН – СН3 |
| Бутен-1 | Бутен-2 | |
| С3Н7ОН | СН3 – СН2 – СН2 – ОН | 
|
| Пропанол-1 | Пропанол-2 |
3) Изомерия функциональных групп (межклассовая изомерия)
| С3Н6О | 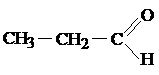
| 
|
| Пропаналь | Пропанон-2 |
Формулы Ньюмена
С6Н12
Циклогексан
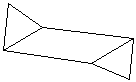
| 
|
| «Кресло» | «Ванна» |
Форма «кресла» более энергетически выгодна, чем «ванна».
Конфигурационные изомеры
Это стереоизомеры, молекулы которых имеют различное расположение атомов в пространстве без учета конформаций.
По типу симметрии все стереоизомеры делятся на энантиомеры и диастереомеры.
Энантиомеры (оптические изомеры, зеркальные изомеры, антиподы) – это стереоизомеры, молекулы которых относятся между собой как предмет и несовместимое с ним зеркальное отображение. Это явление наз-ся энантиомерией. Все химические и физические св-ва энантиомеров одинаковы, кроме двух: вращение плоскости поляризованного света (в приборе поляриметре) и биологическая активность. Условия энантиомерии: 1) атом С находится в состоянии sp3-гибридизации; 2) отсутствие всякой симметрии; 3) наличие асимметрического (хирального) атома С, т.е. атома, имеющего четыре разных заместителя.
Многие окси- и аминокислоты обладают способностью вращать плоскость поляризации луча света влево или вправо. Это явление наз-ся оптической активностью, а сами молекулы оптически активными. Отклонение луча света вправо отмечают знаком «+», влево – «–» и указывают угол вращения в градусах.
Абсолютную конфигурацию молекул определяют сложными физико-химическими методами.
Относительную конфигурацию оптически активных соединений определяют путем сравнения со стандартом глицеринового альдегида. Оптически активные вещ-ва, имеющие конфигурацию правовращающего или левовращающего глицеринового альдегида (М. Розанов, 1906), наз-ся вещ-вами D- и L-ряда. Равная смесь право- и левовращающих изомеров одного соединения наз-ся рацематом и оптически неактивна.
Исследования показали, что знак вращения света нельзя связывать с принадлежностью вещ-ва к D- и L-рядам, его определяют только экспериментально в приборах – поляриметрах. Например, L-молочная к-та имеет угол вращения +3,8 о, D- молочная к-та - -3,8 о.
Энантиомеры изображают с помощью формул Фишера.
 | |||
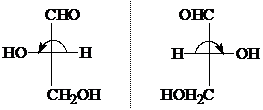 | |||
L-ряд D-ряд
Количество изомеров определяются по формуле 2n, n – число асимметрических атомов углерода.

 Пример:
Пример:

|
| Молочная кислота |
L-ряд D-ряд
Среди энантиомеров могут быть симметричные молекулы, не обладающие оптической активностью, и наз-ся мезоизомерами.
 |
| Например: Винная к-та |

| D – (+) – ряд L – (–) – ряд | Мезовинная к-та |
Рацемат – виноградная к-та
Оптические изомеры, не являющиеся зеркальными изомерами, отличающиеся конфигурацией нескольких, но не всех асимметрических атомов С, обладающие различными физическими и химическими св-вами, наз-ся s- ди - а -стереоизомерами.
p-Диастереомеры (геометрические изомеры) – это стереомеры, имеющие в молекуле p-связь. Они встречаются у алкенов, непредельных высших карбоновых к-т, непредельных дикарбоновых к-т
Биологическая активность органических вещ-в связана с их строением.
Например:
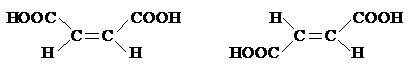
Цис-бутендиовая к-та, Транс-бутендиовая к-та,
малеиновая к-та – фумаровая к-та – не ядовита,
очень ядовита содержится в организме
Все природные непредельные высшие карбоновые к-ты являются цис-изомерами.
ЛЕКЦИЯ 2
Сопряженные системы
В простейшем случае сопряженные системы – это системы с чередующимися двойными и одинарными связями. Они могут быть открытыми и закрытыми. Открытая система имеется в диеновых углеводородах (УВ).





|
 С4Н6
С4Н6


 СН2 = СН – СН = СН2
СН2 = СН – СН = СН2
Бутадиен-1, 3
 |  |  | |||
Все атомы С находится в состоянии sp2 – гибридизации. Четыре негибридные (р-орбитами), перекрываясь между собой, образуют единую электронную систему. Этот вид сопряжения наз-ся p, p-сопряжением.

 С2Н3Сl
С2Н3Сl
|
СН2 = СН – Сl
Здесь происходит сопряжение p-электронов с р-электронами. Этот вид сопряжения наз-ся р, p-сопряжением.
Закрытая система имеется в ароматических УВ.
 С6Н6
С6Н6
|
Ароматичность
Это понятие, включающее различные свойства ароматических соединений. Условия ароматичности: 1) плоский замкнутый цикл, 2) все атомы С находятся в sp2 – гибридизации, 3) образуется единая сопряженная система всех атомов цикла, 4) выполняется правило Хюккеля: “В сопряжении участвуют 4n+2 p-электронов, где n = 1, 2, 3... ”
Простейший представитель ароматических УВ – бензол. Он удовлетворяет всем четырем условиям ароматичности.
Правило Хюккеля: 4n+2 = 6, n = 1.
 Нафталин
Нафталин
| Нафталин – ароматическое соединение Правило Хюккеля: 4n+2 = 10, n = 2. |
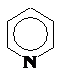 Пиридин
Пиридин
| Пиридин – ароматическое гетероциклическое соединение. |
Взаимное влияние атомов в молекуле
В 1861 г русский ученый А.М. Бутлеров высказал положение: «Атомы в молекулах взаимно влияют друг на друга». В настоящее время это влияние передается двумя путями: индуктивным и мезомерным эффектами.
Индуктивный эффект
Это передача электронного влияния по цепи s-связи. Известно, что связь между атомами с различной электроотрицательностью (ЭО) поляризована, т.е. смещена к более ЭО атому. Это приводит к появлению на атомах эффективных (реальных) зарядов (d). Такое электронное смещение наз-ся индуктивным и обозначается буквой I и стрелкой ®.
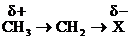 , X = Наl -, НО -, НS -, NН2 - и др.
, X = Наl -, НО -, НS -, NН2 - и др.
Индуктивный эффект может быть положительным или отрицательным. Если заместитель Х притягивает электроны химической связи сильнее, чем атом Н, то он проявляет – I. I(Н) = О. В нашем примере Х проявляет – I.
Если заместитель Х притягивает электроны связи слабее, чем атом Н, то он проявляет +I. Все алкилы (R = СН3 -, С2Н5 - и т.д.), Меn+ проявляют +I.
Мезомерный эффект
 Мезомерный эффект (эффект сопряжения) – это влияние заместителя, передаваемое по сопряженной системе p-связей. Обозначается буквой М и изогнутой стрелкой. Мезомерный эффект может быть «+» или «–».
Мезомерный эффект (эффект сопряжения) – это влияние заместителя, передаваемое по сопряженной системе p-связей. Обозначается буквой М и изогнутой стрелкой. Мезомерный эффект может быть «+» или «–».
Выше было сказано, что имеется два вида сопряжения p, p и р, p.
Примеры:
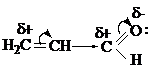 Акролеин
Акролеин
|
 p, p - сопряжение
Альдегидная группа проявляет – М. p, p - сопряжение
Альдегидная группа проявляет – М.
|
|
 Фенол
Фенол
| р, p-сопряжение Гидроксильная группа –ОН проявляет +М. |
Заместитель, притягивающий электроны из сопряженной системы, проявляет –М и наз-ся электроноакцептором (ЭА). Это заместители, имеющие двой-
 |
ную связь и др.
 Заместитель, отдающий электроны в сопряженную систему, проявляет +М и наз-ся электронодонором (ЭД). Это заместители с одинарными связями, имеющие неподеленную электронную пару (и др.).
Заместитель, отдающий электроны в сопряженную систему, проявляет +М и наз-ся электронодонором (ЭД). Это заместители с одинарными связями, имеющие неподеленную электронную пару (и др.).
Таблица 1 Электронные эффекты заместителей
| Заместители | Ориентанты в С6Н5-R | I | М | ||
 Аlk (R-): СН3-, С2Н5-... Аlk (R-): СН3-, С2Н5-...
| Ориентанты I рода: направляют ЭД заместители в орто- и пара- положения | + | |||
– 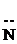 Н2, –NНR, –NR2 Н2, –NНR, –NR2
| – | + | |||
– 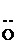 Н, – Н, – 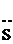 Н, – Н, – 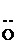 R R
| – | + | |||
–Н 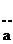 L L
| – | + | |||
 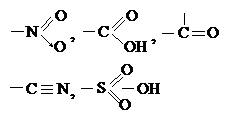
| Ориентанты II рода: направляют заместители в мета- положения | – | – |

Примеры:
ЛЕКЦИЯ 3
Кислотность и основность
Для характеристики кислотности и основности органических соединений применяют теорию Бренстеда. Основные положения этой теории:
1) Кислота – это частица, отдающая протон (донор Н+); основание – это частица, принимающая протон (акцептор Н+).
2) Кислотность всегда характеризуется в присутствии оснований и наоборот.
Примеры:
А – Н +: В Û А– + В – Н+
К-та Осн-ие Сопряженное Сопряженная
осн-ие к-та
СН3СООН + НОН Û СН3СОО– + Н3О+
К-та Осн-ие Сопряженное Сопряженная
осн-ие к-та
НNО3 + СН3СООH Û СН3СООН2+ + NО3-
К-та Осн-ие Сопряженная Сопряженное
к-та осн-ие
Кислоты Бренстеда
3) К-ты Бренстеда делятся на 4 вида в зависимости от кислотного центра:
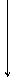 - SН к-ты (тиолы),
- SН к-ты (тиолы),
- ОН к-ты (спирты, фенолы, карбоновые к-ты),
- NН к-ты (амины, амиды),
- СН к-ты (УВ).
В этом ряду сверху вниз кислотность уменьшается.
4) Сила к-ты определяется стабильностью образующегося аниона. Чем стабильнее анион, тем сильнее к-та. Стабильность аниона зависит от делокализации (распределения) «-» заряда по всей частице (аниону). Чем больше делокализован «-» заряд, тем стабильнее анион и сильнее к-та.
Делокализация заряда зависит:
a) от электроотрицательности (ЭО) гетероатома. Чем больше ЭО гетероатома, тем сильнее соответствующая к-та.
Например: R – ОН и R – NН2
Спирты более сильные к-ты, чем амины, т.к. ЭО (О) > ЭО (N).
б) от поляризуемости гетероатома. Чем больше поляризуемость гетероатома, тем сильнее соответствующая к-та.
Например: R – SН и R – ОН
Тиолы более сильные к-ты, чем спирты, т.к. атом S более поляризован, чем атом О.
в) от характера заместителя R (длины его, наличие сопряженной системы, делокализации электронной плотности).
Например: СН3 – ОН, СН3 – СН2 – ОН, СН3 – СН2 – СН2 – ОН
 Кислотность <, т.к. увеличивается длина радикала
Кислотность <, т.к. увеличивается длина радикала
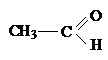 При одинаковом кислотном центре сила спиртов, фенолов и карбоновых к-т не одинакова. Например,
При одинаковом кислотном центре сила спиртов, фенолов и карбоновых к-т не одинакова. Например,
СН3 – ОН, С6Н5 – ОН,

Сила к-ты увеличивается
Фенолы являются более сильными к-тами, чем спирты за счет р, p-сопряжения (+М) группы –ОН.
 Связь О–Н более поляризуется в фенолах. Фенолы могут взаимодействовать даже с солями (FеС13) – качественная реакция на фенолы. Карбоновые
Связь О–Н более поляризуется в фенолах. Фенолы могут взаимодействовать даже с солями (FеС13) – качественная реакция на фенолы. Карбоновые
к-ты по сравнению со спиртами, содержащими одинаковый R, являются более сильными к-тами, т.к. связь О–Н значительно поляризована за счет –М эффекта группы > С = О:
Кроме того карбоксилат-анион более стабилен, чем анион спирта за счет р,p-сопряжения в карбоксильной группе.
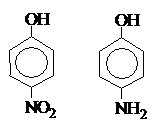 г) от введения заместителей в радикал. ЭА заместители увеличивают кислотность, ЭД заместители уменьшают кислотность.
г) от введения заместителей в радикал. ЭА заместители увеличивают кислотность, ЭД заместители уменьшают кислотность.
Например:
р-Нитрофенол более сильная к-та, чем р-аминофенол, т.к. группа –NО2 является ЭА.
СН3–СООН ССl3–СООН
рК 4,7 рК 0,65
Трихлоруксусная к-та во много раз сильнее СН3СООН за счет – I атомов Сl как ЭА.
Муравьиная к-та Н–СООН сильнее СН3СООН за счет +I группы СН3– уксусной к-ты.
д) от характера растворителя.
Если растворитель является хорошим акцептором протонов Н+, то сила
к-ты увеличивается и наоборот.
Основания Бренстеда
5) Они делятся на:
а) p-основания (соединения с кратными связями);
б) n-основания (аммониевые, содержащие атом 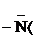 ,
,
оксониевые, содержащие атом 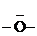 ,
,
сульфониевые, содержащие атом  )
)
Сила основания определяется стабильностью образующегося катиона. Чем стабильнее катион, тем сильнее основание. Другими словами, сила основания тем больше, чем менее прочная связь с гетероатомом (О, S, N), имеющим свободную электронную пару, атакуемую Н+.
Стабильность катиона зависит от тех же факторов, что и стабильность аниона, но с обратным действием. Все факторы, усиливающие кислотность, уменьшают основность.
Самыми сильными основаниями являются амины, т.к. атом азота имеет меньшую ЭО по сравнению с О. При этом вторичные амины более сильные основания, чем первичные, третичные амины слабее вторичных за счет стерического фактора, затрудняющего доступ протона к N.



Ароматические амины более слабые основания, чем алифатические, что объясняется +М группы –NН2. Электронная пара азота, участвуя в сопряжении, становится малоподвижной.
Стабильность сопряженной системы затрудняет присоединение Н+.
В мочевине NН2–СО– NН2 присутствует ЭА группа > С = О, которая значительно снижает оснóвные св-ва и мочевина образует соли только с одним эквивалентом к-ты.
Т.о., чем сильнее к-та, тем слабее образуемое ею основание и наоборот.
Спирты
Это производные УВ, у которых один или несколько атомов Н замещены на –ОН группу.
Классификация:
I. По количеству групп ОН различают одноатомные, двухатомные и многоатомные спирты:
СН3-СН2-ОН 

Этанол Этиленгликоль Глицерин
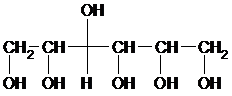
Сорбит
II. По характеру R различают: 1) предельные, 2) непредельные,
3) циклические, 4) ароматические.
2) СН2 = СН-СН2-ОН
Аллиловый спирт
 3) К непредельным циклическим спиртам относятся:
3) К непредельным циклическим спиртам относятся:
ретинол (витамин А) и холестерин

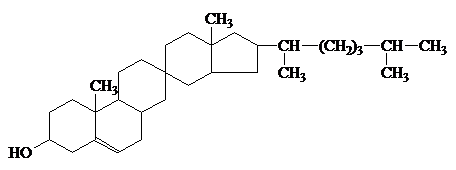 Инозит
Инозит
витаминоподобное в-во
группы В
|
| 4) | 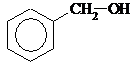 Бензиловый спирт
Бензиловый спирт
|
III. По положению гр. –ОН различают первичные, вторичные и третичные спирты.
IV. По количеству атомов С различают низкомолекулярные и высокомолекулярные.
СН3–(СН2)14 –СН2–ОН (С16Н33ОН) СН3–(СН2)29 –СН2ОН (С31Н63ОН)
Цетиловый спирт Мирициловый спирт
Цетилпальмитат – основа спермацета, мирицилпальмитат содержится в пчелином воске.
Номенклатура:
Тривиальная, рациональная, МН (корень+окончание «ол»+арабская цифра).
Изомерия:
цепи, положения гр. –ОН, оптическая.
Строение молекулы спирта


 СН-кислотный Nu центр
СН-кислотный Nu центр
|
|
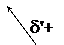 | |||||
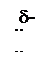 |
| ||||
R ® СН2 ® О Н
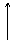 | |||
 | |||
Электрофильный Центр Кислотный
центр основности центр
Р-ции окисления
и Е
1) Спирты – слабые кислоты.
2) Спирты – слабые основания. Присоединяют Н+ лишь от сильных кислот, но они более сильные Nu.
3) –I эффект гр. –ОН увеличивает подвижность Н у соседнего углеродного атома. Углерод приобретает d+ (электрофильный центр, SЕ) и становится центром нуклеофильной атаки (Nu). Связь С–О рвется более легко, чем Н–О, поэтому характерными для спиртов явл-ся р-ции SN. Они, как правило, идут в кислой среде, т.к. протонирование атома кислорода увеличивает d+ атома углерода и облегчает разрыв связи. К этому типу относятся р-ции образования эфиров, галогенопроизводных.
4) Смещение элекронной плотности от Н в радикале приводит к появлению СН-кислотного центра. В этом случае идут р-ции окисления и элиминирования (Е).
Физические св-ва
Низшие спирты (С1–С12) – жидкости, высшие – твердые вещ-ва. Многие св-ва спиртов объясняются образованием Н-связи:

Химические св-ва
I. Кислотно-оснóвные
Cпирты – слабые амфотерные соединения.
2R–ОН + 2Nа ® 2R–ОNа + Н2
Алкоголят
натрия
Алкоголяты легко гидролизуются, что показывает – спирты более слабые кислоты, чем вода:
R– ОNа + НОН ® R–ОН + NаОН
Оснóвный центр в спиртах – гетероатом О:
|
|
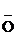 Н +
Н +  Сl- ® [СН3-СН2-
Сl- ® [СН3-СН2- 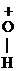 -Н]Сl-
-Н]Сl-
Этилоксонийхлорид
II. Реакции SN по гр. –ОН
Гр. -ОН является плохоуходящей группой (связь мало полярна), поэтому большинство р-ций проводят в кислой среде. Механизм р-ции:
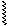
|
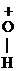 -Н ® СН3-СН2+ + Н2О
-Н ® СН3-СН2+ + Н2О
Если р-ция идет с галогеноводородами, то присоединяться будет галогенид-ион: СН3-СН2+ + Сl- ® СН3-СН2Сl
НС1 RОН R-СООН NН3 С6Н5ОNа
¯ ¯ ¯ ¯ ¯
С1- R-О- R-СОО- NН2- С6Н5О-

Анионы в таких р-циях выступают в качестве нуклеофилов (Nu) за счет «-» заряда или неподеленной электронной пары. Анионы являются более сильными основаниями и нуклеофильными реагентами, чем сами спирты. Поэтому на практике для получения простых и сложных эфиров используются –алкоголяты, а не сами спирты. Если нуклеофилом является другая молекула спирта, то она присоединяется к карбокатиону:
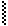
|
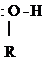 ® СН3-СН2+ -
® СН3-СН2+ - 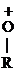 - Н
- Н 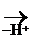 СН3-СН2-О-R
СН3-СН2-О-R
Это р-ция алкилирования (введение алкила R в молекулу).
Заместить –ОН гр. на галоген можно при действии РСl3, РСl5 и SОСl2.
По такому механизму легче реагируют третичные спирты.
Р-цией SЕ по отношению к молекуле спирта является р-ция образования сложных эфиров с органическими и минеральными к-тами:
 R – О Н + Н О –
R – О Н + Н О – 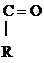
 R – О –
R – О – 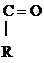 + Н2О
+ Н2О
Сложный эфир
Это р-ция ацилирования – введение ацила в молекулу.
|
 R -
R - 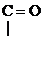
Азотная Сложный
к-та эфир
III. Р-ции Е (отщепления, или элиминирования)
Эти р-ции конкурируют с реакциями SN.

|
|
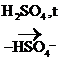 СН3-СН2-
СН3-СН2- 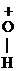 -Н
-Н 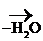 СН3-СН2+
СН3-СН2+
При избытке Н2SО4 и более высокой температуре, чем в случае р-ции образования простых эфиров, идет регенерация катализатора и образуется алкен:
СН3-СН2+ + НSО4- ® СН2 = СН2 + Н2SО4
Легче идет р-ция Е для третичных спиртов, труднее для вторичных и первичных, т.к. в последних случаях образуется менее стабильные катионы. В данных р-циях выполняется правило А. Зайцева: «При дегидратации спиртов атом Н отщепляется от соседнего атома С с меньшим содержанием атомов Н».

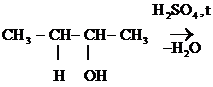 СН3-СН = СН -СН3
СН3-СН = СН -СН3
Бутанол-2
В организме гр. –ОН превращается в легкоуходящую путем образования эфиров с Н3РО4:
|
|
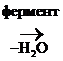 СН3-СН2-ОРО3Н2
СН3-СН2-ОРО3Н2
IV. Р-ции окисления
 1) Первичные и вторичные спирты окисляются СuО, растворами КМnО4, К2Сr2О7 при нагревании с образованием соответствующих карбонилсодержащих соединений:
1) Первичные и вторичные спирты окисляются СuО, растворами КМnО4, К2Сr2О7 при нагревании с образованием соответствующих карбонилсодержащих соединений:


|
|
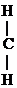 -ОН + О
-ОН + О 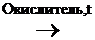 СН3-CH2-
СН3-CH2- 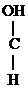 -ОН
-ОН 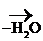 СН3-СН2-
СН3-СН2- 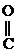 -Н
-Н



|
 - СН3 + О
- СН3 + О 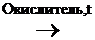 СН3-
СН3- 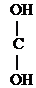 - СН3
- СН3 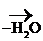 СН3-
СН3- 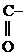 СН3
СН3
Ацетон (кетон)
2) Третичные спирты окисляются с трудом.
К реакциям окисления относятся и р-ции дегидрирования:
|
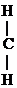 - ОН
- ОН  СН3 -
СН3 - 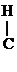 = О + Н2
= О + Н2
Этанол
V. По радикалу (R) протекают р-ции, характерные для соответствующих углеводородов (УВ). В случае предельных – SR, непредельных – АN, ароматических – SЕ:
СН3-СН2-ОН + 3Вr2 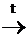 СВr3-СН2-ОН + 3НВr
СВr3-СН2-ОН + 3НВr
Этанол Нарколан
СН2 = СН-СН2-ОН + Вr2 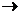 СН2 Вr–СНВr–СН2ОН
СН2 Вr–СНВr–СН2ОН
Аллиловый спирт 2,3-Дибромпропанол

Бензиловый спирт n-Нитрофенилметанол
Многоатомные спирты
Для этих спиртов характерны все р-ции одноатомных спиртов, однако имеется ряд особенностей.
1) За счет – I гр. –ОН многоатомные спирты обладают более выраженными кислотными свойствами. Они образуют алкоголяты не только с щелочными Ме, но и с щелочами:
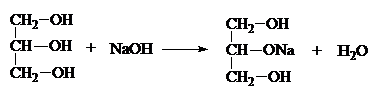
Глицерин
Качественной р-цией на двухатомные и многоатомные спирты (диольный фрагмент) является р-ция с Сu(ОН)2 в щелочной среде:

Глицерин Гликолят меди (II)
или  К2 К2
| 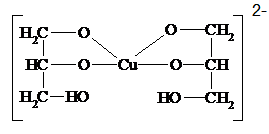
|
Синее окрашивание
Р-ции многоатомных спиртов могут протекать по одной или всем группам –ОН. Они образуют алкоголяты, простые и сложные эфиры, дегидратируются, окисляются.
| 2) | 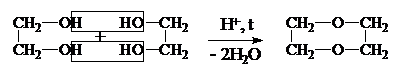
|
Элилен- Диоксан
гликоль (Циклический диэфир)
| 3) | 
|
Нитроглицерин – бесцветная маслянистая жидкость. В виде разбавленных спиртовых растворов (1%) применяется при стенокардии, т.к. оказывает сосудорасширяющее действие. Нитроглицерин – сильное взрывчатое вещество, способное взрываться от удара или при нагревании. При этом в малом объеме, который занимает жидкое вещество, мгновенно образуется очень большой объем газов, что и вызывает сильную взрывную волну. Нитроглицерин входит в состав динамита, пороха.
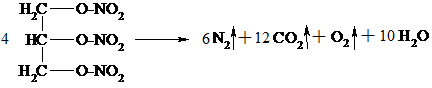
Представители пентитов и гекситов – ксилит и сорбит – соответственно, пяти- и шестиатомные спирты с открытой цепью. Накопление –ОН групп ведет к появлению сладкого вкуса. Ксилит и сорбит – заменители сахара для больных диабетом.
Глицерофосфаты – структурные фрагменты фосфолипидов, применяются как общеукрепляющее средство.
В результате действия Н3РО4 на глицерин получают смесь a- и
b-глицерофосфатов:
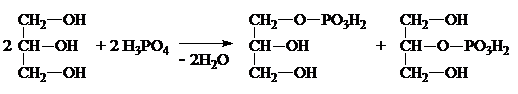
a- b-
Глицерофосфаты
Глицерофосфат железа (III) – при анемии, астении, общем упадке сил. Детям по 0,3 – 0,5 г 2 – 3 раза в день, взрослым по 1 г 3 – 4 раза:
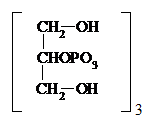
| Fе2+3 × nН2О |
Глицерофосфат кальция – при переутомлении, рахите, упадке питания. Детям по 0,05 – 0,2 г на прием, взрослым 0,2 – 0,5 г.
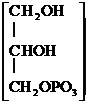 Са × Н2О +
Са × Н2О +  Са × nН2О
Са × nН2О
4) При действии КНSО4 и при нагревании – образуется акролеин:
|
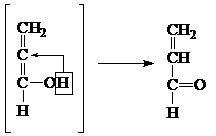
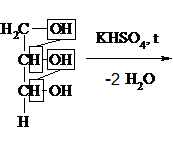
5) При окислении глицерина образуется ряд продуктов. При мягком окислении – глицериновый альдегид (1) и дигидроксиацетон (2):
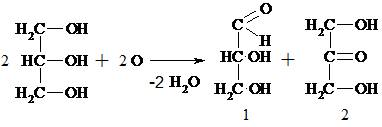
При окислении в жестких условиях образуется 1,3-диоксоацетон.
Химические свойства непредельных спиртов аналогичны предельным, однако за счет двойных или тройных связей они вступают в р-ции присоединения, полимеризации, окисления.
ЛЕКЦИЯ 4
Фенолы
Это производные ароматических УВ, в которых один или несколько атомов Н замещены на –ОН группу.
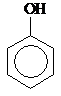
| 
| 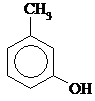
| 
| 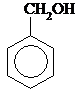
|
 Фенол Фенол
| I-Гидрокси- 2-метилбензол, О-крезол | I-Гидрокси-3-метилбензол, М-крезол | I-Гидрокси-4-метилбензол, n-крезол | Бензиловый спирт |
Изомеры положения
Двухат

Состав сооружений: решетки и песколовки: Решетки – это первое устройство в схеме очистных сооружений. Они представляют...

Двойное оплодотворение у цветковых растений: Оплодотворение - это процесс слияния мужской и женской половых клеток с образованием зиготы...

Типы оградительных сооружений в морском порту: По расположению оградительных сооружений в плане различают волноломы, обе оконечности...

Особенности сооружения опор в сложных условиях: Сооружение ВЛ в районах с суровыми климатическими и тяжелыми геологическими условиями...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!