
Включение углеродных скелетов аминокислот в цикл лимонной кислоты.






Синтез аминокислот
Заменимые аминокислоты образуются в печени из глутаминовой кислоты. Источником всех атомов углерода (а также азота аминогрупп) пролина, орнитина и аргинина является глутамат.
Источником углерода аланина, серина и глицина служат трехуглеродные промежуточные продукты гликолиза, а источником азота их аминогрупп – глутамат; аспартат получает углерод от оксалоацетата, а азот от глутамата.
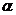 -кетоглутарат + NH3 + НАДН (или НАДФН)
-кетоглутарат + NH3 + НАДН (или НАДФН) 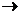 Глутамат + НАД+ (или НАДФ+)
Глутамат + НАД+ (или НАДФ+)
Глутамат + 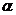 -кетокислота
-кетокислота 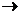
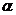 -кетоглутарат + аминокислота
-кетоглутарат + аминокислота
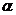 -кетокислота + NH3 + НАДН (НАДФН)
-кетокислота + NH3 + НАДН (НАДФН) 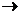 аминокислота + НАД+ (НАДФ+)
аминокислота + НАД+ (НАДФ+)
Восстаниовительное аминирование в печени и других тканях обеспечивает сохраниение и повторное использование аммиака. Большая часть аминокислот синтезируется в результате переноса аминогрупп от других аминокислот без превращения в NH3.
Трансаминирование = переаминирование = аминирование 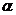 -кетоглутарата.
-кетоглутарата.
Мак-Мюррей, стр.276
Трансаминированию в печени не подвергаются аминокислоты с разветвленной цепью – лейцин, изолейцин, валин.
Эти аминокислоты вступают в реакции трансаминироания в почечной и мышечной тканях.
Лизин и треонин не вступают в реакцию трансаминирования.
Билет 57.
Токсическое действие аммиака-инактивация альфа-кетоглутарата в цикле кребса,энергетическое голодание,к которому чувствителна очень нервная ткань.
Уровень аммиака в норме в крови не превышает 60 мкМоль/литр. Для кроликов концентрация аммиака 3 мМоль/литр является летальной.
В тканях организма происходит отщепление аминогрупп с образованием аммиака. Этот процесс называется дезаминированием. Возможны 4 типа дезаминирования:
1. Восстановительное
R-CH-COOH  R-CH2-COOH + NH3
R-CH2-COOH + NH3
|
NH2
2. Гидролитическое
R-CH-COOH  R-CH-COOH + NH3
R-CH-COOH + NH3
| |
NH2 OH
3. Внутримолекулярное
R-CH2-CH-COOH  R-CH=CH-COOH + NH3
R-CH=CH-COOH + NH3
|
NH2
4. Окислительное
R-CH-COOH  R-C-COOH + NH3
R-C-COOH + NH3
| ||
NH2 O
Окислительное дезаминирование бывает 2 видов: прямое и непрямое (трансдезаминирование).
Прямое окислительное дезаминирование осуществляется оксидазами. В качестве кофермента содержат ФМН или ФАД. Продуктами реакции являются кетокислоты и аммиак.
Трансдезаминирование – основной путь дезаминирования аминокислот. Трансдезаминирование проходит в 2 этапа.
Первый – трансаминирование – перенос аминогруппы с любой аминокислоты на 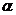 -кетокислоту без промежуточного образования аммиака;
-кетокислоту без промежуточного образования аммиака;
Второй – собственно окислительное дезаминирование.
В результате первого этапа аминогруппы «собираются» в составе глутаминовой кислоты. Второй этап связан с окислительным дезаминированием глутаминовой кислоты.
Трансаминирование аминокислот было открыто советскими учеными Браунштейном и Крицман (1937г).
R R1 R R1
| | | |
HC-NH2 + C=O  C=O + HC-NH2
C=O + HC-NH2
| | | |
COOH COOH COOH COOH
Реакция трансаминирования обратима, она катализируется ферментами – аминотрансферазами.
Акцептором аминогрупп в реакциях трансаминирования являются три 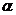 - кетокислоты: пируват, оксалоацетат, 2-оксоглутарат. Наиболее часто акцептором NH2-групп служит 2-оксоглутарат (
- кетокислоты: пируват, оксалоацетат, 2-оксоглутарат. Наиболее часто акцептором NH2-групп служит 2-оксоглутарат (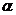 -кетоглутарат), реакция приводит к образованию глутаминовой кислоты:
-кетоглутарат), реакция приводит к образованию глутаминовой кислоты:
1. СН3 COOH CH3 COOH
| | АЛТ | |
НСNH2 + CH2  C=O + (CH2)2
C=O + (CH2)2
| | | |
COOH CH2 COOH CHNH2
| |
C=O COOH
| глутамат
COOH
Аминотрансферазы содержат в качестве кофермента производные пиридоксина (витамин В6) – пиридоксаль-фосфат и пиридоксамин-фосфат.
(Механизм реакции трансаминирования с участием пиридоксальфосфата – учебник.)
2. Окислительное дезаминирование глутаминовой кислоты.
Биологический смысл реакций трансаминирования состоит в том, чтобы собрать аминогрупы всех распадающихся аминокислот в составе одной аминокислоты – глутаминовой. Глутаминовая кислота поступает в митохондрии клеток, где происходит второй этап трансдезаминирования – собственно дезаминирование глутаминовой кислоты. Реакция катализируется глутаматдегидрогеназой, которая в качестве кофермента содержит НАД+ или НАДФ+.
COOH СООН
| |
 (CH2)2
(CH2)2 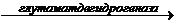 (CH2)2
(CH2)2
| |
CHNH2 НАД НАДН+Н+ C=O
| |
COOH COOH
Клиническое значение определения активности трансаминаз.
Для клинических целей определяют активность АлТ и АсТ, которые катализируют следующие реакции:
Аспартат + 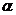 -кетоглутарат
-кетоглутарат  оксалоацетат + глутамат
оксалоацетат + глутамат
Аланин + 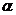 -кетоглутарат
-кетоглутарат  пируват + глутамат
пируват + глутамат
В сыворотке крови здоровых людей активность этих трансаминаз ниже, чем в органах. При поражении органов наблюдается выход трансаминаз из очага поражения в кровь. Так, при инфаркте миокарда уровень АсТ сыворотки крови уже через 3-5 ч после наступления инфаркта повышается в 20-30 раз. При гепатитах повышается более умеренное и затяжное.
В организме биогенные амины подвергаются реакции окислительного дезаминирования с образованием альдегидов и аммиака. Процесс осуществляется при участии моноаминооксидаз.
Схематически механизм трансдезаминирования можно представит так:

Билет 58
Трансдезаминирование – основной путь дезаминирования аминокислот. Трансдезаминирование проходит в 2 этапа.
Первый – трансаминирование – перенос аминогруппы с любой аминокислоты на 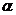 -кетокислоту без промежуточного образования аммиака;
-кетокислоту без промежуточного образования аммиака;
Второй – собственно окислительное дезаминирование.
В результате первого этапа аминогруппы «собираются» в составе глутаминовой кислоты. Второй этап связан с окислительным дезаминированием глутаминовой кислоты.
Трансаминирование аминокислот было открыто советскими учеными Браунштейном и Крицман (1937г).
R R1 R R1
| | | |
HC-NH2 + C=O  C=O + HC-NH2
C=O + HC-NH2
| | | |
COOH COOH COOH COOH
Реакция трансаминирования обратима, она катализируется ферментами – аминотрансферазами.
Акцептором аминогрупп в реакциях трансаминирования являются три 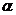 - кетокислоты: пируват, оксалоацетат, 2-оксоглутарат. Наиболее часто акцептором NH2-групп служит 2-оксоглутарат (
- кетокислоты: пируват, оксалоацетат, 2-оксоглутарат. Наиболее часто акцептором NH2-групп служит 2-оксоглутарат (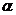 -кетоглутарат), реакция приводит к образованию глутаминовой кислоты:
-кетоглутарат), реакция приводит к образованию глутаминовой кислоты:
3. СН3 COOH CH3 COOH
| | АЛТ | |
НСNH2 + CH2  C=O + (CH2)2
C=O + (CH2)2
| | | |
COOH CH2 COOH CHNH2
| |
C=O COOH
| глутамат
COOH
Аминотрансферазы содержат в качестве кофермента производные пиридоксина (витамин В6) – пиридоксаль-фосфат и пиридоксамин-фосфат.
(Механизм реакции трансаминирования с участием пиридоксальфосфата – учебник.)
4. Окислительное дезаминирование глутаминовой кислоты.
Биологический смысл реакций трансаминирования состоит в том, чтобы собрать аминогрупы всех распадающихся аминокислот в составе одной аминокислоты – глутаминовой. Глутаминовая кислота поступает в митохондрии клеток, где происходит второй этап трансдезаминирования – собственно дезаминирование глутаминовой кислоты. Реакция катализируется глутаматдегидрогеназой, которая в качестве кофермента содержит НАД+ или НАДФ+.
COOH СООН
| |
 (CH2)2
(CH2)2 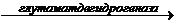 (CH2)2
(CH2)2
| |
CHNH2 НАД НАДН+Н+ C=O
| |
COOH COOH
Клиническое значение определения активности трансаминаз.
Для клинических целей определяют активность АлТ и АсТ, которые катализируют следующие реакции:
Аспартат + 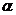 -кетоглутарат
-кетоглутарат  оксалоацетат + глутамат
оксалоацетат + глутамат
Аланин + 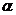 -кетоглутарат
-кетоглутарат  пируват + глутамат
пируват + глутамат
В сыворотке крови здоровых людей активность этих трансаминаз ниже, чем в органах. При поражении органов наблюдается выход трансаминаз из очага поражения в кровь. Так, при инфаркте миокарда уровень АсТ сыворотки крови уже через 3-5 ч после наступления инфаркта повышается в 20-30 раз. При гепатитах повышается более умеренное и затяжное.
Билет 59.




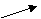






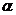 -кетоглутарат + NH3 + НАДН (или НАДФН)
-кетоглутарат + NH3 + НАДН (или НАДФН) 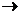 Глутамат + НАД+ (или НАДФ+)
Глутамат + НАД+ (или НАДФ+) R-CH2-COOH + NH3
R-CH2-COOH + NH3 R-CH-COOH + NH3
R-CH-COOH + NH3 R-CH=CH-COOH + NH3
R-CH=CH-COOH + NH3 R-C-COOH + NH3
R-C-COOH + NH3 C=O + HC-NH2
C=O + HC-NH2 (CH2)2
(CH2)2 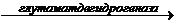 (CH2)2
(CH2)2
 (CH2)2
(CH2)2 


