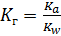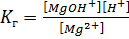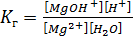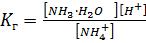I:
S: Водородный показатель вычисляется по формуле
-: рН = -lg[OH-]
-:pH=-lg[H+]
-: pH=lg[OH-]
-: pH =lg[H+]
I:
S: Гидроксильный показатель вычисляется по формуле
-:рOН = -lg[OH-]
-: pOH=-lg[H+]
-: pOH=lg[OH-]
-: pOH =lg[H+]
I:
S: Среднее значение рН плазмы крови 7,4.Концентрация катионов водорода в таком растворе
-: 3,98∙10-8моль/л
-: 4,02∙10-7 моль/л
-: 3,5∙10-6моль/л
-: 8.7∙10-5моль/л
I;
S: Среднее значение рН желудочного сока 1,7.Концентрация катионов водорода в таком растворе
-: 0,02 моль/л
-: 0,078 моль/л
-: 3,5∙10-2моль/л
-: 8.7∙10-3моль/л
I:
S: Среднее значение рН желудочного сока 1,7.Показатель гидроксильной группы рОHдля желудочного сока равен
-: 12,3
-: 1,78
-: 11,5
-: 10,3
I:
S: Среднее значение рН плазмы крови 7,4.рОHдля плазмы крови равен:
-: 8,3
-:6,6
-: 7,5
-: 2
I:
S: Вычислите концентрацию катионов водорода в желудочном соке, если массовая доля соляной кислоты в нем составляет 0,5%. Плотность желудочного сока принять 1 г/мл. Коэффициент активности ионов водородапринять равным единице.
-: 0.25 моль/л
-: 0.137 моль/л
-: 0.38 моль/л
-: 0.56 моль/л
I:
S: При комнатной температуре для любых водных растворов сумма рН+рОН
-: 16
-: 14
-: 15
-: 17
I:
S: При 37 °С для любого водного раствора (в том числе биологических жидкостей) сумма рН+рОН=13,94. Значение рН для нейтральной среды равно
-: 7,0
-: 6,97
-: 8,54
-: 7,56
I:
S: Показатель гидроксид-ионов в растворе NaOHпри комнатной температуре равен 2. рН раствора щелочи равен
-: 10
-: 12
-: 11
-: 13
I:
S: Водородный показатель рН желудочного сока 1,5. Гидроксильный показатель желудочного сока равен
-: 13,5
-: 12.5
-: 10
-: 9,5
I:
S: Концентрация катионов водорода в плазме крови равна 1,58∙10-7 М.
Концентрация гидроксид-ионов в этом образце плазмы крови при комнатной температуре
-: 6,39∙10-7M
-: 6,39∙10-8M
-: 7,0∙10-7M
- 1,1∙10-9М
V2: Гидролиз солей
I:
S: Какие из солей подвергаются гидролизу по аниону?
А. КСlO Б. СаСl2 В. FeCl3 Г. КNO2Д. КNO3
-: АБ
-:АГ
-: ГД
-: БВ
I:
S: Какие из солей подвергаются гидролизу по катиону?
А. КСlOБ. СаСl2В. FeCl3 Г. КNO2Д. Cu(NO3)2
-: АБ
-:ВД
-: ГД
-: БВ
I:
S: Какие из солей подвергаются гидролизу по катиону и аниону?
А. КСlOБ. NH4FВ. FeCl3 Г. КNO2Д. Al(CH3COO)3
-: АБ
-:БД
-: ГД
-: БВ
I:
S: Какие из солей гидролизуне подвергаются?
А. КСlO4Б. NH4FВ. FeCl3 Г. КNO3Д. Al(CH3COO)3
-: АБ
-:АГ
-: ГД
-: БВ
I:
S: Какие из солей в водном растворе создают рН>7?
А. КСlO Б. СаСl2 В. FeCl3 Г. КNO2Д. КNO3
-: АБ
-:АГ
-: ГД
-: БВ
I:
S: Какие из солей в водном растворе создают рН<7
А. КСlOБ. СаСl2В. FeCl3 Г. КNO2Д. Cu(NO3)2
-: АБ
-:ВД
-: ГВ
-:AГ
I:
S: В воде растворили сульфид калия. Выберите правильнуюсхему гидролиза этой соли по первой ступени в ионном виде
-: НS-+H2O ↔H2S+OH-
-:S-2 +H2O ↔HS- +OH-
-: S-2 +H2O ↔H2S+2OH-
-: НS- +H3O+↔Н2S+H2O
I:
S: В воде растворили сульфид калия. Выберите правильную схему гидролиза этой соли по второй ступени в ионном виде
-:НS-+H2O ↔H2S+OH-
-: S-2 +H2O ↔HS- +OH-
-: S-2 +H2O ↔H2S+2OH-
-: НS- +H3O+↔Н2S+H2O
I:
S: В воде растворили хлорид цинка. Выберите правильную схему гидролиза соли по первой ступени
-: ZnOH++H2O ↔Zn(OH)2+H+
-:Zn2+-+H2O ↔ZnOH++H+
-: Zn(OH)2 +2H3O+ ↔Zn2++4H2O
-: Zn2++4H2O ↔Zn(OH)2 +2H3O+
I:
S:Выберите правильный ответ. Выражение для константы гидролизахлорида магния по первой ступени имеет вид:
-: 
-: 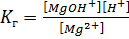
-: 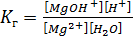
I:
S: Выберите правильный ответ. Выражение для константы гидролиза нитрата аммония имеет вид:
-: 
-: 
-: 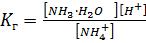
-: 
I:
S: Численное значение константы гидролиза для солей, образованных сильными кислотами и слабымиоднокислотными основаниями, вычисляется по формуле:
-: 
-: 
-: 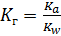
-: 
I:
S: Численное значение константы гидролиза для солей, образованных сильными кислотами и слабыми однокислотными основаниями, вычисляется по формуле:
-: 
-: 
-: 
-: 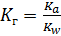
I:
S: Численное значение константы гидролиза для солей, образованных слабыми одноосновными кислотами и сильными основаниями, вычисляется по формуле:
-: 
-: 
-: 
-: