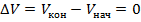Рассмотрим газ, находящийся под поршнем и в цилиндре.
 Если газ, расширяясь, передвигает поршень на бесконечно малое расстояние
Если газ, расширяясь, передвигает поршень на бесконечно малое расстояние  , то газ производит над поршнем работу.
, то газ производит над поршнем работу.

где S - площадь поршня. 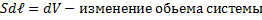

 Полная работа А, совершаемая газом при изменению объема от V1 до V2 равная
Полная работа А, совершаемая газом при изменению объема от V1 до V2 равная

- работа для любого процесса
3 Ср, CV и связь между ними (уравнения Майера)
Запишем выражения I начала термодинамики для 1 моля газа
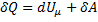



Если газ нагревается при постоянном объеме (V = const, dV = 0), то А = 0, и, сообщаемая газу теплота, идет только на увеличения его внутренней энергии


то есть молярная теплоемкость газа при постоянном объеме CV равна изменению внутренней энергии 1 моля газа при повешении температуры на 1К.
Т.к.
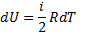

Если газ нагревается при постоянном давление p = const

так как  не зависят от вида процесса (внутренняя энергия не зависит от р и V, а определяется лишь температурой Т) и
не зависят от вида процесса (внутренняя энергия не зависит от р и V, а определяется лишь температурой Т) и 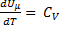
Из уравнения Менделеева-Клапейронаpv=RT
p 
 - уравнение Майера
- уравнение Майера
Уравнение Майера показывает, что Ср всегда больше Cv на величину универсальной газовой постоянной R,так как при p = const требуется дополнительное количество теплоты на совершение работы расширения газа, так как постоянство давления обеспечивается увеличениям объема газа


Величина

представляет характерную для каждого газа величину. Для одноатомных газов  , для двухатомных - 7/5, для трехатомных – 4/3.
, для двухатомных - 7/5, для трехатомных – 4/3.
I начало термодинамики,
Q, U, A для изопроцессов
- Изотермический процесс Т = const, m =const
Закон Бойля-Мариотта
 =const
=const 
a)A= 


б) 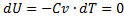
 =0
=0
в) 

т.е. все количество теплоты, сообщаемое газу, расходуется на совершение им работы против внешних сил

чтобы при работе расширения температура не изменялась, к газу в течение изобарного процесса необходимо подводить количество теплоты, эквивалентное внешней работе расширения.
- Изобарический процесс. p=const m=const
- A=
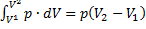

 Из уравнения Менделеева-Клапейрона для состояния 1 и 2:
Из уравнения Менделеева-Клапейрона для состояния 1 и 2:




Физический смысл R: R численно равна работе при нагревании 1 моля газа на 1К (T2 - T1 = 1 K) при изобарическом процессе.
б) 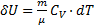
в) 

Q= 
тепло, подведенное к газу, идет на изменение его внутренней энергии и совершение работы.
3.Изохорический процесс. V = const, m = const.


и
 ,
,
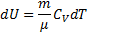
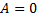



Вся теплота, сообщаемая газу, идет на изменение его внутренней энергии.
Адиабатический процесс.
Политропный процесс
Адиабатическим называется процесс, протекающий без теплообмена с внешней средой. К адиабатическим можно отнести все быстропротекающие процессы. Например, адиабатным процессом можно считать процесс распространения звука в среде, т.к. скорость распространения звука настолько велика, что обмен энергией между волной и средой произойти не успевает. Адиабатические процессы применяются в двигателях внутреннего сгорания, холодильных установках и др.
Найдем уравнение, связывающее параметры идеального газа при адиабатном процессе.
Запишем I начало термодинамики.

Для адиабатического процесса

т.е. внешняя работа совершается за счет изменения внутренней энергии системы.



Из уравнения Менделеева-Клапейрона выразим р:



Перепишем в виде:

т.е

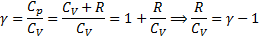
Пропотенцировав


- уравнение адиабаты в координатах Т и V.

Уравнение Пуассона (уравнение адиабаты в координатах р и V):

 -показатель адиабаты (или коэффициент Пуассона).
-показатель адиабаты (или коэффициент Пуассона).
 pV = const - уравнение изотермы, т.к. γ > 1, то адиабата идет круче, чем изотерма. Это объясняется тем, что при адиабатическом сжатии 1-3 увеличение давления газа обусловлено не только уменьшением его объема, как при изотермическом сжатии, но и повышением температуры
pV = const - уравнение изотермы, т.к. γ > 1, то адиабата идет круче, чем изотерма. Это объясняется тем, что при адиабатическом сжатии 1-3 увеличение давления газа обусловлено не только уменьшением его объема, как при изотермическом сжатии, но и повышением температуры



- уравнение адиабаты в координатах p, T.
Вычислим работу совершаемую газом в адиабатическом процессе.
I начало термодинамики для адиабатического процесса
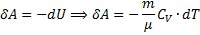
Если газ адиабатически расширяется от объема V1 до V2, то его температура уменьшается от Т1 до Т2 и работа расширения идеального газа







Работа, совершаемая газом при адиабатическом расширении 1-2 равна площади, заштрихованной на рисунке и она меньше, чем работа при изотермическом расширении. Это объясняется тем, что при адиабатическом расширении происходит охлаждение газа, тогда как при изотермическом расширении температура поддерживается постоянной за счет притока извне эквивалентного количества теплоты.
Рассмотренные изохорический, изобарический, изотермический и адиабатический процессы имеют общую особенность – они протекают при постоянной теплоемкости (CV, CP, CT= ∞, CA=0). В первых двух процессах теплоемкости соответственно равны Сv и Cр в изотермическом процессе (dT = 0) СT = ∞, в адиабатическом процессе δQ = 0 и CA=0.
Процесс, в котором теплоемкость остается постоянной называется политропным (C = const).
Исходя из I начала термодинамики при условии постоянства теплоемкости (C = const) можно вывести уравнения политропы


n – показатель адиабаты.
При С = 0 n = γ pvγ=const -уравнения адиабаты
При С = ∞ n = 1 pV = const – уравнение изотермы
При С = Ср n = 0 p = const, 
 -уравнение изобары
-уравнение изобары
При С = СV n = ± ∞ 
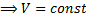
т.о., все рассмотренные процессы являются частными случаями политропного процесса.
Работа газа при адиабатическом процессе
Из первого начала термодинамики ( ) для адиабатического процесса (
) для адиабатического процесса ( ) следует, что
) следует, что  .
.
Если газ адиабатически расширяется от объема V 1 до объема V 2, то его температура уменьшается от T 1 до T 2 и работа расширения идеального газа:
 .
.
Используя уравнение адиабатического процесса в переменных V и Т, то есть 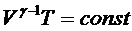 полученное выражение для работы А при адиабатическом расширении газа можно преобразовать к иному виду, отражающему адиабатическое изменение объема газа от величины V 1 до величины V 2 :
полученное выражение для работы А при адиабатическом расширении газа можно преобразовать к иному виду, отражающему адиабатическое изменение объема газа от величины V 1 до величины V 2 :
 .
.
Адиабатный процесс. Изопроцессы в термодинамике
На этом уроке мы будем работать с уже известными нам физическими понятиями, но в несколько иной области применения. А именно с изопроцессами в термодинамике. Мы рассмотрим, какие изменения в первый закон термодинамики (закон сохранения энергии в тепловых процессах) внесут протекания этих самых процессов при неизменном макроскопическом параметре газа. Также мы рассмотрим новый, ранее неизвестный процесс – адиабатный.
В ходе изучения темы «Основы молекулярно-кинетической теории» нами были рассмотрены так называемые изопроцессы, то есть процессы, протекающие при неизменном одном из макроскопических параметров(давлении, объёме или температуре). При подстановке этих данных в уравнение Клапейрона эти условия несколько видоизменяли его. Теперь же мы проделаем схожий анализ, но уже с первым законом термодинамики:

Рассмотрим случай протекания процесса при неизменной температуре:
Так как:

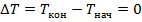
Следовательно:

А, значит, первый закон термодинамики приобретает вид:

Рассмотрев случай для выполнения над газом внешними силами положительной работы:


То есть, при изотермическом сжатии или расширении газ выделяет теплоту в окружающую среду.
Рассмотрим случай, когда процесс протекает при постоянном давлении:
Так как ни в одну термодинамическую величину не входит множитель  , то никакое слагаемое первого закона термодинамики не обнуляется, и он сохраняет свой прежний вид:
, то никакое слагаемое первого закона термодинамики не обнуляется, и он сохраняет свой прежний вид:

Теперь рассмотрим, какие изменения произойдут в записи первого закона термодинамики, если процесс происходит в фиксированном объёме.
Так как:

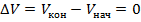
Следовательно:

А значит, первый закон термодинамики приобретает вид:

То есть теряется смысл использования изохорных процессов в тепловых двигателях, ведь вся энергия сгораемого топлива пойдёт на изменение внутренней энергии, и газ не будет совершать полезной работы.
Существует также ещё один очень важный процесс – адиабатный.
Определение. Адиабатный процесс – процесс, протекающий в теплоизолированной системе. То есть без подвода газу или выделения газом теплоты.
Так как:

Первый закон термодинамики приобретает вид:

Или


То есть в результате выполнения над газом работы внешними силами его внутренняя энергия, а следовательно, и температура увеличивается, а при выполнении работы газом – уменьшается.
Наглядными примерами последних двух утверждений являются следующие опыты.
1. В закрытом подвижным поршнем цилиндре находится небольшое количество топлива. После быстрого нажатия на поршень топливо воспламеняется.
2. В закрытом пробкой с продетым шлангом насоса сосуде находится небольшое количество воды. После нагнетания в сосуд определенно количества воздуха, пробка быстро вылетает и в сосуде наблюдается туман (рис. 1).


Рис. 1. Наглядные примеры адиабатных процессов (Источник)
В двух случаях газ выполняет разные по знаку работы, и, следовательно, изменение внутренней энергии и температуры имеет разные знаки. В обоих случаях делается акцент на быстром изменении объёма потому, что невозможно создать идеально изолированную систему, но если рассматривать очень скоротечный процесс, то тепло не успеет передаться, и процесс можно считать адиабатным.
График адиабатных процессов в координатах P-V выглядит следующим образом (рис. 2).

Рис. 2. График адиабатного процесса (Источник)
Начиная со следующего урока, мы переходим к изучению нового раздела физики – электростатики.



 Если газ, расширяясь, передвигает поршень на бесконечно малое расстояние
Если газ, расширяясь, передвигает поршень на бесконечно малое расстояние  , то газ производит над поршнем работу.
, то газ производит над поршнем работу.
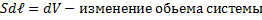

 Полная работа А, совершаемая газом при изменению объема от V1 до V2 равная
Полная работа А, совершаемая газом при изменению объема от V1 до V2 равная
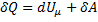





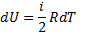


 не зависят от вида процесса (внутренняя энергия не зависит от р и V, а определяется лишь температурой Т) и
не зависят от вида процесса (внутренняя энергия не зависит от р и V, а определяется лишь температурой Т) и 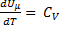

 - уравнение Майера
- уравнение Майера


 , для двухатомных - 7/5, для трехатомных – 4/3.
, для двухатомных - 7/5, для трехатомных – 4/3. =const
=const 



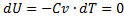
 =0
=0


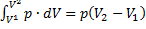

 Из уравнения Менделеева-Клапейрона для состояния 1 и 2:
Из уравнения Менделеева-Клапейрона для состояния 1 и 2:



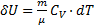




 ,
,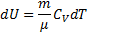
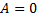












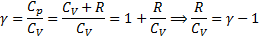




 -показатель адиабаты (или коэффициент Пуассона).
-показатель адиабаты (или коэффициент Пуассона). pV = const - уравнение изотермы, т.к. γ > 1, то адиабата идет круче, чем изотерма. Это объясняется тем, что при адиабатическом сжатии 1-3 увеличение давления газа обусловлено не только уменьшением его объема, как при изотермическом сжатии, но и повышением температуры
pV = const - уравнение изотермы, т.к. γ > 1, то адиабата идет круче, чем изотерма. Это объясняется тем, что при адиабатическом сжатии 1-3 увеличение давления газа обусловлено не только уменьшением его объема, как при изотермическом сжатии, но и повышением температуры


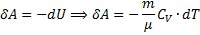










 -уравнение изобары
-уравнение изобары
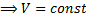
 ) для адиабатического процесса (
) для адиабатического процесса ( ) следует, что
) следует, что  .
. .
.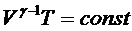 полученное выражение для работы А при адиабатическом расширении газа можно преобразовать к иному виду, отражающему адиабатическое изменение объема газа от величины V 1 до величины V 2 :
полученное выражение для работы А при адиабатическом расширении газа можно преобразовать к иному виду, отражающему адиабатическое изменение объема газа от величины V 1 до величины V 2 : .
.

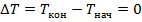




 , то никакое слагаемое первого закона термодинамики не обнуляется, и он сохраняет свой прежний вид:
, то никакое слагаемое первого закона термодинамики не обнуляется, и он сохраняет свой прежний вид: