ЛЕКЦИИ ПО ДИСЦИПЛИНЕ «МАТЕРИАЛОВЕДЕНИЕ»
Материаловедение - это наука, изучающая связь между составом, строением и свойствами материалов, а так же закономерности их изменения под влиянием механических, физико-химических и других видов воздействий (тепловых, электромагнитных, радиоактивных, химических и др.).
Курс материаловедения состоит из двух основных частей:
1. Металловедение и термическая обработка металлов.
2. Неметаллические материалы (пластмассы, древесина, резина, стекло, керамика, асбест и др.).
Раздел 1. Металловедение и термическая обработка
Тема 1.1. Кристаллическое строение металлов
Металловедение - это наука, изучающая строение и свойства металлов и сплавов, устанавливающая связь между их составом, строением, свойствами и разрабатывающая пути воздействия на их свойства.
1.1.1 Общая характеристика, классификация металлов и конструкционных материалов
Основными характерными свойствами металлов являются:
1) металлический блеск;
2) непрозрачность;
3) вязкость;
4) пластичность;
5) теплопроводность;
6) электропроводность;
7) кристаллическое строение.
Существует общепринятая классификация, согласно которой все металлы подразделяются на две большие группы – черные и цветные. К черным относят – железо и сплавы на его основе, а к цветным все остальные металлы и их сплавы.
Однако каждый металл отличается строением и свойствами от другого, и по некоторым признакам их можно объединить в группы. Такая классификация дана русским металловедом А.П. Гуляевым.
Классификация металлов ( А.П. Гуляева)
Атомно-кристаллическое строение металлов
Вещества в твердом состоянии имеют кристаллическое или аморфное строение.
Кристаллическое строение имеют большинство минералов, а так же всеметаллы и сплавы.
Свойства кристаллических тел (металлов и сплавов):
1) атомы металлов располагаются в строго определенном порядке;
2) имеют определенную температуру плавления;
3) монокристаллы металлов анизотропы (их свойства зависят от направления); поликристаллы изотропны (их свойства не зависят от направления).
Аморфное строение имеют: смола, кварцевое стекло, битум, янтарь.
Свойства аморфных тел:
1) атомы располагаются хаотически (беспорядочно);
2) не имеют определенной температуры плавления; при нагревании аморфные вещества размягчаются и переходят в жидкое состояние в широком диапазоне температур;
3) аморфные тела анизотропны (их свойства зависят от направления).
Атомы (ионы) в металле располагаются закономерно, образуя правильную кристаллическую решетку, что соответствует минимальной энергии взаимодействия атомов.
Кристаллическая решетка изображается с помощью элементарной кристаллической ячейки.
Элементарная кристаллическая ячейка - это минимальное число атомов, при многократном повторении которого воспроизводится вся решетка металла в целом.
Элементарная кристаллическая ячейка - это наименьший объем кристалла, дающий представление об атомной структуре всего металла.
Металлы имеют кристаллические решетки различных типов. Чаще всего встречаются кристаллические решетки трех типов:

1. Объемно-центрированная кубическая (ОЦК)
Такую решетку имеют: альфа-железо (α-Fe), хром Cr, бетта-титан (β-Ti), вольфрам W, ванадий Va, молибден Mo.
2. Гранецентрированная кубическая (ГЦК)
Такую решетку имеют: гамма-железо (ϒ-Fe), медь Cu, алюминий Al, золото Au, серебро Ag, никель Ni.
3. Гексогональная плотноупакованная (ГПУ)
Такую решетку имеют: магний Mg, альфа-титан (α-Ti), цинк Zn, кобальт Co, кадмий Cd.
Точечное расположение атомов в кристаллической решетке является условным, так как в действительности атомы имеют определенный размер и могут соприкасаться друг с другом.
Металлическая связь
Металл представляет собой совокупность закономерно расположенных в кристалле положительно заряженных ионов, окруженных отрицательно заряженными частицами-электронами, слабо связанными с ядром. Эти коллективизированные (общие) электроны непрерывно перемещаются внутри металла, при этом образуя «электронный газ». Между ионами и коллективизированными электронами проводимости возникают электростатические силы притяжения, которые стягивают ионы, компенсируя силу отталкивания. Такая связь называется металлической связью.
Хотя в узлах кристаллической решетки располагаются ионы, между которыми движутся электроны, но обычно говорят не ионы, а атомы.
Анизотропия
Вследствие того, что расстояние между атомами в кристаллической решетке в разных направлениях различно, многие свойства (химические, физические, механические и др.) кристалла зависят от направления.
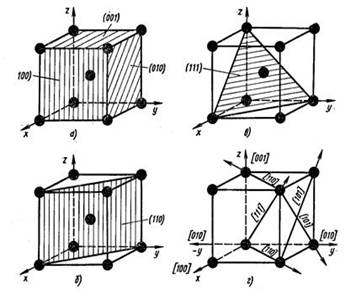 Подобная неодинаковость свойств монокристалла в различных кристаллографических направлениях называется анизотропией.
Подобная неодинаковость свойств монокристалла в различных кристаллографических направлениях называется анизотропией.
Технические металлы являются поликристаллами и состоят из большого количества анизотропных кристаллов. Произвольность ориентировки каждого кристалла приводит к тому, что свойства поликристалла во всех направлениях более или менее одинаковы.
Поэтому поликристаллическое тело можно считать изотропным.
Схема кристаллизации


Пока образовавшиеся кристаллы растут свободно, они могут иметь правильную геометрическую форму, но при столкновении растущих кристаллов, их правильная форма нарушается. В результате после затвердевания кристаллы приобретают неправильную форму. Кристаллы неправильной формы называют зёрнами или кристаллитами.
Выводы по схеме кристаллизации:
1. Величина зерна зависит от числа центров кристаллизации (зародышей), чем больше центров кристаллизации, тем размеры зерна будут меньше.
2. Величина зерна зависит от скорости роста зародышей (от скорости охлаждения), чем больше скорость охлаждения, тем мельче будет конечное зерно.
3. На образование центров кристаллизации влияет степень переохлаждения.
Чем больше степень переохлаждения, тем больше центров кристаллизации и тем меньше размер зерна.
В процессе кристаллизации возникают зародыши разного размера, однако не все они способны к росту. Минимальный размер зародыша, способного к росту при данной температуре называется критическим (Rкр). Зародыши, размером меньше Rкр расти не могут и растворяются в жидком металле. Если возникают зародыши размером больше или равным Rкр, то они устойчивы и способны к росту.
Строение металлического кристалла
Кристаллы, образующиеся в процессе затвердевания металла, в зависимости от скорости охлаждения, характера и количества примесей, могут иметь различную форму. Чаще в процессе кристаллизации образуются разветвленные или древовидные кристаллы, получившие название дендритов.

 При образовании кристалла первоначально образуются длинные ветви-оси 1го порядка (главные оси дендрита). На их ребрах происходит зарождение и рост перпендикулярных к ним таких же ветвей 2-го порядка, на этих осях зарождаются и растут оси 3-го порядка.
При образовании кристалла первоначально образуются длинные ветви-оси 1го порядка (главные оси дендрита). На их ребрах происходит зарождение и рост перпендикулярных к ним таких же ветвей 2-го порядка, на этих осях зарождаются и растут оси 3-го порядка.
Полиморфные превращения
Полиморфизмом или аллотропией называется способность металла существовать в различных кристаллических формах в зависимости от температуры.
Полиморфизм - это способность металла при изменении температуры перестраивать свою кристаллическую решетку.
Различные кристаллические формы одного металла называют полиморфными модификациями. Они обозначаются буквами греческого алфавита α, β, ϒ, δ.
В результате полиморфного превращения атомы кристаллического тела, имеющие решетку одного типа, перестраиваются таким образом, что получается кристаллическая решетка другого типа. Полиморфную модификацию, устойчивую при более низкой температуре, принято обозначать буквой альфа, для большинства металлов.
Полиморфные превращения протекают благодаря переходу кристаллического вещества (металла) в состояние с меньшей свободной энергией. Полиморфные превращения осуществляются образованием зародышей и последующим их ростом в результате перехода атомов из старой модификации в новую.
Строение сплавов
Сплавом называется вещество, полученное сплавлением или спеканием двух и более элементов.
Вещества, из которых состоят сплавы, называются - компонентами.
Сплавы могут быть 2-х компонентные, 3-х компонентные, многокомпонентные.
Твёрдые растворы
Твердый раствор - это фаза, в которой одни из компонентов сплава сохраняет свою кристаллическую решётку и атомы другого компонента располагаются в кристаллической решётке первого компонента, изменяя её размеры.
Твёрдый раствор характеризуется тем, что:
1. Представляет собой одну фазу;
2. Имеет один тип решётки (рентгеновский анализ покажет решётку растворителя).
3. Концентрация твёрдого раствора непостоянна, она зависит от температуры, чем выше температура, тем выше концентрация.
Различают твёрдые растворы замещения и твердые растворы внедрения:
1. При образовании твёрдого раствора замещения атомы растворяемого компонента замещают часть атомов растворителя (основного металла) в его кристаллической решётке.
2. При образовании твёрдого раствора внедрения атомы растворимого компонента располагаются (междоузлия) пустотах решётки растворителя (основного металла).
Твердые растворы замещения
Твердый раствор замещения – это фаза, в которойатомы растворяемого компонента замещают часть атомов растворителя (основного металла) в его кристаллической решётке.

При образовании твёрдого раствора замещения периоды решётки могут увеличиваться, могут уменьшаться в зависимости от соотношения атомных радиусов, атомов растворителя и растворяемого элемента.
В случае твёрдого раствора внедрения периоды решётки могут только увеличиваться.
В металловедении принято обозначать твёрдые растворы буквами греческого алфавита (α, β, ϒ, δ и т.д.)
Когда компоненты могут замещать один другого в кристаллической решётке в любых количественных соотношениях, то образуются твердые растворы замещения неограниченной растворимости.
Твёрдые растворы замещения неограниченной растворимости могут образовываться при условиях:
1. Компоненты должны обладать одинаковыми по типу кристаллическими решётками.
2. Различия в размерах атомов (ионов) компонентов не должны быть большими не более 9-15%.
3. Компоненты должны принадлежать к одной и той же группе периодической системы элементов или к смежным, родственным группам.
Твердые растворы внедрения
3. Твёрдый раствор внедрения – это фаза, в которой атомы растворимого компонента располагаются (междоузлия) пустотах решётки растворителя (основного металла).
Твёрдые растворы внедрения могут возникнуть только в тех случаях, когда диаметр атома растворимого элемента невелик, поэтому твёрдые растворы внедрения образуются лишь при растворении в металле (например: в железе, молибдене, хроме и т.д.) углерода, азота, водорода, т.е. элементов с малым атомным радиусом.
В случае твёрдого раствора внедрения периоды решётки могут только увеличиваться.
Твёрдые растворы внедрения могут быть только ограниченной растворимости, поскольку число пор в решётке ограниченно, а атомы основного компонента сохраняются в узлах решётки.
Например, железо способно растворить углерод, в железоуглеродистых сплавах (сталях и чугунах) образуются два твердых раствора внедрения феррит и аустенит.
.
Феррит - это твёрдый раствор внедрения углерода в α-железе (Ф).
α-железо максимально может растворять 0,025%С углерода при температуре 727 ° С;
α-железо минимально может растворять 0,006%С углерода при температуре 0 ° С.
Аустенит - это твёрдый раствор внедрения углерода в гамма-железе.(А)
ϒ-железо максимально может растворять до 2,14% С углерода при температуре 1147 ° С;
ϒ-железо минимально может растворять до 0,8% С углерода при температуре 727 ° С.
Химические соединения
Химическое соединение – это фаза, которая образуется, когда компоненты вступают в химическую реакцию.
Характерные особенности Х.С., образованных по закону нормальной валентности:
1. Кристаллическая решётка ХС отличается от решёток компонентов, образующих данное соединение.
2. В соединении всегда сохраняются краткое массовое соотношение элементов. Их состав всегда можно выразить формулой Am Bn, где А и В – соответствующие элементы, а
m и n – простые числа.
3. Свойства химических соединений резко отличаются от свойств, образующих его компонентов.
4. Температура плавления ХС величина постоянная.
5. Концентрация ХС величина постоянная.
6. В отличии от твёрдых растворов химические соединения образуются между компонентами с разным электронным строением атомов.
7. Рентгеновский анализ покажет новую кристаллическую решетку при образовании ХС.
Механические смеси
Механическая смесь – это не фаза, это структура, образованная несколькими фазами.
Механическая смесь – это смесь 2-х компонентов А и В образуется тогда, когда эти компоненты не способны к взаимному растворению в твёрдом состоянии и не вступают в химические реакции с образованием химических соединений.
Характерные особенности:
1. Рентгенограмма сплава покажет наличие 2-х решёток компонентов А и В.
2. Свойства отдельных компонентов А и В не изменяются.
3. Под микроскопом будет отчётливо видно кристаллы компонентов А и В.
Перлит- это сочетание 2-х фаз феррита и цементита. это структура.
Ледебурит- это механическая смесь аустенита и цементита.
Диаграммы состояния сплавов
Процесс кристаллизации металлических сплавов и связанные с ним закономерности строения сплавов описывают с помощью диаграмм состояния сплавов (диаграмм фазового равновесия).
Диаграмма состояния сплава - это графическое изображение состояния сплава на плоскости координатах температура, ТºС, концентрация, с %.
Диаграмма состояния в удобной графической форме показывает устойчивое состояние сплава, которое при данных температурных условиях обладает минимальной свободной энергией.
Диаграммы могут быть фазовыми и структурными, стабильными и метастабильными, равновесными и неравновесными.
По диаграмме состояния можно определить:
1. Фазовый состав сплава в зависимости от температуры и концентрации.
2. Структурный состав сплава в зависимости от температуры и концентрации.
3. Все превращения, которые происходят в сплавах при охлаждении или при нагреве.
4. Характерное окончательное состояние сплава, после того как все превращения произошли.
ЛЕКЦИИ ПО ДИСЦИПЛИНЕ «МАТЕРИАЛОВЕДЕНИЕ»
Материаловедение - это наука, изучающая связь между составом, строением и свойствами материалов, а так же закономерности их изменения под влиянием механических, физико-химических и других видов воздействий (тепловых, электромагнитных, радиоактивных, химических и др.).
Курс материаловедения состоит из двух основных частей:
1. Металловедение и термическая обработка металлов.
2. Неметаллические материалы (пластмассы, древесина, резина, стекло, керамика, асбест и др.).
Раздел 1. Металловедение и термическая обработка





 Подобная неодинаковость свойств монокристалла в различных кристаллографических направлениях называется анизотропией.
Подобная неодинаковость свойств монокристалла в различных кристаллографических направлениях называется анизотропией.


 При образовании кристалла первоначально образуются длинные ветви-оси 1го порядка (главные оси дендрита). На их ребрах происходит зарождение и рост перпендикулярных к ним таких же ветвей 2-го порядка, на этих осях зарождаются и растут оси 3-го порядка.
При образовании кристалла первоначально образуются длинные ветви-оси 1го порядка (главные оси дендрита). На их ребрах происходит зарождение и рост перпендикулярных к ним таких же ветвей 2-го порядка, на этих осях зарождаются и растут оси 3-го порядка.






