

История развития пистолетов-пулеметов: Предпосылкой для возникновения пистолетов-пулеметов послужила давняя тенденция тяготения винтовок...

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...

История развития пистолетов-пулеметов: Предпосылкой для возникновения пистолетов-пулеметов послужила давняя тенденция тяготения винтовок...

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...
Топ:
Марксистская теория происхождения государства: По мнению Маркса и Энгельса, в основе развития общества, происходящих в нем изменений лежит...
Проблема типологии научных революций: Глобальные научные революции и типы научной рациональности...
Когда производится ограждение поезда, остановившегося на перегоне: Во всех случаях немедленно должно быть ограждено место препятствия для движения поездов на смежном пути двухпутного...
Интересное:
Уполаживание и террасирование склонов: Если глубина оврага более 5 м необходимо устройство берм. Варианты использования оврагов для градостроительных целей...
Распространение рака на другие отдаленные от желудка органы: Характерных симптомов рака желудка не существует. Выраженные симптомы появляются, когда опухоль...
Принципы управления денежными потоками: одним из методов контроля за состоянием денежной наличности является...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Атомы и молекулы имеют абсолютные массы порядка 10–24–10–21 г, неудобные для сравнения, поэтому химики пользуются относительными значениями масс атомов. Представление об относительной атомной массе было введено Дж. Дальтоном в 1803 г. За единицу массы он принял массу самого легкого атома – водорода. В настоящее время в качестве эталона принята масса 1/12 массы атома углерода изотопа 12С, равная 1,66043×10–24 г.
Относительная атомная (А r) масса показывает во сколько раз данный атом тяжелее 1/12 массы атома изотопа углерода 12С.
 , ,
| (1.2) |
где m а – масса атома, m а(С) – масса атома изотопа углерода 12С.
Для определения атомной массы элементов в 19 веке использовался метод, основанный на законе теплоемкости П.Л. Дюлонга и А.Т. Пти (1819 г.): молярная теплоемкость (СМ) для различных простых веществ в кристаллическом состоянии одинакова и равна приблизительно 26,4 Дж. Она равна произведению удельной теплоемкости (Суд) на молярную массу элемента:
| Смолярная=Суд×М =26,4 Дж | (1.3) |
Используя величину удельной теплоемкости, которая легко определяется экспериментально (отношение количества теплоты полученного или отданного 1 г вещества к соответствующему изменению температуры) можно найти приближенное значение атомной массы. Исключения составляют легкие элементы, особенно неметаллы, имеющие теплоемкость значительно меньше (бериллий, бор, кремний, алмаз).
В настоящее время атомные массы элементов определяют методом масс-спектроскопии. Массы атомов определяют по отклонению траектории их ионов, двигающихся в магнитном поле, поскольку величина отклонение зависит от отношения массы иона к его заряду.
Относительная молекулярная масса (M r)показывает во сколько раз данная молекула тяжелее 1/12 массы атома 12С.
|
|
 , ,
| (1.4) |
где m м – масса молекулы.
Количество вещества
Другой характеристикой вещества является количество вещества – физическая величина, определяемая числом частиц. Единица количества вещества – моль содержит такое же число частиц, как и 12 граммов углерода 12С. Это число частиц, равное 6,02×1023, называется Авогадровым числом (N A).
 , ,
| (1.5) |
где n – количество вещества,
М – молярная масса (масса одного моля),
V m – молярный объем.
Для железа M = 56 г/моль, для воды M = 18 г/моль.
Молярные объемы твердых и жидких веществ зависят от их плотности:
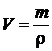 .
.
V m(H2O) = 18 мл/моль, т.к. плотность воды (r) равна 1 г/мл.
Закон Авогадро
У газообразных веществ при атмосферном давлении собственные размеры молекул незначительны по сравнению с расстояниями между ними. Молярные объемы газов при одинаковых условиях постоянны, и при нормальных условиях близки к 22,4 л/моль. Это следствие из закона Авогадро (1811 г.): в равных объемах различных газов при одинаковых условиях содержится одинаковое число молекул.
Относительная плотность газов
Из закона Авогадро следует, что плотности различных газов будут относиться друг к другу, как молярные массы. Для определения молярных масс газов используется значение относительной плотности газов – отношение массы определенного объема одного газа к массе такого же объема другого газа (при тех же условиях):
Измерив относительную плотность одного газа по другому, можно определить его молекулярную массу, что используется в аналитической химии для идентификации газообразных веществ.
|
|
|

Таксономические единицы (категории) растений: Каждая система классификации состоит из определённых соподчиненных друг другу...

Особенности сооружения опор в сложных условиях: Сооружение ВЛ в районах с суровыми климатическими и тяжелыми геологическими условиями...

Наброски и зарисовки растений, плодов, цветов: Освоить конструктивное построение структуры дерева через зарисовки отдельных деревьев, группы деревьев...

Типы сооружений для обработки осадков: Септиками называются сооружения, в которых одновременно происходят осветление сточной жидкости...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!