1. CH3—СCl3 + 3NaOH → CH3—COOH + 3NaCl + Н2O (гидролиз тригалогенопроизводных)
2. R—CHO + [О] → R—COOH (окисление альдегидов и кетонов)
3. CH3—CH=CH2 + CO + Н2O/Н+ → Ni, р, t → CH3—CH2—CH2—COOH (оксосинтез)
4. CH3C≡N + 2Н2O/ Н+ → CH3COOH + NH4 (гидролиз нитрилов)
5. CO + NaOH → HCOONa; 2HCOONa + H2SO4 → 2HCOOH + Na2SO4 (получение HCOOH)
Химические свойства карбоновых кислот и их производных
Карбоновые кислоты проявляют высокую реакционную способность и вступают в реакции с различными веществами, образуя разнообразные соединения, среди которых большое значение имеют функциональные производные: сложные эфиры, амиды, нитрилы, соли, ангидриды, гало-генангидриды.
1. а) 2CH3COOH + Fe → (CH3COO)2Fe + Н2 (образование солей)
б) 2CH3COOH + MgO → (CH3COO)2Mg + Н2O
в) CH3COOH + KOH → CH3COОК + Н2O
г) CH3COOH + NaHCO3 → CH3COONa + CO2 + Н2O
CH3COONa + H2O ↔ CH3COOH + NaOH (соли карбоновых кислот гидролизуются)
2. (образование вложных эфиров)

(омыление вложного эфира)

3. (получение хлорангидридов кислот)

4. (разложение водой)

5. CH3—COOH + Cl2 → hv → Cl—CH2—COOH + HCl (галогенирование в α-положение)
6. HO—CH=O + Ag2O → NH3 → 2Ag + Н2CO3 (Н2O + CO2) (особенности HCOOH)
HCOOH → t → CO + Н2O
Жиры
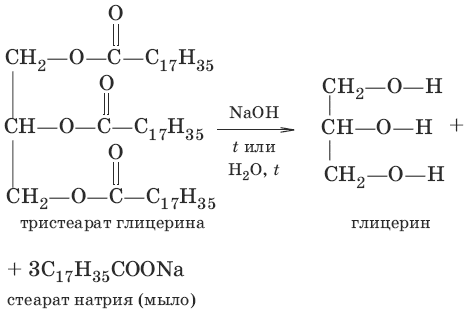
Жиры – сложные эфиры глицерина и высших одноатомных карбоновых кислот. Общее название таких соединений – триглицериды. В состав природных триглицеридов входят остатки насыщенных кислот (пальмитиновой С15Н31COOH, стеариновой С17Н35COOH) и ненасыщенных (олеиновой С17Н33COOH, линолевой С17Н31COOH). Жиры состоят главным образом из триглицеридов предельных кислот. Растительные жиры – масла (подсолнечное, соевое) – жидкости. В состав триглицеридов масел входят остатки непредельных кислот.

Жирам как сложным эфирам свойственна обратимая реакция гидролиза, катализируемая минеральными кислотами. При участии щелочей гидролиз жиров происходит необратимо. Продуктами в этом случае являются мыла – соли высших карбоновых кислот и щелочных металлов. Натриевые соли – твердые мыла, калиевые – жидкие. Реакция щелочного гидролиза жиров называется также омылением.
Амины
Амины – органические производные аммиака, в молекуле которого один, два или три атома водорода замещены на углеводородные радикалы. В зависимости от числа углеводородных радикалов различают первичные RNH2, вторичные R2NH, третичные R3N амины. По характеру углеводородного радикала амины подразделяются на алифатические (жирные), ароматические и смешанные (или жирноароматические). Названия аминов в большинстве случаев образуют из названий углеводородных радикалов и суффикса –амин. Например, CH3NH 2 – метиламин; CH3—CH2—NH2 – этиламин. Если амин содержит различные радикалы, то их перечисляют в алфавитном порядке: CH3—CH2—NH—CH3 – ме-тилэтиламин.
Изомерия аминов определяется количеством и строением радикалов, а также положением аминогруппы. Связь N—Н является полярной, поэтому первичные и вторичные амины образуют межмолекулярные водородные связи. Третичные амины не образуют ассоциирующих водородных связей. Амины способны к образованию водородных связей с водой. Поэтому низшие амины хорошо растворимы в воде. С увеличением числа и размеров углеводородных радикалов растворимость аминов в воде уменьшается.
Способы получения аминов
1. R—NO2 + 6[Н] → R—NH2 + 2H2O (восстановление нитросоединений)
2. NH3 + CH3I → [CH3N+H3]I¯ → NH3 → CH3NH 2 + NH 4I (алкилирование аммиака)
3. а) С6Н5—NO2 + 3(NH4)2S → С6Н5—NH2 + 3S + 6NH3 + 2H2O (реакция Зинина)
б) С6Н5—NO2 + 3Fe + 6HCl → С6Н5—NH2 + 3FeCl2 + 2Н2O (восстановление нитросоединений)
в) С6Н5—NO2 + ЗН2 → катализатор, t → C6H5—NH 2 + 2Н2O
4. R—C≡N + 4[H] → RCH2NH2 (восстановление нитрилов)
5. ROH + NH3 → Al2O3,350 °C → RNH2 + 2H2O (получение низших алкиламинов С2—С4)
Химические свойства аминов
Амины имеют сходное с аммиаком строение и проявляют подобные ему свойства. Как в аммиаке, так и в аминах атом азота имеет неподеленную пару электронов. Для аминов характерны ярко выраженные основные свойства. Водные растворы алифатических аминов проявляют щелочную реакцию. Алифатические амины – более сильные основания, чем аммиак. Ароматические амины являются более слабыми основаниями, чем аммиак, поскольку не-поделенная электронная пара атома азота смещается в сторону бензольного кольца, вступая в сопряжение с его π-электронами.

На основность аминов влияют различные факторы: электронные эффекты углеводородных радикалов, пространственное экранирование радикалами атома азота, а также способность образующихся ионов к стабилизации за счет сольватации в среде растворителя. В результате донорного эффекта алкильных групп основность алифатических аминов в газовой фазе (без растворителя) растет в ряду: первичные < вторичные < третичные. Основность ароматических аминов зависит также от характера заместителей в бензольном кольце. Электроноакцепторные заместители (—F, —Cl, —NO2 и т. п.) уменьшают основные свойства ариламина по сравнению с анилином, а электронодонорные (алкил R—, —OCH3, —N(CH3)2 и др.), напротив, увеличивают.
1. CH3—NH 2 + Н2O → [CH3—NH3]OH (взаимодействие с водой)
2. (CH 3)2NH + HCl → [(CH3)2NH2]Cl хлорид диметиламмония (взаимодействие с кислотами)
[(CH 3)2NH 2]Cl + NaOH → (CH 3)2NH + NaCl + H2O (взаимодействие солей аминов со щелочами)
3.

(ацителирование, с третичными аминами не идет)
4. R—NH2 + CH3I → [CH3N+H2R]I¯ → NH3 → CH3NHR + NH4I (алкилирование)
5. Взаимодействие с азотистой кислотой: строение продуктов реакции с азотистой кислотой зависит от характера амина. Поэтому данная реакция используется для различия первичных, вторичных и третичных аминов.
а) R—NH2 + HNO2 → R—OH + N2 + H2O (первичные жирные амины)
б) С6Н5—NH2 + NaNO2 + HCl → [С6Н5—N≡N]+Cl¯ – соль диазония (первичные ароматические амины)
в) R2NH + Н—О—N=O → R2N—N=O (N-нитрозамин) + Н2O (вторичные жирные и ароматические амины)
г) R3N + Н—О—N=O → при низкой температуре нет реакции (третичные жирные амины)
д)

(третичные ароматические амины)
Свойства анилина. Для анилина характерны реакции как по аминогруппе, так и по бензольному кольцу. Бензольное кольцо ослабляет основные свойства аминогруппы по сравнению с алифатическими аминами и аммиаком, но под влиянием аминогруппы бензольное кольцо становится более активным в реакциях замещения по сравнению с бензолом.
C6H5—NH2 + HCl → [C6H5—NH3]Cl = C6H5NH2 • HCl
C6H5NH2 • HCl + NaOH → C6H5NH2 + NaCl + H2O
C6H5NH2 + CH3I → t → [C6H5NH2CH3]+I¯

Аминокислоты
Аминокислотами называются гетеро-функциональные соединения, молекулы которых содержат одновременно аминогруппу и карбоксильную группу. В зависимости от взаимного расположения амино– и карбоксильной групп аминокислоты подразделяют на α-, β-, γ– и т. д. По ИЮПАК, для наименования аминокислот группу NH2— называют приставкой амино-, указывая цифрой номер углеродного атома, с которым она связана, а затем следует название соответствующей кислоты.

2-аминопропановая кислота (α-аминопропановая, α-аланин)

3-аминопропановая кислота (β-аминопропановая, β-аланин)

6-аминогексановая кислота (ε-аминокапроновая)
По характеру углеводородного радикала различают алифатические (жирные) и ароматические аминокислоты. Изомерия аминокислот зависит от строения углеродного скелета, положения аминогруппы по отношению к карбоксильной группе. Для аминокислот характерна еще оптическая изомерия.



















