КАРДИОТОНИЧЕСКИЕ СРЕДСТВА
Препараты, стимулирующие деятельность сердца, нередко подразделяются на:
1. Сердечные гликозиды.
2. Препараты «негликозидной» структуры.
Исходя из механизма действия, кардиотонические средства можно представить следующими группами.
I. Средства, повышающие внутриклеточное содержание ионов Са
1. Ингибиторы Na+, К+-АТФазы Сердечные гликозиды:
Дигоксин Целанид Строфантин Коргликон
2. Средства, повышающие содержание цАМФ А. За счет рецепторной активации адренилатциклазы
Средства, стимулирующие β1-адренорецепторы: Дофамин Добутамин Б. За счет ингибирования фосфодиэстеразы III Амринон Милринон II. Средства, повышающие чувствительность миофибрилл к ионам Са Левосимендан
СЕРДЕЧНЫЕ ГЛИКОЗИДЫ
Сердечные гликозиды - это вещества растительного происхождения, которые оказывают выраженное кардиотоническое действие. Они повышают работоспособность миокарда, обеспечивая наиболее экономную и вместе с тем эффективную деятельность сердца. Сердечные гликозиды используются при лечении сердечной недостаточности, которая чаще всего развивается на фоне ишемической болезни сердца, поражениях миокарда разной этиологии, при нарушениях ритма сердечных сокращений.
Сердечные гликозиды состоят из несахаристой части (агликона или генина) и сахаров (гликона1). Основой агликона является стероидная (циклопентанпергидрофенантреновая) структура, связанная у большинства гликозидов с ненасыщенным лактоновым кольцом. Гликон может быть представлен разными сахарами: D-дигитоксо- зой, D-глюкозой, D-цимарозой, D-рамнозой и др. (см. структуры). Число сахаров в молекуле варьирует от 1 до 4.
Иногда к сахаристой части присоединен ос- таток уксусной кислоты. Кардиотонический эффект связывают с агликоном. Что касается роли сахаристой части, то от нее зависят растворимость гликозидов и их фиксация в тканях. Гликон влияет также на активность и токсичность соединений.
Сердечные гликозиды легко подвергаются гид- ролизу (энзиматическому, кислотному, щелочному). Отмечено, что в самих растениях имеются ферменты, гидролизующие сердечные гликозиды. Последним объясняется возможность гидролитического расщепления первичных (генуинных2) гликозидов в самом лекарственном сырье в пери-

В. УИТЕРИНГ (1741-1799). Внедрил в практическую медицину препараты наперстянки (1785).
1 От греч. glykys - сладкий.
2 От греч. genos - род, происхождение.
од его хранения или подготовки к обработке. Для предупреждения этого процесса ферменты можно ингибировать.
Основные пути химического превращения ряда сердечных гликозидов, содержащихся в соответствующих растениях, показаны на схеме 14.1. Они используются в фармацевтической промышленности для получения лекарственных препаратов сердечных гликозидов (особенно более стойких вторичных гликозидов).
В медицинской практике применяют препараты сердечных гликозидов, получаемые из следующих растений:
• наперстянки пурпуровой (Digitalis purpurea; рис. 14.1) - дигитоксин;
• наперстянки шерстистой (Digitalis lanata) - дигоксин, целанид (ланатозид С, изоланид);

Схема 14.1. Распад гликозидов наперстянки, строфанта, ландыша
• строфанта Комбё (Strophanthus Komb é)- строфантин К1;
• ландыша (Convallaria) - коргликон;
• горицвета (Adonis vernalis) - настой травы горицвета.
Источники получения сердечных гликозидов, применяемые препараты и их действующие начала приведены в табл. 14.12. Наибольший интерес представляют индивидуальные гликозиды. Простые, галеновы и новогаленовы препараты утрачивают свое значение.
Основным свойством сердечных гликозидов является их избирательное действие на сердце. Главную роль в фармакотерапевти- ческом эффекте сердечных гликозидов играет усиление систолы (кардиотоническое действие, положительное инотропное3 действие), связанное с прямым влиянием препаратов на миокард. Систолическое сокращение стано-

Рис. 14.1. Наперстянка пурпуровая - Digitals purpurea L. (содержит первичные гликозиды наперстянки - пурпуреагликозиды А и В, которые в процессе высушивания растения превращаются во вторичные гликозиды - дигитоксин и гитоксин).
Таблица 14.1. Растения и препараты, содержащие сердечные гликозиды
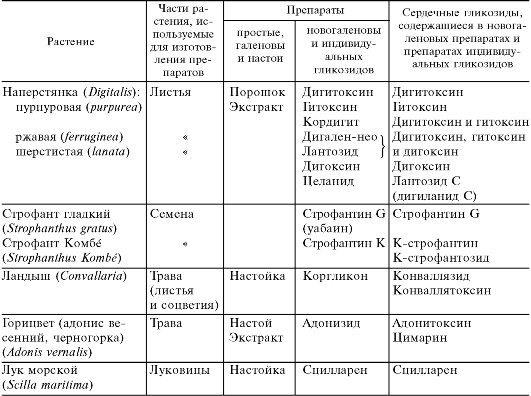
1 Смесь гликозидов из семян строфанта Комбе (в основном β-строфантина К и К-строфантозида).
2 Более полную таблицу см. в 1-м и 2-м изданиях этого учебника (1980, 1981).
3 От греч. is (род. п. inos) - волокно, мускул, tropos - направление.
вится более энергичным и быстрым. На ЭКГ это проявляется укорочением интервала Q-T; со стороны желудочкового комплекса типичны также снижение сегмента S-T ниже изоэлектрической линии, уменьшение, сглаживание или инверсия зубца T.
При сердечной недостаточности сердечные гликозиды заметно увеличивают ударный и минутный объем сердца. Важно, что работа сердца повышается без увеличения потребления им кислорода (на единицу работы).

Примечание. Структуру дофамина и добутамина см. в главе 4.
Механизм кардиотонического действия сердечных гликозидов связан с их ингибирующим влиянием на Nа+,К+-АТФ-азу мембраны кардиомиоцитов (рис. 14.2). Это приводит к нарушению тока Na+ и К+. В итоге содержание К+ внутри кардиомиоцитов снижается, а Na+ - повышается. При этом разница между внутри- и внеклеточной концентрацией Na+ уменьшается, что понижает трансмембранный Na+/Са2+-обмен. Последнее снижает интенсивность выведения Са2+, что способствует увеличению его содержания в саркоплазме и накоплению в саркоплазматическом ретикулуме. В свою очередь это стимулирует поступление извне дополнительных количеств Са2+ в кардиомиоциты через кальциевые L-каналы. На этом фоне потенциал действия вызывает повышенное высвобождение Са2+ из сарко- плазматического ретикулума. При этом увеличивается содержание свободных ионов

Рис. 14.2. Предполагаемый механизм кардиотонического действия сердечных гликозидов. а-в - этапы действия сердечных гликозидов; ми- нус - угнетающее действие; (↑) - повышение содержания ионов; (↓) - снижение содержания ионов.
Са2+ в саркоплазме, что и обеспе- чивает кардиотонический эффект. Ионы Са2+ взаимодействуют с тро- пониновым комплексом и устраняют его тормозное влияние на сократительные белки миокарда. Происходит взаимодействие актина с миозином, что проявляется быстрым и сильным сокращением миокарда (см. рис. 14.2).
Важно, что работа сердца повышается на фоне урежения сердечного ритма (отрицательное хронотропное1 действие) и удлинения диастолы. Это создает наиболее экономный режим работы сердца: сильные систолические сокращения сменяются достаточными периодами «отдыха» (диастолы), благоприятствующими восстановлению энергетических ресурсов в миокарде. Урежение ритма сердечных сокращений в значительной степени связано с кардио-кардиальным рефлексом. Под воздействием сердечных гликозидов возбуждаются окончания чувствительных нервов сердца и рефлекторно, через систему блуждающих нервов возникает брадикардия. Не исключено, что опре- деленную роль играет усиление рефлексов на сердце с механорецепторов синоаортальной зоны во время систолы в результате повышения артериального давления. На ЭКГ наблюдается увеличение интервала Р-Р.
Кроме того, сердечные гликозиды, оказывая прямое угнетающее влияние на проводящую систему сердца и тонизируя блужда- ющий нерв, снижают скорость проведения возбуждения (отрицательное дромо- тропное1 действие). Рефрактерный период предсердно-желудочкового (атриовентрикулярного) узла и предсердно-желудочкового пучка (пучок Гиса) увеличивается. Интервал Р-Q становится более продолжительным. В токсических дозах сердечные гликозиды могут вызывать предсердно-желудочковый блок.
1 От греч. chronos - время.
2 От греч. dromos - путь, дорога.
В больших дозах сердечные гликозиды повышают автоматизм сердца. Это приводит к образованию эктопических очагов возбуждения, генерирующих импульсы независимо от синусного узла. Возникают аритмии (в частности, экстрасистолы).
Судя по опытам на животных, в малых дозах сердечные гликозиды повышают возбудимость миокарда (положительное батмотропное1действие). Это проявляется в снижении порога возбудимости миокарда в ответ на поступающие к нему стимулы. В больших дозах сердечные гликозиды понижают возбудимость мышцы сердца.
Таким образом, возбудимость и автоматизм - два различных параметра, которые изменяются под влиянием сердечных гликозидов неоднозначно. Изменение автоматизма и возбудимости связано с прямым действием сердечных гликозидов на миокард.
При сердечной недостаточности повышение под влиянием сердечных гликозидов его минутного объема положительно сказывается на кровообращении в целом (табл. 14.2). Основное действие сердечных гликозидов на кровообращение при
Таблица 14.2. Эффекты сердечных гликозидов при сердечной недостаточности
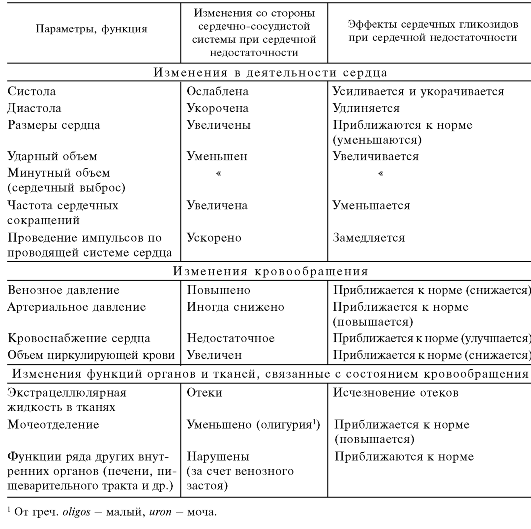
1 От греч. bathmos - порог.
декомпенсации сердца заключается в уменьшении венозного застоя. При этом венозное давление падает и отеки постепенно исчезают. При устранении венозного застоя не происходит рефлекторного учащения сердечного ритма (рефлекс Бейнбриджа с устьев верхних полых вен). Артериальное давление не изменяется или повышается (если было понижено). Общее периферическое сопротивление сосудов уменьшается, кровоснабжение и оксигенация тканей улучшаются. Нарушенные функции внутренних органов (печени, желудочно-кишечного тракта и др.) восстанавливаются. Кровоснабжение сердца сердечные гликозиды могут улучшать за счет нормализации общей гемодинамики (у препаратов наперстянки при их введении в высоких дозах отмечено незначительное прямое коронаросуживающее действие).
Функция почек в результате благоприятного влияния сердечных гликозидов на кровообращение нормализуется. Диурез увеличивается. Имеются данные о том, что препараты наперстянки и строфанта оказывают и прямое действие на почки, уменьшая реабсорбцию ионов натрия. Однако это имеет второстепенное значение.
Повышение диуреза способствует выведению из организма избыточной жидкости. Последнее облегчает условия гемодинамики, так как вследствие уменьшения объема циркулирующей крови снижается нагрузка на сердце. Кроме того, уменьшается или полностью исчезает отек тканей.
До сих пор речь шла об общих свойствах сердечных гликозидов. Вместе с тем разные препараты имеют и определенные отличия. Это касается активности, скорости развития эффекта, его продолжительности, а также фармакокинетики веществ.
По активности сердечные гликозиды различаются довольно существенно. При определении активности лекарственного сырья и многих препаратов (галеновых, новогаленовых и др.) используют биологическую стандартизацию. В этом случае активность сердечных гликозидов наиболее часто обозначают лягушачьими единицами действия (ЛЕД1).
Для примера приведены требуемая активность лекарственного сырья, содержащего ряд сердечных гликозидов, и активность индивидуальных гликозидов.
Лекарственное сырье
1 г листьев наперстянки содержит 50-66 ЛЕД
1 г травы горицвета содержит 50-66 ЛЕД
1 г травы ландыша содержит 120 ЛЕД
1 г семян строфанта содержит 2000 ЛЕД
Индивидуальные гликозиды
1 г дигитоксина содержит 8000-10 000 ЛЕД
1 г целанида содержит 14 000-16 000 ЛЕД
1 г конваллятоксина содержит 63 000-80 000 ЛЕД
1 г строфантина К содержит 44 000-56 000 ЛЕД
Таким образом, биологическая активность строфантина К и конваллятоксина (гликозид ландыша) значительно выше, чем гликозидов наперстянки - дигитоксина и целаида.
В клинике об активности сердечных гликозидов можно судить по равноэффективным дозам при их внутривенном введении.
Различия сердечных гликозидов заключаются также в длительности латентного2 периода действия и скорости нарастания эффекта. Так, при внутривенном введении строфантин и конваллятоксин начинают действовать на сердце через 5-10 мин, а целанид - через 5-30 мин. При введении дигоксина внутрь эффект
1 1 ЛЕД соответствует минимальной дозе стандартного препарата, в которой он вызывает остановку сердца в систоле у большинства подопытных лягушек. Кроме того, используют кошачьи (КЕД) и голубиные (ГЕД) единицы действия (подробности методик см. в Государственной фармакопее).
2 От лат. latens - скрытый.
развивается через 30 мин, а при приеме дигитоксина - примерно через 2 ч (табл. 14.3).
При применении веществ в равноэффективных дозах и одинаковом пути их введения (внутривенном) максимальный эффект особенно быстро наступает у строфантина и конваллятоксина1 (через 30 мин-1,5 ч), далее следуют целанид и дигоксин (1-5 ч), затем - дигитоксин (4-12 ч). Следовательно, даже среди препаратов наперстянки скорость развития эффекта неодинакова. По скорости развития кардиотропного эффекта сердечные гликозиды можно представить следующим рядом: строфантин = конваллятоксин > целанид > дигоксин > дигитоксин.
Длительность кардиотонического влияния сердечных гликозидов определяется скоростью их инактивации в организме, связыванием с белками плазмы и скоростью выведения (см. табл. 14.3). Препараты строфанта, горицвета и ландыша выводятся обычно в течение суток или несколько дольше. Особенно продолжительный эффект вызывает гликозид наперстянки пурпуровой дигитоксин (элиминация длится 2-3 нед). Промежуточное положение занимают гликозиды наперстянки шерстистой дигоксин и целанид (время их выведения 3-6 дней).
Важной характеристикой сердечных гликозидов является их способность к кумуляции. Чем продолжительнее действуют сердечные гликозиды, тем больше они кумулируют. Речь идет о материальной кумуляции, т.е. о накоплении самого вещества в организме. Особенно выраженная кумуляция отмечена для дигитоксина. Связано это с медленно протекающими процессами инактивации и выведения дигитоксина из организма (t1/2 ≈ 160 ч). В меньшей степени кумулируют дигоксин (t1/2 ≈ 34-36 ч) и целанид.
Примерно 7/8 введенной дозы строфантина выводится в первые 24 ч, поэтому при его применении кумуляция выражена в небольшой степени. По длительности действия и способности кумулировать гликозиды наперстянки и строфантин рас-
Таблица 14.3. Сравнительная характеристика ряда сердечных гликозидов наперстянки и строфанта
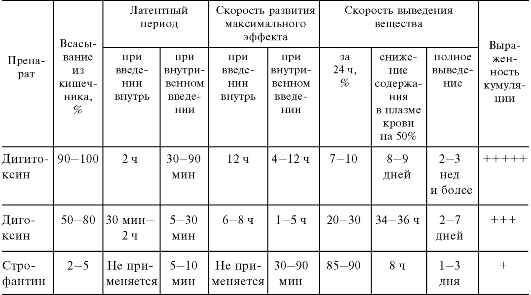
1 Это относится и к новогаленовому препарату коргликону, одним из действующих начал которого является конваллятоксин.
полагаются в следующем порядке: дигитоксин > дигоксин > целанид > строфантин. Препараты горицвета и ландыша кумулируют еще меньше, чем строфантин.
Всасываются препараты сердечных гликозидов из желудочно-кишечного тракта неодинаково. Очень хорошо всасываются более липофильные дигитоксин (90- 95%) и дигоксин (50-80%), хорошо - целанид (20-40%). Очень плохо всасывается (2-5%) и частично разрушается строфантин. Гликозиды ландыша в пищеварительном тракте в значительной степени разрушаются. Поэтому энтерально целесообразно вводить в основном препараты наперстянки (дигоксин). Внутрь принимают также препараты горицвета (настой травы горицвета).
После всасывания сердечные гликозиды распределяются по разным органам и тканям. В сердце обнаруживается не более 1% от введенной дозы. Таким образом, основная направленность действия сердечных гликозидов объясняется высокой чувствительностью тканей сердца к этой группе лекарственных веществ.
Часть вводимых гликозидов обратимо связывается с альбуминами плазмы (например, дигоксин на 30-35%, строфантин менее чем на 5%).
Биотрансформации сердечные гликозиды подвергаются главным образом в печени. Один из основных принципов химического превращения заключается в том, что они последовательно отщепляют молекулы сахаров (гликонов) до образования несахаристой части (агликона, или генина). Кроме того, могут происходить их гидроксилирование (например, дигитоксина) и частичное образование конъюгатов (с глюкуроновой кислотой).
Выделяются сердечные гликозиды и продукты их превращения в основном почками, а также с желчью (из кишечника они частично повторно абсорбируются). При патологии почек длительность действия сердечных гликозидов увеличивается.
Дигитоксин выделяется преимущественно в виде метаболитов и конъюгатов. Дигоксин лишь в небольшой части подвергается химическим превращениям. Строфантин выделяется в неизмененном виде.
Применяют сердечные гликозиды главным образом при острой и хронической сердечной недостаточности. При острой сердечной недостаточности вводят сердечные гликозиды с коротким латентным периодом (строфантин, коргликон). Основным препаратом для введения внутрь при хронической сердечной недостаточности является дигоксин. Иногда гликозиды (в основном препараты наперстянки) назначают при сердечных аритмиях (при мерцательной аритмии, при пароксизмальной предсердной и узловой тахикардии). Эффективность гликозидов при указанных аритмиях связана с повышением тонуса блуждающего нерва и угнетением проведения возбуждения по проводящей системе сердца (см. главу 14.2).
Вводят сердечные гликозиды чаще внутрь (препараты наперстянки, горицвета) и внутривенно (строфантин, дигоксин, целанид, коргликон), иногда - внутримышечно и ректально. Подкожные инъекции нецелесообразны, так как они могут быть причиной нежелательных реакций - раздражения на месте введения, боли, абсцессов.
Противопоказаниями к применению сердечных гликозидов являются неполный предсердно-желудочковый блок, выраженная брадикардия, острый инфекционный миокардит. С осторожностью следует использовать сердечные гликозиды с препаратами кальция и при гипокалиемии. Это связано с тем, что при повышенном содержании ионов кальция в сыворотке крови чувствительность миокарда к сердечным гликозидам повышается и соответственно возрастает возможность токсического действия этих препаратов. Аналогичным образом меняется действие сердечных гликозидов при снижении содержания ионов калия (что может возникать при применении мочегонных средств из группы салуретиков, при диарее, в послеоперационном периоде).
Токсические явления связаны с передозировкой сердечных гликозидов. Чаще это наблюдается при использовании препаратов наперстянки с выраженной способностью к кумуляции. Интоксикация препаратами наперстянки проявляется кардиальными и экстракардиальными нарушениями. При этом возникают разнообразные аритмии (например, экстрасистолы), частичный или полный предсердно-желудочковый блок. Наиболее частая причина смерти от отравлений - мерцание желудочков.
Со стороны других систем отмечаются ухудшение зрения (в том числе цветового), утомляемость, мышечная слабость, диспепсические явления (тошнота, рвота1, диарея), могут быть психические нарушения (возбуждение, галлюцинации), головная боль, кожные высыпания.
Лечение отравления препаратами наперстянки и другими сердечными гликозидами направлено прежде всего на устранение неблагоприятных изменений функций сердца. Помимо отмены препарата или уменьшения его дозы, применяют ряд физиологических антагонистов. С учетом того, что сердечные гликозиды вызывают снижение содержания ионов калия в кардиомиоцитах, показано применение препаратов калия (калия хлорид, калий нормин и др.). Вводят их внутрь или внутривенно в таких количествах, чтобы содержание ионов калия в сыворотке крови не превышало обычных величин. Препараты калия используют для предупреждения токсического влияния гликозидов на сердце, особенно нарушений ритма сердечных сокращений. С этой же целью назначают препараты магния (магния оротат), а также панангин (содержит калия аспарагинат и магния аспарагинат) и аналогичные ему по составу таблетки «Аспаркам»2. Панагин и аспаркам выпускают и в ампулах для внутривенного введения. Следует учитывать, что вещества, снижающие концентрацию ионов калия в крови (ряд мочегонных средств, кортикостероиды), способствуют проявлению кардиотоксического действия сердечных гликозидов.
При аритмиях используют дифенин, лидокаин, амиодарон, оказывающие противоаритмическое действие (см. главу 14.2). При предсердно-желудочковом блоке для устранения влияния блуждающего нерва на сердце назначают атропин.
При интоксикации сердечными гликозидами могут быть также использованы моноклональные антитела. Так, к числу антидотов дигоксина относится один из таких препаратов Digoxin immune fab (Digibind).
Некоторый положительный эффект при интоксикации сердечными гликозидами дает также содержащий в своей молекуле сульфгидрильные группы унитиол. По-видимому, это связано с тем, что он реактивирует транспортную АТФазу клеток миокарда, ингибированную сердечными гликозидами. Однако применяют его редко.
Исходя из того что в действии сердечных гликозидов принимают большое участие ионы кальция, предложено использовать препараты, связывающие ионы кальция и понижающие их содержание в сыворотке крови. Такими свойствами обладают динатриевая соль этилендиаминтетрауксусной кислоты (динатриевая соль ЭДТА, динатрия эдетат, Na2 ЭДТА, трилон Б), а также цитраты.
Вводят динатриевую соль ЭДТА внутривенно при аритмиях, возникающих при отравлении сердечными гликозидами. Однако эффект выражен в небольшой степени и непродолжителен, поэтому применяют ее редко.
1 Тошнота и рвота, наблюдаемые при введении препаратов наперстянки, связаны главным образом с возбуждением пусковой зоны центра рвоты и частично - с раздражающим влиянием на слизистую оболочку пищеварительного тракта.
2 Следует, однако, учитывать, что содержание ионов калия в панангине (0,158 г калия аспарагината в 1 таблетке) и в таблетках «Аспаркам» (0,175 г калия аспарагината в 1 таблетке) при обычном дозировании этих препаратов недостаточно для устранения токсического действия сердечных гликозидов. Калий-нормин содержит в одной таблетке 1 гкалия хлорида.
Препараты
| Название
| Средняя терапевтическая доза для взрослых; путь введения
| Форма выпуска
|
|
|
|
|
| Дигоксин - Digoxinum
| Внутрь и внутривенно 0,00025 г
| Таблетки по 0,00025 г; ампулы по 1 мл 0,025% раствора
|
1 В англоязычной литературе эта группа препаратов обозначается как calcium sensitisers. От англ. sensitize - сенсибилизировать, делать чувствительным.
Продолжение табл.
|
|
|
|
| Целанид - Celanidum
| Внутрь 0,00025 г; внутривенно
0,0002 г
| Таблетки по 0,00025 г; флаконы по 10 мл 0,05% раствора (для приема внутрь); ампулы по 1 мл 0,02% раствора
|
| Строфантин К - Strophanthinum K
| Внутривенно 0,00025 г
| Ампулы по 1 мл 0,05% раствора
|
| Коргликон - Corglyconum
| Внутривенно 0,0003 г
| Ампулы по 1 мл 0,06% раствора
|
| Настойтравыгорицвета - Infusum herbae Adonidis vernalis
| Внутрь 15 мл настоя 1:50-1:20
| Настой в концентрации 1:50-
1:20
|
ЛЕКАРСТВЕННЫЕ СРЕДСТВА, ПРИМЕНЯЕМЫЕ ПРИ НАРУШЕНИЯХ РИТМА СЕРДЕЧНЫХ СОКРАЩЕНИЙ (ПРОТИВОАРИТМИЧЕСКИЕ СРЕДСТВА)
Ритмическая активность миокарда зависит от состояния водителя ритма и проводящей системы сердца, от биохимизма миокарда, его кровоснабжения и других кардиальных факторов. Значительную роль играют также нейрогенные и гуморальные экстракардиальные влияния. Нарушения в отдельных звеньях этой сложной системы могут вызывать патологические изменения сердечного ритма.
Причины сердечных аритмий весьма разнообразны. Они могут быть связаны с ишемией миокарда, пороками сердца, электролитными нарушениями, изменениями кислотно-основного состояния, интоксикацией химическими веществами, нарушением иннервации сердца, эндокринными и инфекционными заболеваниями и др.
Нарушения ритма сердечных сокращений обусловлены изменениями автоматизма и(или) проводимости проводящей системы и мышечных клеток сердца (рис. 14.3).
Патологические изменения автоматизма проявляются нарушением генерации импульсов в физиологическом водителе ритма (основным является синуснопредсердный, или синоатриальный, узел) либо возникновением эктопических водителей ритма. Электрофизиологически появление эктопических водителей ритма и увеличение частоты разрядов могут быть связаны с увеличением скорости диастолической деполяризации (рис. 14.4), снижением потенциала покоя мембраны (максимального диастолического потенциала; потенциал становится менее электроотрицательным) и снижением порога потенциала действия (порог становится более электроотрицательным). Указанные изменения способствуют развитию аритмий.
Нарушения проводимости проявляются в разных степенях блока проведения по проводящей системе сердца. О проводимости судят по скорости нарастания амплитуды потенциала действия (фаза 0). При снижении проводимости скорость систолической деполяризации - фазы 0 (Vmax) - уменьшается (максимальное значение потенциала действия достигается более медленно). На ЭКГ нарушение проводимости в предсердно-желудочковом (атриовентрикулярном) узле проявля-
ется увеличением интервала P-R, а внутрижелудочковой - длительности QRST. Функциональный блок проведения может быть односторонним (рис. 14.5). В этом случае аритмии развиваются по механизму «повторного входа» (или «возврата возбуждения»1). Таким путем могут возникать аритмии и в предсердиях, и в желудочках.
Для развития аритмий важное значение имеет величина эффективного рефрактерного периода2. При его уменьшении возможность экстрасистол и проведения более частых стимулов повышается. Это часто сопровождается укороче-

Рис. 14.3. Проводящая система сердца. Обозначения 0-4 те же, что на рис. 14.4.
1 В англоязычной литературе такой тип аритмий известен как reentry arrhythmias (от англ. reentry - повторное поступление).
2 Эффективный рефрактерный период характеризуется минимальным временным интервалом между двумя стимулами, вызывающими распространяющееся возбуждение (потенциалы действия).

Рис. 14.4. Влияние хинидина сульфата на потенциалы действия изолированного волокна Пуркинье с искусственно вызванным автоматизмом (схема).
ЭРП - эффективный рефрактерный период; 0-4 - фазы потенциала действия: 0 - быстрая деполяризация; 1-3 - фазы реполяризации; 4 - медленная (диастолическая) деполяризация.

Рис. 14.5. Развитие аритмии по механизму «повторного входа» (б) и принципы ее лече ния (в, г).
нием фазы реполяризации (фазы 2 и 3) и соответственно длительности потенциала действия. На ЭКГ наблюдается уменьшение интервала Q-T.
Следует, однако, учитывать, что нарушения ритма сердечных сокращений могут быть связаны с изменением не только функционального состояния непосредственно миокарда и проводящей системы, но и тонуса адренергической и холинергической иннервации сердца (табл. 14.4).
Таблица 14.4. Основная направленность действия ряда противоаритмических средств

Примечание. АР - адренорецепторы; ХР - холинорецепторы; ч.а. - частичный агонист. Количеством плюсов отмечена относительная блокирующая активность веществ.
Нейрогенная стимуляция β1-адренорецепторов сердца ускоряет диастолическую деполяризацию (фаза 4), что приводит к учащению ритма. Проводимость в синусно-предсердном и предсердно-желудочковом узлах улучшается. Укорачиваются реполяризация и продолжительность потенциала действия. Все это способствует развитию аритмий. Не менее важное значение имеют циркулирующие в крови катехоламины, избыточные концентрации которых могут вызывать аритмии. Нарушения ритма возникают и при сенсибилизации адренорецепто- ров сердца к катехоламинам (например, при гипертиреозе).
Холинергическая иннервация (ацетилхолин) оказывает на многие параметры противоположное влияние. Так, автоматизм синусно-предсердного и предсердно-желудочкового узлов снижается и ритм сердечных сокращений урежается. Проводимость в предсердно-желудочковом узле ухудшается, его эффективный рефрактерный период удлиняется, может развиться предсердно-желудочковый блок. В клетках предсердий облегчается проводимость, укорачивается эффективный рефрактерный период. При возбуждении блуждающего нерва наиболее выраженно изменяется функция синусно-предсердного узла.
Таким образом, в формировании различных типов аритмий принимают участие как кардиальные, так и экстракардиальные механизмы.
Для лечения и профилактики нарушений ритма сердечных сокращений используют многие лекарственные средства. Исходя из основной направленности и механизма действия, их можно систематизировать следующим образом1.
I. Средства, преимущественно блокирующие ионные каналы кардиомиоцитов (проводящей системы сердца и сократительного миокарда)
1. Средства, блокирующие натриевые каналы (мембраностабилизирующие средства; группа I)
Подгруппа IA (хинидин и хинидиноподобные средства):
Хинидина сульфат Дизопирамид Новокаинамид Аймалин
Подгруппа IB:
Лидокаин Дифенин
Подгруппа IC
Флекаинид Пропафенон Этмозин Этацизин
2. Средства, блокирующие кальциевые каналы L-типа (группа IV) Верапамил Дилтиазем
3. Средства, блокирующие калиевые каналы (средства, увеличивающие продолжительность реполяризации и соответственно потенциала действия; группа III)
Амиодарон Орнид Соталол
4. Средства, избирательно блокирующие Na+-K+ входящий ток (If) синусного узла (группа V; брадикардические средства)
Ивабрадин Фалипамил Алинидин
СРЕДСТВА, ПРЕИМУЩЕСТВЕННО БЛОКИРУЮЩИЕ ИОННЫЕ КАНАЛЫ КАРДИОМИОЦИТОВ (ПРОВОДЯЩЕЙ СИСТЕМЫ СЕРДЦА И СОКРАТИТЕЛЬНОГО МИОКАРДА)
Фармакотерапевтический эффект таких противоаритмических средств основан на их способности подавлять автоматизм, влиять на проводимость, пролонгировать эффективный рефрактерный период. Изменение этих параметров обусловлено воздействием препаратов на ионные каналы, что может дополняться их воздействием на рецепторы сердца, иннервируемые адренергическими или холинергическими нервами (табл. 14.4).
Автоматизм клеток сердца под влиянием противоаритмических средств данной группы снижается. В основном это связано с удлинением диастолической деполяризации (фаза 4) и отчасти - с некоторым повышением порога возбуди- мости. Все это препятствует чрезмерной активации естественного водителя ритма и появлению эктопических очагов возбуждения.
Многие противоаритмические средства, например хинидин, новокаинамид, угнетают проводимость (в проводящей системе сердца, в предсердиях, желудочках). Это приводит к снижению скорости быстрой деполяризации (фаза 0) и замедлению процесса деполяризации-реполяризации в целом. На ЭКГ снижение
проводимости отражается удлинением интервала P-Q и желудочкового комплекса. Положительное влияние угнетения проводимости проявляется, в частности, в том, что угнетение предсердно-желудочковой проводимости при тахиаритмиях предсердий (например, при трепетаниях, мерцаниях) лимитирует распространение патологически высоких ритмов от предсердий к желудочкам, что имеет важное значение для купирования таких аритмий. Способность угнетать проводимость оказывает положительный эффект и при аритмиях, развивающихся по механизму «повторного входа». В этом случае односторонний блок превращается в двусторонний (см. рис. 14.5).
Важным параметром является также эффективный рефрактерный период. Под влиянием многих противоаритмических препаратов (хинидина, хинидиноподобных средств и др.) он увеличивается. Обычно (хотя и необязательно) это связано с увеличением продолжительности потенциала действия, т.е. с замедлением процесса реполяризации. Совершенно очевидно, что удлинение эффективного рефрактерного периода ограничивает частоту распространяющихся стимулов, что сказывается на течении аритмии.
Возбудимость (определяется по порогу потенциала действия) многие препараты снижают.
При использовании противоаритмических средств следует учитывать, что многие из них угнетают сократимость миокарда. Выраженное угнетение сократимости миокарда, естественно, отрицательно сказывается на функциональном состоянии сердца, особенно при сердечной недостаточности.
При оценке кардиотропных эффектов противоаритмических средств нельзя не учитывать способность некоторых из них изменять экстракардиальные влияния, реализуемые через блуждающие и симпатические нервы. Так, известно, что угнетение передачи с блуждающего нерва на сердце (за счет м-холиноблокирующего действия) повышает синусный ритм, улучшает проводимость в предсердно-желудочковом узле и укорачивает его рефрактерный период. В частности, если речь идет о хинидине и ряде хинидиноподобных веществ, то их ваголитический эффект ослабляет те влияния на сердце, которые обеспечивают противоаритмическое действие этих веществ (см. ниже). Что касается угнетающего влияния отдельных противоаритмических средств из группы блокаторов ионных каналов на адренергическую иннервацию, то оно выражено у них мало (за исключением амиодарона) и не сказывается на основном противоаритмическом эффекте либо незначительно усиливает его.
Таким образом, действие противоаритмических средств может быть связано не только с непосредственным влиянием на ионные каналы кардиомиоцитов, но и с изменением их эфферентной иннервации, что следует учитывать при назначении препаратов и оценке их эффективности.
а) Средства, блокирующие натриевые каналы (мембраностабилизирующие средства; группа I)
Наиболее типичным представителем противоаритмических средств подгруппы IА является алкалоид коры хинного дерева хинидин (является правовращающим изомером хинина). В медицинской практике используют хинидина суль- ф а т. Блокируя натриевые каналы, хинидин уменьшает входящий натриевый ток, генерирующий потенциал действия (фаза 0). Хинидин действует на все отделы сердца. Вследствие угнетения автоматизма, увеличения длительности реполяризации и соответственно потенциала действия и эффективного рефрактерного периода, а также снижения проводимости хинидин эффективен при аритмиях, свя-
занных с нарушением автоматизма и проводимости (табл. 14.5). На ЭКГ наблюдается небольшое удлинение P-R, QRS, Q-T.
Хинидин угнетает передачу возбуждения с блуждающего нерва на сердце (за счет м-холиноблокирующих свойств), а также несколько уменьшает кардиотропные симпатические (адренергические) влияния. Блокирующее воздействие на α-адренорецепторы проявляется также в отношении периферических сосудов (несколько снижается общее периферическое сопротивление). Следует учитывать, что хинидин заметно снижает

















