Многие металлы с положительным электродным потенциалом, образующие устойчивые оксидные пленки, не растворяются в какой-либо кислоте, а растворяются и травятся в смесях кислот. Данные смеси состоят из кислоты, обладающей ярко выраженными окислительными свойствами (HNO3, H2SO4, H2SeO4, HClO3, HClO4), и кислоты, анион которой образует устойчивые комплексные ионы с ионом металла (HCl, HF и т.д.).
Взаимодействие металла со смесями кислот происходит по реакции
Me + HF + HNO3 → H m-z [Me z +F m ] + NO + H2O. (4.25)
Металл окисляется, анион окислительной кислоты восстанавливается.
Золото, платиновые металлы, ниобий, тантал растворяют или травят в смесях кислот. Рассмотрим на примере палладия:
3Pd + 4HNO3 + 18 HCl → 3H2[PdCl6] + 4NO + 8H2O. (4.26)
7.1.5. Взаимодействие металлов с растворами щелочей. Взаимодействие металлов с растворами щелочей происходит по реакции
Me + NaOH + H2O → Na х [Me(OH) z ] + H2; (4.27)
Me - z 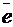 → Me z+ ; (4.28)
→ Me z+ ; (4.28)
восст.
2H2O + 2 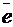 → 2OH- + H2 . (4.29)
→ 2OH- + H2 . (4.29)
окисл.
Данная реакция возможна, если электродный потенциал металла (φ 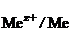 ) меньше потенциала водородного электрода в щелочной среде (φ
) меньше потенциала водородного электрода в щелочной среде (φ 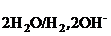 = –0,82 B) и оксид и гидроксид металла амфотерны.
= –0,82 B) и оксид и гидроксид металла амфотерны.
Взаимодействуют с растворами щелочей амфотерные металлы, электродные потенциалы которых меньше –0,82 В. К таким металлам относятся Zn, Al, Be, которые взаимодействуют с щелочными растворами по реакции:
Al + NaOH + H2O → Na3[Al(OH)6] + H2; (4.30)
Na[Al(OH)4]
Be, Zn + NaOH + H2O → Na2[Zn(OH)4] + H2. (4.31)
Na2[Be(OH)4]
Магний и титан не образуют комплексных соединений с гидроксид-ионом. При взаимодействии магния со щелочами продуктом реакции, кроме водорода, является Mg(OH)2, а титана – TiO (см. диаграмму Пурбе).
Взаимодействие металлов с окислителями в расплавах
Щелочей
Ряд металлов, оксиды и гидроксиды которых амфотерны или обладают кислотными свойствами (Re, Mo, W, Ru, Os) взаимодействуют с окислителями в расплавах щелочей. В качестве окислителей используются соли (нитраты, хлораты, перхлораты, пероксиды). При взаимодействии металлов с такими смесями металл переходит в расплав в виде аниона соли щелочного металла.
Например, платиновые металлы (Ru, Os) окисляются в расплавленной окислительно-щелочной смеси смеси КОН и KNO3 по реакции
Ru + 4KOH + 6 KNO3 → 5K2RuO4 + 3N2 + 2H2O. (4.32)
В данной реакции окислитель KNO3 восстанавливается до низшей степени окисления (N 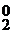 ). Рутений окисляется и связывается в анионы типа K
). Рутений окисляется и связывается в анионы типа K 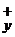 [MeO x ] y-, которые растворимы и не мешают дальнейшему окислению металла.
[MeO x ] y-, которые растворимы и не мешают дальнейшему окислению металла.
Коррозия – необратимое самопроизвольное разрушение металлов и сплавов вследствие химического или электрохи-мического воздействия среды. Закономерности химической и электрохимической коррозии металлов и основные методы защиты представлены на рис. 4.1 – 4.3.
Химическая стойкость металла характеризуется показателями скорости его коррозии – массовым, объемным, глубинным.
Массовый показатель Km определяется соотношением
 , (4.33)
, (4.33)
где m 0и m 1 – массы образующегося металла до и после коррозии в течение времени τ; S 0 – площадь образца до коррозии. Размерность Кm – г/м2·ч.
Глубинный показатель
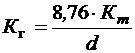 , (4.34)
, (4.34)
где d – плотность металла. Размерность К г – мм/год.
По (4.34) оценивают баллы коррозионной стойкости (см. табл. П 2.1).
По механизму протекания различают химическую и электрохи-мическую коррозию.
Химическая или газовая коррозия наблюдается при взаимодействии металлов с сухими газами, органическими веществами в отсутствие электролитов:
х Ме + y О2 = Me x O2 y. (4.35)
Для оценки термодинамической вероятности реакции (4.35) определяют значение Δ G при данном значении парциального давления окислителя
Δ G = 4,57· Т (lg К + lg 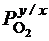 ), (4.36)
), (4.36)
где К – константа диссоциации оксида.
Коррозия наблюдается, если
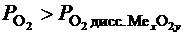 . (4.37)
. (4.37)
Кинетика химической коррозии зависит от свойств оксидной пленки, образующейся на поверхности металла. К поверхности пленки подходит молекулярный кислород, происходят его адсорбция и атомизация. От поверхности металла атомы кислорода перемещаются вглубь пленки оксида, а им навстречу – ионы металла и электроны. В пленке в одном акте происходит ионизация кислорода и образование химического соединения с металлом.
Для характеристики защитной способности образующейся оксидной пленки применяется коэффициент α
α = 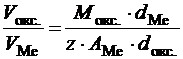 , (4.38)
, (4.38)
где V окс., V Me – мольные объемы; М окс. – молекулярная масса оксида; А Me – атомная масса металла; d Me, d окс. – плотности; z – число атомов металла в молекуле оксида.
Низкие значения коэффициента α < 1 не обеспечивают получения плотных пленок и защиты от коррозии, что достигается только при α = 1, 0 – 2,5; более высокие α ведут к высоким внутрен-ним напряжениям, растрескиванию и отслаиванию оксидов.
Широко применяемый метод защиты от газовой коррозии – жаростойкое легирование – исходит из того, что сродство к кислоро-ду у легирующего элемента должно быть больше, чем у защищае-мого:
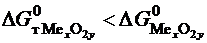 ,
,
а радиус атома – меньше: r легир < ri. В этом случае на поверхности формируются защитные оксиды, например, ВеО при добавлении
в медь 1 % бериллия (Ве).
Химическую коррозию предотвращают, насыщая поверхност-ный слой диффузионным покрытием, например, алюминиевым (алитирование), а также плакированием, нанесением жаростойких эмалей, тугоплавких карбидов, смешанных соединений покрытия
с основой – шпинелей типа NiСг2O4, NiFe2O4.
Детали, работающие при высоких температурах, можно защищать специальной защитной атмосферой: Н2 + N2 + H2O;
СО + СО2 + Н2 + СН4 + N2; СО + СО2 + N2; СО + СО2 + H2 + Н2О + N2.
Для уменьшения газовой коррозии применяют сжигание топлива с недостатком воздуха, используют защитные обмазки и др.
Электрохимическая коррозия протекает при наличии на поверхности металла слоя электролита (растворов солей, кислот или щелочей, атмосферной влаги в почве и т. п.). Сущность электро-химической коррозии заключается в том, что процесс окисления сопровождается полным удалением валентных электронов его атома и передачей их другой частице – деполяризатору (Н+, О2). Термо-динамическая возможность электрохимической коррозии опреде-ляется соотношением
Δ G 0 = – zF ·ЭДС < 0, (4.39)
где ЭДС =  > 0.
> 0.
Процессы окисления металла (анодный) и восстановления деполяризатора (катодный) могут протекать на одном и том же участке детали, но в различные моменты времени.
Hапpимер, при атмосферной коррозии с кислородной деполяризацией происходит анодное окисление железа
Fe – 2 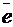 = Fe2+ (4.40)
= Fe2+ (4.40)
и катодное восстановление кислорода
О2 +2Н2О + 4 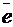 = 4OН
= 4OН  (при рН
(при рН  7); (4.41)
7); (4.41)
О2 + 4Н+ + 4 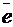 = 2Н2О (при рН < 7). (4.42)
= 2Н2О (при рН < 7). (4.42)
Последний процесс протекает преимущественно на участках с минимальным перенапряжением кислорода, например, на включениях углерода и никеля в стали, и его скорость зависит от возможностей для диффузии кислорода через пленку электролита.
В растворах электролитов в роли окислителя при коррозии может выступать ион водорода или вода:
2Н+ + 2 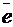 = Н2 (рН < 7); (4.43)
= Н2 (рН < 7); (4.43)
2Н2О + 2 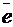 = 2ОН
= 2ОН  + Н2 (рН
+ Н2 (рН  7). (4.44)
7). (4.44)
Для реакций (4.43), (4.44) механизм процесса определяется преимущественно стадией присоединения электрона к иону Н+.
Для защиты от электрохимической коррозии используют различные методы, например, рациональное конструирование, заключающееся в подборе коррозионностойких материалов, а для случая контакта двух металлов необходимо предусмотреть, чтобы их электродные потенциалы не различались значительно.
Кроме того, конструкция деталей не должна допускать участков, где может скапливаться влага.
Другой метод – электрохимическая защита; в случае одной из ее распространенных разновидностей – протекторной защиты – вместо анодного участка создают как бы новый, введя в контакт с защищаемым металлом более отрицательный металл, по сравнению с которым прежний анод становится катодом. Этой же цели добиваются, подключив защищаемую деталь к отрицательному полюсу внешнего источника тока. Для нержавеющих сталей в кислотах применяют положительную поляризацию в области потенциалов, отвечающих пассивации.
Для уменьшения скорости электрохимической коррозии целесообразно проводить обработку среды путем уменьшения концентрации деполяризатора за счет нейтрализации кислых сред или удаления кислорода, например, по реакции
3Fe + 2O2 = Fe3O4. (4.45)
Замедлители коррозии – ингибиторы вводят в коррозионную среду, например, при сернокислотном дотравливании окалины (после предварительной обработки в расплаве 80 % NaOH + 20 % NaNO3 при 723 К в течение 20 мин с последующим охлаждением в воде) с нержавеющих сталей типа Х18Н9 добавка 5-10 кг/м3 NaCl в травильный раствор (18 % H2SO4 при 343 К) ускоряет удаление окалины, уменьшает коррозионные потери стали и улучшает качество поверхности протравленного металла.
Галоидные ионы, адсорбируясь на поверхности металла, образуют хемосорбционный слой, тормозящий протекание и катодного и анодного процессов в равной степени. Однако повышение концентрации этих ионов сверх указанных выше пределов может способствовать ускорению процесса растворения металла.
Анодные замедлители коррозии, в первую очередь окислители, большей частью обладают пассивирующими свойствами. Принцип торможения коррозии сводится к тому, что они уменьшают скорость перехода ионов металла в раствор или уменьшают анодные участки за счет изоляции их нерастворимыми пленками, часто оксидными. Однако поскольку анодные замедлители коррозии – окислители, в некоторых случаях они могут усиливать коррозию, являясь катодными ускорителями коррозии, что учитывается при выборе как ингибиторов, так и условий их применения.
Хроматы и бихроматы тормозят преимущественно анодный процесс и незначительно катодный, в значительной мере пассивируют Fe, Al, Zn, Cu. Добавка в водопроводную воду 0,1 % K2Cr2O7 резко снижает скорость коррозии углеродистой стали и алюминия. В присутствии в воде сильных активаторов коррозии, например, хлористых солей, концентрацию K2Cr2O7 следует увеличить до 2-3 %. К анодным замедлителям относят также NaNO3, NaNO2, Na2SiO3. Нитрит натрия значительно уменьшает скорость коррозии стали и некоторых цветных металлов в растворах ряда солей, в том числе, и в морской воде. Действие нитрита натрия сказывается в том, что ион NO 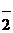 окисляет продукты коррозии металлов – соединения Fe2+ или Sn2+ – в оксидные соединения, которые осаждаются на поверхности металла. Добавка NaNO2 2 кг/м3 существенно уменьшает коррозию стали в растворе 7,5 кг/м3 NaCl. При длительном хранении стальных деталей, в том числе с хромовыми и никелевыми покрытиями, их рекомендуется упаковывать в бумагу, пропитанную 10-15 % раствором NaNO2.
окисляет продукты коррозии металлов – соединения Fe2+ или Sn2+ – в оксидные соединения, которые осаждаются на поверхности металла. Добавка NaNO2 2 кг/м3 существенно уменьшает коррозию стали в растворе 7,5 кг/м3 NaCl. При длительном хранении стальных деталей, в том числе с хромовыми и никелевыми покрытиями, их рекомендуется упаковывать в бумагу, пропитанную 10-15 % раствором NaNO2.
Защитное действие Na2SiO3 проявляется при коррозии стали в нейтральных водных растворах и обусловлено образованием на поверхности металла защитной пленки.
Известны также анодные замедлители вторичного действия, образующие на анодных участках нерастворимые продукты коррозии. Например, фосфатные соли образуют нерастворимые фосфаты железа.
Некоторые ингибиторы избирательно тормозят катодный процесс по одному из следующих путей: 1) торможением отдельных стадий катодного процесса; 2) сокращением площади катодных участков. В процессах коррозии металлов, протекающих с водород-ной деполяризацией, торможение катодной реакции восстановления водорода достигается путем повышения перенапряжения водорода добавкой в раствор солей AsCl3, Bi2(SO4)3, катионы которых восстанавливаются на микрокатодах и повышают перенапряжение водорода. Сокращение площади катодных участков с целью уменьшения скорости коррозии достигается добавлением Са(НСО3)2 в подщелоченную среду (у катодных участков корродирующей поверхности металлов), в результате чего образуется нерастворимое соединение СаСО3, осаждающееся и изолирующее часть поверхности от действия электролита. Катодные ингибиторы совершенно безопасны, так как никогда не приводят к увеличению интенсивности коррозии.
Наиболее эффективными ингибиторами в нейтральных и щелочных средах являются неорганические вещества, в кислых агрессивных средах – органические, например, амины, альдегиды, гетероциклические соединения. Механизм их действия в основном сводится к адсорбции на катодных участках и повышению перенапряжения водорода; некоторые органические вещества адсорбируются на анодных участках и затормаживают протекание процесса коррозии. Соли аминов и спиртов используют и как летучие ингибиторы коррозии, парами которых насыщается воздух в складских помещениях, контейнерах.
Наиболее распространенный метод защиты от коррозии в машиностроении – применение защитных покрытий.
Металлические покрытия подразделяются на катодные и анодные. В случае катодного покрытия, например, для стали – Au, Ag, Cu, Ni; 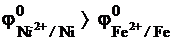 и при повреждении покрытия коррозия основы ускоряется. Для анодных покрытий (Zn, A1, Mg), например, в случае цинка:
и при повреждении покрытия коррозия основы ускоряется. Для анодных покрытий (Zn, A1, Mg), например, в случае цинка:  , при повреждении покрытия коррозия основы не происходит и обеспечивается не только механическая, но и химическая защита.
, при повреждении покрытия коррозия основы не происходит и обеспечивается не только механическая, но и химическая защита.
Наряду с металлическими покрытиями применяют формирование покрытий химическими соединениями металлов – оксидирование алюминия, получение фосфатных пленок FeHPO4, нанесение органических покрытий – лаками, смолами, неоргани-ческих – эмалями.
По условию и назначению методы лабораторных испытаний материала на коррозионную стойкость в среде электролита подразделяют на общие, специальные и электрохимические.
Общие методы основаны преимущественно на гравиметрии (на убыли веса испытуемого образца с определенной площадью), объемных методах (на измерениях объемов выделившихся при коррозии газов).
При использовании электрохимических методов измеряются величины электродных потенциалов металла или сплавов без тока, а для полной характеристики кинетики процесса коррозии данного материала в электролите необходимо снимать поляризационные кривые гальваностатическим методом.
При измерении потенциалов без тока в электролите необходимо собрать электрохимическую систему, где исследуемый материал в виде электрода с определенной площадью соединяется проводником первого рoда с электродом сравнения. Значения стационарного потенциала позволяют судить о влиянии природы и концентрации электролита на активацию, пассивацию металла.
ОТВЕТИТЬ НА КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Какую роль играют металлы в окислительно-восстано-вительных процессах?
2. Какими параметрами можно оценить химическую активность металла как элемента и простого вещества?
3. Какими свойствами обладают оксиды металлов в разных степенях окисления?
4. Оксиды какого металла (никеля, хрома, меди) имеют большую прочность? Используйте значения D Н 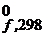 (табл. П 1.7).
(табл. П 1.7).
5. Как оценить термодинамическую вероятность взаимодействия металлов с водой, кислотами, диссоциирующими с образованием Н+ (Н3О)+ и растворами щелочей?
6. Какие продукты реакции следует ожидать при взаимодействии различных металлов с азотной кислотой и почему? Как влияет на это концентрация раствора?
7. Какие продукты следует ожидать при взаимодействии металлов с разбавленной и концентрированной серной кислотой? Объясните ответ.
8. Какой процесс называют коррозией металлов?
9. Дайте характеристику показателям скорости коррозии металлов – массовому, объемному, глубинному.
10. Какие виды коррозии различают по механизму протекания?
11. В каких средах наблюдается химическая коррозия?
12. Как оценивается термодинамическая вероятность химической коррозии?
13. Как характеризует защитную способность образующейся
на поверхности металла оксидной пленки коэффициент α?
14. Расположите заданные металлы в порядке уменьшения стойкости против газовой коррозии, рассчитав коэффициент «α»
по данным табл. П 2.4:
l) Ag, Fe, W – для студентов по списку группы №1-4;
2) Al, Cu, Ti - №5-8;
3) Ве,Cr, Pt - №9-11;
4) Ва, Со, Pd – №12-14;
5) Са, Cd, Ni - №15-17;
6) Cd, Fe, Na - №18-20;
7) Са, Cu, Mg - №21-23;
8) Ва, Cr, Li - №24-26;
9) Ве, Са, К - №27-29;
10) W, Ti, Al - №30-32;
11) Pt, Ni, Ag - №33-36;
12) Рb, W, Ве - №37-40.
15. Опишите методы защиты металлов от химической коррозии.
16. Опишите механизм электрохимической коррозии металлов.
17. Как определяется термодинамическая вероятность электро-химической коррозии?
18. Какие процессы протекают при коррозии металла с кисло-родной деполяризацией?
19. Опишите особенности коррозии металла с водородной деполяризацией.
20. Дайте характеристику методам защиты металлов от электро-химической коррозии.
21. Какие из конструктивных решений (а, б) удачны в антикоррозионном отношении? Ответ подтвердите примерами возможных коррозионных процессов (рис. 4.11).
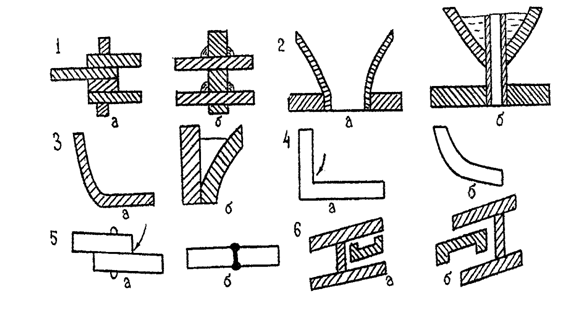
Рис. 4.11



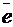 → Me z+ ; (4.28)
→ Me z+ ; (4.28)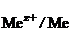 ) меньше потенциала водородного электрода в щелочной среде (φ
) меньше потенциала водородного электрода в щелочной среде (φ 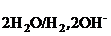 = –0,82 B) и оксид и гидроксид металла амфотерны.
= –0,82 B) и оксид и гидроксид металла амфотерны.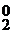 ). Рутений окисляется и связывается в анионы типа K
). Рутений окисляется и связывается в анионы типа K 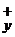 [MeO x ] y-, которые растворимы и не мешают дальнейшему окислению металла.
[MeO x ] y-, которые растворимы и не мешают дальнейшему окислению металла. , (4.33)
, (4.33)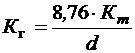 , (4.34)
, (4.34)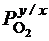 ), (4.36)
), (4.36)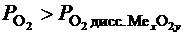 . (4.37)
. (4.37)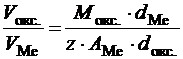 , (4.38)
, (4.38)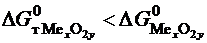 ,
, > 0.
> 0. (при рН
(при рН  7); (4.41)
7); (4.41)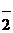 окисляет продукты коррозии металлов – соединения Fe2+ или Sn2+ – в оксидные соединения, которые осаждаются на поверхности металла. Добавка NaNO2 2 кг/м3 существенно уменьшает коррозию стали в растворе 7,5 кг/м3 NaCl. При длительном хранении стальных деталей, в том числе с хромовыми и никелевыми покрытиями, их рекомендуется упаковывать в бумагу, пропитанную 10-15 % раствором NaNO2.
окисляет продукты коррозии металлов – соединения Fe2+ или Sn2+ – в оксидные соединения, которые осаждаются на поверхности металла. Добавка NaNO2 2 кг/м3 существенно уменьшает коррозию стали в растворе 7,5 кг/м3 NaCl. При длительном хранении стальных деталей, в том числе с хромовыми и никелевыми покрытиями, их рекомендуется упаковывать в бумагу, пропитанную 10-15 % раствором NaNO2.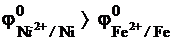 и при повреждении покрытия коррозия основы ускоряется. Для анодных покрытий (Zn, A1, Mg), например, в случае цинка:
и при повреждении покрытия коррозия основы ускоряется. Для анодных покрытий (Zn, A1, Mg), например, в случае цинка:  , при повреждении покрытия коррозия основы не происходит и обеспечивается не только механическая, но и химическая защита.
, при повреждении покрытия коррозия основы не происходит и обеспечивается не только механическая, но и химическая защита. (табл. П 1.7).
(табл. П 1.7).


