

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

Состав сооружений: решетки и песколовки: Решетки – это первое устройство в схеме очистных сооружений. Они представляют...

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

Состав сооружений: решетки и песколовки: Решетки – это первое устройство в схеме очистных сооружений. Они представляют...
Топ:
Оценка эффективности инструментов коммуникационной политики: Внешние коммуникации - обмен информацией между организацией и её внешней средой...
Определение места расположения распределительного центра: Фирма реализует продукцию на рынках сбыта и имеет постоянных поставщиков в разных регионах. Увеличение объема продаж...
Особенности труда и отдыха в условиях низких температур: К работам при низких температурах на открытом воздухе и в не отапливаемых помещениях допускаются лица не моложе 18 лет, прошедшие...
Интересное:
Лечение прогрессирующих форм рака: Одним из наиболее важных достижений экспериментальной химиотерапии опухолей, начатой в 60-х и реализованной в 70-х годах, является...
Средства для ингаляционного наркоза: Наркоз наступает в результате вдыхания (ингаляции) средств, которое осуществляют или с помощью маски...
Инженерная защита территорий, зданий и сооружений от опасных геологических процессов: Изучение оползневых явлений, оценка устойчивости склонов и проектирование противооползневых сооружений — актуальнейшие задачи, стоящие перед отечественными...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
НЕФТЕГАЗОВЫЙ КОМПЛЕКС
Методические указания для самостоятельной работы
для подготовки и повышения квалификации рабочих по профессии "Лаборант химического анализа"
Тюмень 2013
Нефтегазовый комплекс: метод. указ. для подготовки и повышения квалификации рабочих по профессии "Лаборант химического анализа" / сост. Л.В. Трушкова; Тюменский государственный нефтегазовый университет.- Тюмень: Издательский центр БИК ТюмГНГУ 2013.- 45с.
Аннотация
Методические указания "Нефтегазовый комплекс" предназначены для подготовки и повышения квалификации рабочих по профессии "Лаборант химического анализа"
Рассмотрены вопросы состава и свойств нефтей, производственно-проектной оценки качества нефтей и направлений её переработки; первичной переработки нефти на установках АТ, ВТ. Приведена оценка качества прямогонных фракций нефти и их использования, рассмотрены вторичные процессы переработки нефти.
Рассмотрены вопросы состава, основных свойств и показателей качества природных газов.
ОГЛАВЛЕНИЕ
Тема 1. Подготовка нефти и газового конденсата к транспорту и переработке………………………………4
1.1. Балластные компоненты нефти……………………………………4
1.2. Водонефтяная эмульсия. Методы разрушения
водонефтяных эмульсий………………………………………….5
1.3. Требования, предъявляемые к нефти перед транспортом. Товарная нефть………………………………………………………....8
Тема 2. Фракционирование нефти. Определение потенциального выхода фракций………………………10
2.1.Определение потенциального содержания дистиллятных продуктов перегонки нефти с помощью ИТК………………………12
|
|
2.2.Технологическая классификация нефти.
Технологический индекс……………………………………………13
Тема 3. Процессы ПЕРВИЧНОЙ переработки нефти……..14 3.1. Первичная перегонка нефти на промышленных установках …………….15 3.2. Классификация установок первичной перегонки нефти…………….17 3.3. Продукты первичной перегонки нефти ………………………………..19
3.4. Установки вакуумной перегонки мазута……………………………22
ТЕМА 4. ОСНОВНЫЕ НАПРАВЛЕНИЯ ПЕРЕРАБОТКИ НЕФТИ 24
4.1. Выбор варианта переработки нефти……………………………….24
ТЕМА5. ОСНОВНЫЕ СВОЙСТВА ПРИРОДНЫХ ГАЗОВ…………26
ТЕМА 6. ПОДГОТОВКА И ПЕРЕРАБОТКА ГАЗОВ………………..34
ТЕМА 7. МЕТОДЫ АНАЛИЗА ОСНОВНЫХ ПОКАЗАТЕЛЕЙ КАЧЕСТВА ПРИРОДНОГО ГАЗА………………………………………37

 Литература…………………………………………………………………45
Литература…………………………………………………………………45
ВВЕДЕНИЕ
Понятие «топливо» объединяет вещества, выделяющие (в результате тех или иных преобразований) энергию, которая может быть использована.
Таким образом, энергетическим топливом называются горючие вешества, которые экономически целесообразно использовать для получения в промышленных целях большого количества теплоты. Это является основным требованием, предъявляемым к топливу.
Основными видами органического топлива являются органические вещества: дрова, близкие к ним растительные материалы, торф, уголь, сланцы, нефть и природные газы.
По способу получения топливо подразделяют на природное и искусственное.
Природным топливом являются дрова, уголь, сланцы, торф, нефть, газовые конденсаты и природные газы.
К искусственному относится топливо, полученное в результате термической переработки природного топлива: кокс; брикеты угля; древесный уголь; мазут; бензин; керосин; солярное масло; дизельное топливо; доменный и коксовый генераторные газы; газы подземной газификации.
Топливо также подразделяют на твердое (дрова, уголь, сланцы, торф), жидкое (нефть, мазут, бензин, керосин, солярное масло, дизельное топливо) и газовое (природные газы, искусственные газы и газы подземной газификации).
|
|
Тема 1. Подготовка нефти и газового конденсата к транспорту и переработке
Нефть приготавливается к переработке в два этапа – на нефтепромысле и на нефтеперерабатывающем заводе. В задачу подготовки к переработке на обоих этапах входит удаление от нефти примесей, которые выходят из скважины вместе с нею: попутного нефтяного газа, механических примесей, воды и минеральных солей.
Балластные компоненты нефти
Добываемая из нефтепромысловых скважин нефть, строго говоря, нефтью является лишь частично, поскольку вместе с ней из скважины выносится: газ, пластовая вода, содержащая минеральные соли и механические примеси. Углеводородный газ, называемый попутным газом, растворен в нефти и механически смешан с нею, количество его составляет от 10 до 300 м3/т нефти и называется газовым фактором скважины.
Содержание пластовой воды в нефти колеблется от 5 до 90% на нефть и называется обводненностью скважины. Причем чем больше эксплуатируется скважина, тем больше воды содержит добываемая нефть в виде эмульсии.
Пластовая вода сильно минерализирована. В добываемой из скважин нефти общее содержание минеральных солей составляет от 3000 до 12000 мг/л.
Механические примеси (до 1% на нефть) состоят из песчинок, пластовой породы, кристалликов минеральных солей, окалины и др.
Все перечисленные примеси являются балластными компонентами нефти, ухудшают ее качество и подлежат удалению. Такую «сырую» нефть нельзя транспортировать и перерабатывать на НПЗ без тщательной подготовки по следующим причинам:
1) высокое содержание растворенного газа в нефти отрицательно в ввиду того, что:
а) увеличивается давление насыщенных паров нефти (Рн.к.), что снижает безопасность эксплуатации нефтепроводов;
б) увеличиваются потери легких компонентов нефти (при транспорте даже с допустимым Рн.n. потери нефти составляют 2-4% нас.;
в) легкие компоненты попутного газа (С2-С4) ухудшают ректификацию нефти.
2) Присутствие пластовой воды в нефти удорожает ее транспортировку по трубопроводам (увеличивается вязкость нефти) и увеличивает энергозатраты на ее испарение и конденсацию при переработке.
3) Наличие в нефти минеральных солей (особенно хлоридов Ca, Mg, Na и др.) придает ей высокие коррозионноактивные свойства, поскольку при повышенных температурах (выше 1000С) в присутствии воды они подвергаются гидролизу с образованием хлороводородной кислоты, разрушающей стальное оборудование:
|
|

 MgCl2+H2O MgOHCl+ HCl
MgCl2+H2O MgOHCl+ HCl

 2HCl + FeS FeCl2 + H2S
2HCl + FeS FeCl2 + H2S
 H2S+Fe FeS + H2.
H2S+Fe FeS + H2.
4) При большом содержании механических примесей усиливается износ труб и образование отложений в нефтеаппаратах, что приводит к снижению коэффициента теплоотдачи.
На нефтепромыслах эксплуатируются различные системы сбора и подготовки нефти. Используется герметизированная схема сбора и подготовки нефти, включающая следующие этапы:
I. Разгазирование нефти (дегазация). Попутный нефтяной газ отделяют в сепараторах высокого и низкого давления гравитационным разделением. Полного разделения при этом достичь не удается, и в нефти остается в растворенном состоянии 0,5-1,5% углеводородов до бутана включительно.
Эту растворенную часть газа извлекают после отделения на промысле остальных примесей на стадии стабилизации нефти
II. Обезвоживание и обессоливание (установки подготовки нефти). В основе процесса обезвоживания и обессоливания лежит разрушение (дестабилизация нефтяных эмульсий), образующихся в результате контакта нефти с водой, закачиваемой в пласт для поддержания пластового давления.
III. Стабилизация нефти (при высоком давлении растворенного газа).
IV. Сортировка и смешение нефти. Оценка качества нефти.
Водонефтяных эмульсий
Вода и нефть, взаимно нерастворимы (лиофобны) и при интенсивном перемешивании образуют водонефтяную дисперсную смесь (эмульсию «вода в нефти»).
 Образуется такая эмульсия за счет турбулизации водонефтяной смеси при движении ее по стволу скважины, через задвижки и штуцеры и по трубопроводам от скважины до узла подготовки нефти. Структура водонефтяной эмульсии схематично показана на рис. 1
Образуется такая эмульсия за счет турбулизации водонефтяной смеси при движении ее по стволу скважины, через задвижки и штуцеры и по трубопроводам от скважины до узла подготовки нефти. Структура водонефтяной эмульсии схематично показана на рис. 1
|
Капли (глобулы) диспергированной воды имеют диаметр (dk) от 0,1 до 1000 мкм, и каждая из них окружена адсорбированной на поверхности глобул сольватной оболочкой – концентратом высокомолекулярных полярных веществ нефти (смолисто-асфальтовых веществ), называемых эмульгаторами. Наличие этого сольватного слоя толщиной σ создает как бы защитную «скорлупу» вокруг каждой глобулы воды, препятствующую слиянию (коалесценции) глобул даже при самопроизвольном столкновении. Интенсивность адсорбции эмульгаторов на поверхности глобул воды определяется тем, что дисперсная фаза (вода) при указанных выше размерах капель имеет огромную межфазную поверхность (десятки квадратных метров в литре нефти). На такой поверхности может адсорбироваться большое количество веществ, стабилизирующих эмульсию.
|
|
Устойчивость эмульсий зависит от следующих факторов:
1. Средний диаметр глобул воды.
Чем меньше диаметр глобулы, тем медленнее будет глобула оседать в массе нефти и тем более устойчивым будет эмульсия. Согласно формуле Стокса скорость оседания частиц (ω0, м/с) в спокойной жидкости (Re<1) описывается формулой:
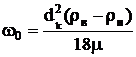 , где (1)
, где (1)
dk – диаметр капли, м
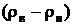 - плотность воды и нефти, кг/м3
- плотность воды и нефти, кг/м3
μ – динамическая вязкость нефти, Па·с.
 Для того чтобы снизить устойчивость эмульсии и облегчить отделение от нее воды, необходимо, как следует из формулы (1), укрупнить капли воды.
Для того чтобы снизить устойчивость эмульсии и облегчить отделение от нее воды, необходимо, как следует из формулы (1), укрупнить капли воды.

 2. Время «жизни» эмульсии.
2. Время «жизни» эмульсии.
 Чем больше прошло времени с момента образования эмульсии, тем толще сольватный слой. Имеет значение и характер гидродинамических воздействий на поток нефти; чем их больше тем меньше диаметр капель, т.е. устойчивее эмульсия.
Чем больше прошло времени с момента образования эмульсии, тем толще сольватный слой. Имеет значение и характер гидродинамических воздействий на поток нефти; чем их больше тем меньше диаметр капель, т.е. устойчивее эмульсия.

3. Физико-химических свойств нефти и химического состава эмульгированнной воды.
 Из формулы 1 следует, что скорость осаждения капель при прочих равных условиях зависит от плотности нефти (чем больше ρн, тем меньше ω0).
Из формулы 1 следует, что скорость осаждения капель при прочих равных условиях зависит от плотности нефти (чем больше ρн, тем меньше ω0).
 Обратно пропорционально влияет на скорость осаждения капель воды вязкость: снижение ее (например, за счет повышения температуры) также увеличивает скорость осаждения.
Обратно пропорционально влияет на скорость осаждения капель воды вязкость: снижение ее (например, за счет повышения температуры) также увеличивает скорость осаждения.
 4. Температура эмульсии.
4. Температура эмульсии.
 Она определяет плотность и вязкость нефти. Кроме того, с повышением температуры меняются состав и толщина сольватного слоя вокруг глобул воды (за счет увеличения растворимости в нефти).
Она определяет плотность и вязкость нефти. Кроме того, с повышением температуры меняются состав и толщина сольватного слоя вокруг глобул воды (за счет увеличения растворимости в нефти).
Требования, предъявляемые к нефти перед транспортом. Товарная нефть
В соответствии с ГОСТР51858-2002 условное обозначение товарной нефти, поставляемой в магистральные нефтепроводы, состоит из четырех цифр:
Класс нефти (по содержанию серы).
Тип нефти (по плотности, а при поставке на экспорт – дополнительно по выходу фракций и массовых долей парафина).
Группа нефти (по степени промысловой подготовки).
Вид нефти (по содержанию сероводорода и легких меркаптанов).
По этим признакам регламентированы следующие классификационные нормы:
|
|
Класс нефти (по содержанию серы, % мас.):
1) малосернистая (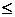 0,60);
0,60);
2) сернистая (0,61-1,80);
3) высокосернистая (1,81-3,50);
4) особо высокосернистая (> 3,50).
Тип нефти
| Показатель | (особо легкая) | (легкая) | (средняя) | (тяжелая) | (битуминозная) | |||||
| Россия | экспорт | Россия | экспорт | Россия | экспорт | Россия | экспорт | Россия | экспорт | |
| 1. Плотность, кг/м3, при температуре: 200С 150С | <830,0 <834,5 | 830,1-850,0 834,6-854,4 | 850,1-870,0 854,5-874,4 | 870,1-895,0 874,5-899,3 | >895,0 >899,3 | |||||
| 2.Выход фракции, % не менее, при температуре до: 2000С 3000С 3500С | - - - | - - - | - - - | - - - | - - - | - - - | - - - | |||
| 3. Массовая доля парафина, % не более | - | 6,0 | - | 6,0 | - | 6,0 | - | - | - | - |
Группа нефти
| Показатель | Норма для группы | |||
| 1. Массовая доля воды, % не более | 0,5 | 0,5 | 1,0 | |
| 2. Концентрация хлористых солей, мг/дм3, не более | ||||
| Показатель | ||||
| 3. Массовая доля механических примесей, % не более | 0,05 | 0,05 | 0,05 | |
| 4.Давление насыщеных паров, кПа, не более | 66,7 | 66,7 | 66,7 | |
| 5.Содержание хлорорганических соединений во фракции выкипа-ющей до 204оС, ppm, не более | ||||
Вид нефти
| Показатель | Норма для вида | |
| 1. Массовая доля сероводорода млн-1 (ррm), не более | ||
| 2. Массовая доля метил-и этилмеркаптанов, ррm, не более |
Рис.2.1. Кривая ИТК нефти
Технологический индекс
Предварительную оценку потенциальных возможностей нефтяного сырья можно осуществлять по комплексу показателей, входящих в технологическую классификацию нефти.
В основу индексации нефти (в соответствие с ГОСТ 38-01197-97) входят: содержание серы в нефти; потенциальное содержание фракций, выкипающих до 3500С; потенциальное содержание и качество базовых масел; содержание парафина в нефти.
Таблица 2.1
| Класс | Тип | Группа | Подгруппа | Вид | |
| Массовая доля серы в нефти, % мас. | Массовая доля фракций, выкипающих до 3500С | Потенциальное содержание базовых масел, % мас. | Индекс вязкости базовых масел | Массовая доля парафина в нефти, % мас. | |
| на нефть | на мазут | ||||
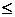 0,60 0,60
| 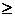 55,0 55,0
| 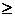 25,0 25,0
| 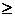 45,0 45,0
| >95 | 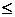 1,50 1,50
|
| 0,61-1,80 | 45,0-54,9 | 15,0-24,9 | 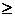 45,0 45,0
| 90-95 | 1,51-6,00 |
| >1,80 | <45,0 | 15,0-24,9 | 30,0-44,9 | 85-89,9 | >6,00 |
| <15,0 | <30,0 | <85 |
Используя эту классификацию для любой промышленной нефти
можно составить технологический индекс, состоящий из пяти цифр.
Например:
Усть-Балыкская нефть - 2.3.1.1.2
Самотлорская нефть - 2.1.3.1.2
Шаимская нефть - 1.1.2.1.2
Туймазинская нефть - 2.2.3.3.2
Ножовская нефть - 3.3.4.2.2
Шифр нефти является как бы ее технологическим паспортом, определяющим направление ее переработки (на топлива или масла), набор технологических процессов и ассортимент конечных продуктов.
Физические свойства газов
Важнейшими физическими свойствами газов являются молярная масса, плотность, вязкость и влажность. От свойств простых горючих и балластных газов, входящих в состав газового топлива, зависят его теплофизические свойства.
Молярная масса М, кг/кмоль — это отношение массы вещества к его количеству. Молярная масса некоторых простых газов дана в табл. 5
Плотность р, кг/м3 — это масса газа, приходящаяся на 1 м3 занимаемого им объема.
Вязкость — это способность газа оказывать сопротивление взаимному перемещению частиц.
В технических расчетах чаще применяют производную величину — коэффициент кинематической вязкости, м2/с:
υ = μ/ρ
Вязкость может быть определена лишь в условиях ламинарного течения газа. В условиях турбулентного движения вязкость перестает быть физической константой. В этом случае вместо вязкого сопротивления оперируют понятиями о турбулентном сопротивлении, турбулентной вязкости.
Таблица5.3
Значение коэффициентов вязкости некоторых газов при температуре 00С и давлении 101,3 кПа
| Газ | Коэффициент динамической вязкости μ, Па•с•10-6 | Коэффициент кинематической вязкости υ, (м2/с)•10-6 | Коэффициент С в формуле Сутсрленда |
| Водород | 8,35 | 93,8 | |
| Оксид углерода | 16,93 | 13,55 | |
| Метан | 10,55 | 14,71 | |
| Этан | 8,77 | 6,45 | |
| Пропан | 7,65 | 3,82 | |
| Бутан | 6,97 | 2,55 | |
| Пропилен | 7,82 | 4,11 | |
| Бутилен | 7,78 | 3,12 | |
| Диоксид углерода | 14,09 | 7,10 | |
| Кислород | 19,58 | 13,73 | |
| Азот | 16,93 | 13,55 | |
| Атмосферный воздух | 17,53 | 13,56 | |
| Сероводород | 11,82 | 7,68 | |
| Водяной пар при температуре 1000С | 8,7 | 14,80 |
Влажностью называется содержание в газе водяного пара.
Насыщение водяными парами газа может быть только до определенного предела, который зависит от температуры и давления. Температура, при которой газ, находящийся под определенным давлением, насыщен до предела водяными парами, называется точкой росы. Охлаждение от этой точки приводит к конденсации водяных паров.
Различают абсолютную, удельную и относительную влажность газа.
Абсолютной влажностью (влагосодержанием) газа называется количество или масса водяных паров, содержащихся в единице объема газа. Единица измерения абсолютной влажности — г/м3.
Удельной влажностью газа называется количество или масса водяного пара, приходящаяся на единицу массы влажного газа. Единица измерения удельной влажности — г/кг.
Относительной влажностью газа (степенью насыщения газа водяными парами) называется отношение абсолютной влажности газа к максимально возможной при заданных температуре и давлении. Относительную влажность газа φ выражают в процентах и определяют как отношение парциального давления содержащегося в газе водяного пара р к давлению насыщенного водяного пара Р при той же температуре:
φ = р/Р
Насыщенные пары углеводородных газов при данных температуре и давлении находятся в точке росы. При постоянном давлении и уменьшении температуры часть паров конденсируется. Изменение давления при постоянной температуре приводит к смещению равновесия точки росы, но состояние насыщенности паров сохраняется.
Точка росы имеет важное значение в двухфазных системах (пример таких систем — сжиженные газы, представляющие собой пропан-бутановые смеси). Для предотвращения конденсатообразования при естественном испарении в различных климатических зонах и в различные периоды года необходимо применять сжиженные газы с различным соотношением пропана и бутана.
Точки росы для пропан-бутановой смеси при давлении 3 кПа приведены в табл. 5.4.
Точка росы для углеводородных газов, представляющих собой смеси простых газов, зависит от их состава и давления. В точке росы должно выполняться соотношение:
l/P = Σ Xi / Pi
где Р — общее давление смеси; и Рi — соответственно мольная доля и парциальное давление i-го компонента газовой смеси.
Таблица 5.4
Точки росы для смесей пропана и н-бутана при давлении 3 кПа
| Пропан, % | |||||||||||
| н-бутан, % | |||||||||||
| Точка росы, °С | -42 | -32 | -26 | -2 | -17 | -13 | -10 | -8 | -5 | -2 |
Точку росы из-за сложности ее расчета обычно определяют по специальным номограммам. Номограммы имеют вид треугольника, на каждой стороне которого отложено содержание того или иного газа. В качестве примера на рис. 1 приведена номограмма для определения точки росы смеси пропана, изобутана и н-бутана при атмосферном давлении. Для смеси, состоящей из 25 % пропана, 60 % н-бутана и 15 % изобутана находят точку пересечения:

|
Рис.5.1 Номограмма для определения точки росы смеси пропана, изобутана и н-бутана при атмосферном давлении.
Из этой точки опускают перпендикуляр на шкалу температур и находят точку росы данной смеси (-7,6 °С).
Для определения точки росы можно использовать также специально разработанные графики зависимости точки росы различных смесей от давления и объемной доли компонентов, которые приводятся в справочной литературе.
При относительной влажности φ > 0,6 углеводороды с водой образуют кристаллогидраты, представляющие собой белые кристаллические тела, похожие на снег или лед. Они приводят к закупорке газопроводов, клапанов регуляторов давления, запорной арматуры. Метан с водой образует гидрат СН4•8Н2О, этан СН4•Н2О.
Гидраты появляются при температуре, значительно превышающей температуру образования льда. Максимальная температура, выше которой ни при каком повышении давления нельзя вызвать гидратообразование газов, называется критической температурой гидрообразования. Для метана она составляет 21,5 °С, этана — 14,5 °С, пропана — 5,5 °С.
Таблица 5.5
Условия образования гидратов
| Этан | Пропан | ||
| Температура, °С | Давление, МПа | Температура, °С | Давление, МПа |
| -9,5 | 0,32 | -11,9 | 0,1 |
| -6,7 | 0,36 | -9 | 0,12 |
| -3,9 | 0,41 | -6,3 | 0,13 |
| -1,1 | 0,46 | -5,6 | 0,14 |
| 0,6 | 0,51 | -3,3 | 0,16 |
| 1,7 | 0,58 | -1,0 | 0,17 |
| 10,8 | 1,7 | 1,7 | 0,24 |
| 2,7 | 2,3 | 0,27 | |
| 14,5 | 3,4 | 3,3 | 0,34 |
| — | — | 4,4 | 0,41 |
| — | — | 5,5 | 0,48 |
Чем тяжелее углеводородный газ, тем скорее он образует гидрат при наличии влаги.
Для предотвращения образования кристаллогидратов необходимо снижать влажность газов до φ < 0,6 при самой низкой расчетной температуре в газопроводе.
Образовавшиеся гидраты можно разложить подогревом газа, снижением его давления и вводом веществ, уменьшающих упругость водяных паров и понижающих точку росы газа. Одним из таких веществ является метанол (метиловый спирт), который надо вводить в количестве 0,26 кг на 1000 кг газа.
Тепловые свойства газов
Тепловые свойства газов определяются их теплоемкостью, теплопроводностью, теплосодержанием и теплотой сгорания.
Теплоемкостью газа называется его способность при нагревании поглощать теплоту. Теплоемкость газа С можно выразить отношением подведенного к газу количества теплоты ∆ Q к изменению температуры ∆ Т:
С=lim ∆ Q/ ∆ Т,
∆ Т→0
Теплоемкость газа представляет собой количество теплоты, необходимое для нагрева газа на 1 К. Единица измерения теплоемкости — Дж/К. Если теплоемкость отнести к количеству газа, то получим удельную теплоемкость.
Удельной теплоемкостью называется отношение подведенного к газу количества теплоты к произведению единицы количества газа и изменения его температуры.
В зависимости от того, что принимается за единицу количества газа, удельная теплоемкость называется массовой ст, Дж/(кг•К), молярной см, Дж/моль•К), объемной СV, Дж/(м3•К). Указанные теплоемкости связаны друг с другом следующими соотношениями:
Cm = CM /M, СV=CM/VM, CM = CmM = CVVM
где М — молярная масса, кг/моль; VM — молярный объем, м3/моль (для идеального газа при стандартных условиях VM ~ 22,4•10-3 м3/моль).
Удельная теплоемкость зависит от температуры. Различают удельные теплоемкости при постоянном объеме сv и при постоянном давлении ср.
Из термодинамики известно, что в случае нагревания газа при постоянном объеме теплота расходуется на увеличение только внутренней энергии. При нагревании газа при постоянном давлении теплота расходуется также и на работу расширения. Следовательно, ср > сv. Для идеального газа работа расширения равна универсальной газовой постоянной R и справедливо уравнение:
ср - сv = R
Отношение удельной теплоемкости при постоянном давлении к удельной теплоемкости при постоянном объеме называется показателем адиабаты
ср / сv = К.
Массовая и объемная теплоемкости с повышением температуры возрастают, а с увеличением молекулярной массы уменьшаются. Показатель адиабаты с повышением температуры и увеличением молекулярной массы уменьшается. Для идеального газа он примерно равен 1,667, для двухатомных газов — 1,41, для трехатомных — 1,34.
Различают истинную с и среднюю с' теплоемкости.
Истинной теплоемкостью называется количество теплоты, необходимое для изменения температуры единицы количества газа на 1 К при данных р и Т или V и Т.
Средняя теплоемкость — это количество теплоты, необходимое для изменения температуры единицы количества газа на 1 К в заданном интервале температур, т.е. от Т1 до Т. Среднюю объемную теплоемкость при постоянном давлении газа можно определить по средним теплоемкостям компонентов и их объемным долям:
с'р = 0,01 (с'Н2 *Н2+ с'СО *СО+ с'СН4 *СН4 +….+ с'n *N2)
где с'Н2 с'СО с'СН4 с'n — средние объемные теплоемкости указанных в индексах компонентов; Н2, СО, СН4... N2 — объемные доли компонентов, %. Значения средней объемной теплоемкости горючих газов и продуктов сгорания приведены в табл. 5.6.
Теплопроводность газа — это его способность проводить теплоту, т.е. осуществлять молекулярный перенос энергии. Молекулы участков газа, где температура выше, обладают большей энергией и передают ее соседним молекулам, обладающим меньшей энергией. Это приводит к выравниванию разности температур ∆Т, но передача теплоты не связана с переносом частиц.
Таблица 5.6
Средняя объемная теплоемкость при постоянном давлении кДж /(м3К) горючих газов в интервале температур от о до t
| Температура, °С | СО | Н2 | H2S | СН4 | С2Н4 | C2H6 | С3Н8 | С4Н10 | С5Н12 |
| 1,299 | 1,277 | 1,513 | 1,544 | 1,792 | 2,227 | 3,039 | 4,128 | 5,129 | |
| 1,302 | 1,292 | 1,543 | 1,653 | 2,031 | 2,525 | 3,450 | 4,517 | 5,837 | |
| 1,307 | 1,297 | 1,574 | 1,765 | 2,257 | 2,800 | 3,860 | 5,255 | 6,515 | |
| 1,317 | 1,300 | 1,608 | 1,890 | 2,466 | 3,077 | 4,271 | 5,774 | 7,135 | |
| 1,329 | 1,302 | 1,644 | 2,019 | 2,658 | 3,333 | 4,681 | 6,268 | 7,742 | |
| 1,343 | 1,305 | 1,682 | 2,144 | 2,839 | 3,571 | 5,095 | 6,691 | 8,257 | |
| 1,357 | 1,308 | 1,719 | 2,264 | 3,006 | 3,793 | 5,431 | 7,114 | 8,784 | |
| 1,372 | 1,312 | 1,756 | 2,381 | 3,157 | 4,003 | 5,724 | 7,486 | 9,232 |
ТЕМА 6. ПОДГОТОВКА И ПЕРЕРАБОТКА ГАЗОВ
Природный газ, поступающий из скважин, содержит механические примеси (песок, пыль), которые увеличивают абразивный износ газовых компрессоров, а углеводородный конденсат, пары воды и свободную влагу с растворенными в ней солями – они вызывают трудности (главным образом – коррозию, образование гидратов или льда, что является причиной возникновения пробок в нем) при транспортировки газа по трубопроводу.
Для удаления механических примесей используются сепараторы различных конструкций. Для предотвращения конденсации воды из газа при его охлаждении и образовании гидратов одним из наиболее важных звеньев в процессе подготовки газа транспорту является искусственная осушка, с помощью которой добиваются состояния газа, когда его точка росы ниже, чем температура транспортировки.
По своему классификационному признаку методы осушки газов подразделяются на три основные группы:
1. Физические. В основе лежит искусственное охлаждение газов, компримирование их, а также сочетание компримирования с охлаждением. Осуществляются следующими способами:
- вымораживанием влаги из газа с использованием низких температур атмосферы;
- охлаждением газа с дополнительным компримированием и без него;
- инжекцией химических веществ в газовый поток промысловых газосборных трубопроводов с последующим улавливанием продуктов гидратации на сепарационных и центральных установках;
- низкотемпературной сепарацией (т.е. охлаждением природного газа с последующим разделением газоконденсатной смеси в сепараторе на жидкую и газовую фазы).
2. Химические. Химическая реакция между водой и химическими веществами может быть столь полной, что образующиеся при этом продукты гидратации будут иметь чрезвычайно низкую упругость водяных паров. Имеются химические реагенты, обеспечивающие практически полную осушку газа. Однако эти реагенты очень трудно или вообще невозможно регенерировать, что делает их непригодными для использования в качестве промышленных осушителей. Они широко применяются при лабораторном определении влажности газов.
3. Физико-химические. Основаны на поглощении влаги различными поглотителями (сорбентами) и делятся на две основные группы: адсорбция (с применением твердых сорбентов) и абсорбция (с применением жидких сорбентов).
Методы газового анализа
Вопросы рационального использования газа, создания эффективных газоиспользующих установок и их автоматизации не могут быть решены без знания физических свойств газа и способов их контроля, позволяющих вести процесс сжигания газа в соответствии с режимными картами. Основной задачей анализа горючих газов является определение их компонентного состава, физических и теплофизических свойств и состава продуктов сгорания, так как свойства технических газов зависят от свойств отдельных компонентов, входящих в их состав. Контроль за сжиганием газа предусматривает определение состава продуктов сгорания; контроль безопасности производств, связанных с использованием газа, — определение наличия в атмосфере помещений токсичных и взрывоопасных веществ.
Газовый анализ подразделяется на общий и специальный. Для количественного определения природных и искусственных газов применяется общий анализ. Приборы, предназначенные для анализа газов, называются газоанализаторами.
В зависимости от того какие свойства газа используют при анализе, методы газового анализа условно разделяют на химические и физические.
Химические методы основаны на последовательном избирательном поглощении компонентов газовой смеси различными поглотителями или на сжигании горючих газов с последующим анализом продуктов горения. При поглощении благодаря химическому взаимодействию поглотителя с компонентами газовой смеси и растворению продуктов реакции объем газа уменьшается. Если в газовой смеси определяют несколько компонентов, то их последовательно удаляют из смеси и после каждого определения измеряют объем. Содержание компонентов определяют по разности объемов до и после поглощения.
Физические методы основаны на измерении какой-либо физической величины, находящейся в закономерной зависимости от состава газа. При этом используют такое физическое свойство газового компонента, которое значительно отличается от того же свойства остальных компонентов газовой смеси. Иногда анализ проводят путем сравнения с эталонным газом, для которого данное свойство известно. Свойства газов, используемые в газовом анализе, разнообразны. Наиболее часто применяют следующие методы анализа.
Денсиметрический. Метод основан на сравнении массы анализируемого газа с массой известного газа. Обычно определяют плотность по воздуху. Этим методом в многокомпонентной смеси можно определить только содержание одного компонента, имеющего плотность, отличающуюся от плотности всех остальных компонентов смеси. Из рассматриваемых нами газов этот метод наиболее применим к определению диоксида углерода (С02) в отходящих газах, который по плотности резко отличается от остальных компонентов смеси.
Термокондуктометрический. В основе метода — сравнение относительной теплопроводности газов. При анализе многокомпонентной смеси можно определить концентрацию только одного компонента, причем теплопроводность остальных компонентов должна быть примерно одинаковой. Метод применим для определения С02, Н2, S02 в продуктах горения, причем при определении одного из этих компонентов два других должны быть удалены из газовой смеси.
Термохимический. Этот метод применим при анализе горючих газов (СО, СН4, Н2). В нем используется тепловой эффект реакции горения этих компонентов. Сжигая СО, Н2 и СН4 при различных температурах, можно проводить их раздельный анализ.
Манометрический. В основе метода — измерение разрежения, получающегося в результате реакции анализируемого газа с соответствующим поглотителем.
Вискозиметрический. Метод основан на измерении вязкости газа.
Оптический. Метод базируется на различной способности газов поглощать инфракрасные или ультрафиолетовые лучи, сравнении коэффициентов преломления анализируемого газа и газа известной концентрации, спектральных измерениях и т.д.
Магнитный. Метод основан на свойстве газов втягиваться в магнитное поле. Особенно сильной магнитной восприимчивостью (парамагнитными свойствами) обладает кислород (02). Поэтому при анализе газовой смеси на 02 час<
|
|
|

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...

Историки об Елизавете Петровне: Елизавета попала между двумя встречными культурными течениями, воспитывалась среди новых европейских веяний и преданий...

Эмиссия газов от очистных сооружений канализации: В последние годы внимание мирового сообщества сосредоточено на экологических проблемах...

Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!