Горение топлива – сложный физикохим. пр-сс окисления горючих компонентов, сопровождаемый выделением теплоты и света. Большинство пр-ссов горения представляют собой соединение горючих компонентов с О2 воздуха. При хим. превращениях происходит разрыв молекулярных связей с образованием новых связей и молекул. Число атомов при хим. реакциях не меняется, а лишь происходит их перегруппировка. Энергия, необходимая для разрыва существующих связей и начала хим. реакции – энергия активации. Инициирование волны хим. реакции – это приведение в действие механизма, переводящего скрытую хим. энергию реакции компонентов в тепло. Отсюда можно выделить несколько видов зажигания топлива: 1). Эл. искра; 2). Лазерный пробой в газе; 3). Путем контакта горючей смеси с нагретым телом; 4). Путем смешивания с горячими продуктами сгорания; 5). Внесение в газовую смесь активных хим. центров. Действие этих инициаторов горения основано на 2-х способах: повышение температуры газа; развитие цепного разветвления в реакции горения. Механизм горения – при тепловом механизме распространения пламени, тепло, выделившееся при хим реакции передается в соседние участки непрореагировавшей газовой смеси, нагревай и инициируя дальнейшую реакцию. При распространении пламени реакция идет в каждый момент времени в относительно тонком слое – зона реакции. В непосредственной близости от зоны реакции происходит разогрев несгоревшей смеси, за зоной реакции остаются продукты реакции. Виды горения: 1) Гетерогенное – реакция между веществами, находящимися в разных фазовых состояниях (горение тв. и жидк. топлива)2) Гомогенное – реакция между веществами, находящимися в одном фазовом состоянии с окислителем (горение газа) При сжигании топлива важно знать время, за которое произойдет полное сгорание, т.к. от него зависит производительность котлоагрегата (чем быстрее, тем выше производительность) Полное время сгорания топлива состоит из 2-х составляющих:а) диффузионная – время, затраченное на подвод окислителя к горючемуб) кинетическая – время на саму реакцию горения. Для снижения диффузионной составляющей тв топлива необходимо уменьшить гранулы; для жидкого – разбиение основной струи на отдельные струи, распыление на капли; для газа – закрутка потока, организация пульсации или детонации. Для снижения кинетической составляющей – правильная организация процесса сжигания, верное соотношение топливо-окислитель, повышение температуры сжигания топлива. Механизмы горения топлива: 1) Газовое топливо. Горение газового топлива – окисление исходной газо-воздушной смеси и разложение на компоненты. Основная характеристика горения газа – скорость нормального (по нормали к фронту) распространения пламени. Массовая скорость горения – масса смеси, соприкасающаяся в единицу времени на единицу поверхности фронта пламени. При горении газа в трубе свежая газовая смесь, как более тяжолое в-во по сравнению с продуктами сгорания растекается по нижней части трубы, а более легкие продукты сгорания стремятся вверх, следовательно фронт пламени искривлен. Различают 2 вида форм движения пламени: ламинарное и турбулентное.При турбулентной форме движения фронт пламени может разрываться на отдельные зоны, на отдельные части горящего газа и продукты сгорания, создавая отдельные очаги пламени.2) Жидкое топливо. Горение жидкого топлива – горение каждой капли. При сжигание жидкого топлива основной поток горючего за счет форсунки разбивается на ряд струй, которые закручиваются, но не перемешиваются. Далее эти струи распыляются на отдельные капли, попадают в топочное пространство с высокой температурой, испаряются, образуя летучее в-во, которое сгорает. При этом последней догорает коксовая частица, минеральные примеси оседают на стенках экранов хвостовой поверхности нагрева.3) Твердое топливо. Тверд. топливо попадает в топочную камеру, в которой большая температура, при этом атомы О2 адсорбируются на поверхности топлива и при термическом воздействии реагируют с углеродом топлива, идет реакция образования СО и СО2. При высоких температурах может идти реакция восстановления. При термическом разложении топлива из него выделяются летучие в-ва, образуется газо-воздушная смесь, которая сгорает, отдавая тепло топочной камере, а также непрореагировавшему топливу
19. Расчёт процессов горения топлива. Определение теоретического и действительного объемов воздуха и продуктов сгорания. Коэффициент В ходе расчетов определяются следующие показатели:1.Теплота сгорания QHP для газообразных топлив в кДж/м3, для жидких и твердых топлив кДж/кг и плотность газа ρ.2.Теоретически необходимое количество воздуха, необходимое для сжатия 1м3 газа либо 1 кг топлива:
Для газов: V0 = 0,0476*(0,5 СО2 + 0,5 H2 + 1,5 H2S + Σ (m+n/4)*CmHn-O2), м3/м3 Для жидких и твердых топлив: V0 = 0,0889*(Ср + 0,375 Sрор+к) + 0,265 Hр – 0,0333 Ор м3/кг 3.Действительное количество воздуха, необходимое для сжатия 1м3 газа либо 1 кг топлива, м3/м3:Vд = V0×αт, где αт – коэффициент избытка воздуха, показывающий во сколько раз необходимо увеличить подачу воздуха в топочное пространство, αт = 1,1 (всегда больше 1), αт >1 так как при сжатии топлива не возможно обеспечить 100% сгорание, ввиду неполного сгорания топлива при слабом смешении топлива с окислителем и не идеальной конструкции котлоагрегата.
Коэффициент избытка воздуха зависит от:- вида топлива, - способа его сжигания, - технологии организации топливных процессов.Для газообразного топлива αт = 1,05 – 1,3; Для жидкого топлива (мазут) αт = 1,05 – 1,1; Для твердого топлива: при сжигании в слоевой топке αт = 1,3 – 1,7, в камерной топке αт = 1,2 – 1,25.
1.Теоретический объем продуктов горения V0г, м3/м3, м3/кг: V0г = VRO2 + V0Н2О + V0N2
2Действительный объем продуктов горения будет определяться следующим выражением: VГ = VRO2 + V0Н2О + V0N2 + (αт – 1)∙V0,
Для расчёта действительного объёма продуктов горения используют следующие формулы: объем водяных паров, для газов в м3/м3, для жидких и твердых топлив м3/кг:
V0Н2О = 0,01*(H2S + H2 + Σ (n/2)*CmHn) +0,0161*V0, м3/м3
V0Н2О = 0,111*Hр + 0,124*Wр + 0,016*V0, м3/кг объем трехатомных газов: для газообразных топлив в м3/м3, для жидких и твердых топлив м3/кг: VRO2 = 0,01*(СО2 + СО + H2S + Σ m*CmHn), м3/м3
VRO2 = 1,866*(Ср + 0,375 Sр)/100, м3/кг
объем паров азота: для газообразных топлив в м3/м3, для жидких и твердых топлив м3/кг:
V0N2 = 0,79*V0 + 0,01*N2, м3/м3 V0N2 = 0,79*V0 + 0,8*Nр, м3/кг где CmHn – углеводороды, входящие в состав газа, %. Определение КПД котлоагрегата, %: ηка = 100 – (q2 + q3 + q4 + q5 + q6), где: q2 – потери теплоты с уходящими газами %, q2 = [(Hух – αух* H0хв)*(100 - q4)]/ QHP; Н – энтальпии уходящих из топки газов и воздуха подаваемого в топку; q3 – потери теплоты с хим. недожогом, для газа 0,5%, для мазута 0,82%; q4 – потери теплоты с механическим недожогом q5 – потери теплоты через ограждающие конструкции КА, принимаются 1,7; q6 - потери теплоты со шлаком, для газа и мазута 0 %. Таким образом, видно, что коэффициент избытка воздуха влияет на КПД котлоагрегатаза счет q2 = [(Hух – αух* H0хв)*(100 - q4)]/ QHP. При чем больше αух тем меньше q2 и тем больше КПД котлоагрегата.
20. Топочные устройства котельных агрегатов. Виды топок, особенности работы и конструкции, применяемое топливо. Топки: - слоевые;-камерные; - циклонные; - топки с кипящим слоем;- топки со специализированным назначением(сжигание бытю мусора, отходов произ-ва) По виду сжигаемого топлива: 1 тв. Топливо, 2 жид, 3 газообразное, 4комбинированные. По разположению относительно поверхности нагрева: 1внутренние 2нижние(внешние) 3выносные
 1.Ручные слоевые топки: схема топки.
1.Ручные слоевые топки: схема топки.
1-передняя (бортовая) стена котла;2-задняя стена котла; 3-боковая стена котла; 4-колосниковая решетка; 5-окно для подачи топлива; 6-окно для подачи воздуха; 7-шлаковая шапка; 8-первый ряд пучковых труб.
2Полумеханические слоевые топки -в них частично механизированы некоторые процессы. в котельных установках малой мощности получили распространение топки с подачей топлива на неподвижную колосниковую решетку с помощью ротационных забрасывателей. 3.Механические слоевые топки: бывают двух типов: 1)с цепной колосниковой решеткой 2) с шурующей планкой.:
Топки с кипящим слоем кипящий слой характеризуется скоростью воздуха, подаваемого под слой топлива, превышающей предел устойчивости плотного слоя, но далеко не достигающей скорости витания средних частиц.Все частицы в слое перемещаются, двигаясь колебательно вверх и вниз «+»: - позволяют сжигать высокозольное топливо,- коэф. Теплопередачи в 2-3 раза выше, чем в слоевых,- меньшие размеры,-меньше вредных выбрасов: - требуют высокого давления воздуха,- возможен унос части топлива,- быстрый износ металлич. Поверностей,- трудность организации и регулирования процессов. Камерные топки: представляют собой устройства, в кот. Топливо горит в объёме камеры в виде факела при отсутствии какого либо слоя топлива- пылеугольные,(для сжигания пылевидной составляющей торфа, угля.),газомазутные
 21. Горелочные устройства для твердого, жидкого и газообразного топлива. Виды горелок, особенности работы и конструкции. 1. Газовые горелки. Для сжигания газообразного топлива используются горелки различных типов. По давлению газа перед горелками они делятся на два основных типа - горелки низкого давления и горелки среднего давления Либо используется газ второй категории высокого давления В зависимости от конструкции горелки, используемые в котельных, бывают: 1) диффузионные н/давления и с/давления, 2) инжекционные н/давления и с/давления, 3) вихревые н/давления и с/давления.1) Диффузионные горелки – это горелки без предварительного смешения воздуха с топливом. Через горелку в топку подается газ, а воздух поступает по отдельным каналам. Примером дифф-й горелки является подовая щелевая горелка. Дост-во: 1.Простота. 2.Эти горелки дают меньший выход азота. Инжек-е горелки Устанавливаются на котлах малой производительности. Эти горелки используют энергию газовой струи для подсоса или инжектирования воздуха необходимого для горения горелки. Эти горелки при повышенной производительности имеют большие размеры. Дост-во: не требуют вентиляторов.
21. Горелочные устройства для твердого, жидкого и газообразного топлива. Виды горелок, особенности работы и конструкции. 1. Газовые горелки. Для сжигания газообразного топлива используются горелки различных типов. По давлению газа перед горелками они делятся на два основных типа - горелки низкого давления и горелки среднего давления Либо используется газ второй категории высокого давления В зависимости от конструкции горелки, используемые в котельных, бывают: 1) диффузионные н/давления и с/давления, 2) инжекционные н/давления и с/давления, 3) вихревые н/давления и с/давления.1) Диффузионные горелки – это горелки без предварительного смешения воздуха с топливом. Через горелку в топку подается газ, а воздух поступает по отдельным каналам. Примером дифф-й горелки является подовая щелевая горелка. Дост-во: 1.Простота. 2.Эти горелки дают меньший выход азота. Инжек-е горелки Устанавливаются на котлах малой производительности. Эти горелки используют энергию газовой струи для подсоса или инжектирования воздуха необходимого для горения горелки. Эти горелки при повышенной производительности имеют большие размеры. Дост-во: не требуют вентиляторов.
1-Газовое сопло, 2-Конфузор, 3-Горловина,
4-Диффузор, 5-Газовая горловина, 6-Отверстие для выдачи газо-мазутной смеси.
| 1-молотковая мельница, 2-шахта
3-эжекционное сопло, 4-амбразура
| - дробленое топливо, || - первичный воздух, - вторичный воздух
| |
3)
Вихревые горелки (смесительные с принудительной подачей воздуха) работают с вентилятором, который нагнетает воздух в горелку.
Дост-ва: 1.Число струек может быть больше. 2.Выше производительность с периферийной подачей газа.
2. Устройства для сжигания угольной пыли. Горелочные устройства для сжигания угольной пыли делятся на: 1)Амбразуры – для сжигания топлива, размолотого в молотковых мельницах; 2)Вихревые горелки; 3)Щелевые угловые (прямоточные) горелки. 1)
Амбразуры – используются в шахтно-мельничных топках

2) Вихревые горелки. Наибольшее распространение получили два типа: 1. ОРГРЭС – идет закрутка (завихрения) вторичного воздуха. 2. ТКЗ – происходит закручивание, как вторичного так и первичного воздуха. С помощью маховиков рассекатель (3) перемещается вдоль оси горелки, благодаря чему изменяется угол раскрытия факела, что приводит к возможности сжигания различных топлив. В вихревых горелка ТКЗ первичный воздух закручивает сразу, а затем вторичный.
I II 1 2
 3
3
1-Канал первичного воздуха с угольной пылью, 2-Канал вторичного воздуха, закручивающийся в улитке, 3-Рассекатель аэросмеси, 4-Маховик, |. Аэросмесь, ||. Вторичный воздух.3) Щелевые угловые горелки. Такие горелки обладают большой дальнобойностью, поэтому их размещают под углом к топочной камере, т.о. чтобы их оси оказались касательными к некоторой воображаемой окружности. При этом происходит завихрения внутри самой топки. Твердые частицы вращаются до тех пор, пока полностью не выгорают. Такие горелки подходят для низко реакционных топлив, т.к. увеличено время горения топлива 3. Мазутные форсунки Мазутные форсунки – устройства для сжигания мазута.По способу распыления: 1)механические, 2)с распыляющей средой, 3)комбинированные 1) Механические форсунки предназначены для крупных котлов. Достоинства: экономичные, малошумные, с низким пределом регулирования. Недостатки: очень требовательны к чистоте мазута и твердым примесям.2) С распыляющей средой. 3) Комбинированные форсунки.. Достоинства: менее шумные, повышены пределы регулирования нагрузки, уменьшен удельный расход пара на распыление мазута примерно в 10 раз по сравнению с паровыми форсунками.
22.Экономайзеры котлов, их основные виды и схемы. Методика конструкторского расчета (постановка задачи, основные уравнения тепло-гидравлического расчета).
 Экономайзеры – устройства, предназначенные для подогрева воды или воздуха в котельной установке с помощью тепла уходящих продуктов сгорания топлива, которые для лучшего теплообмена двигаются сверху вниз, а вода – снизу вверх. Экономайзер повышает КПД котельной установки. Область применения экономайзеров – нагрев питательной воды паровых котлов и воды систем теплоснабжения. Экономайзеры котла выполняют либо из гладких, либо из ребристых чугунных труб; на более высокие температуру и давление – из стальных гладких труб.
Экономайзеры – устройства, предназначенные для подогрева воды или воздуха в котельной установке с помощью тепла уходящих продуктов сгорания топлива, которые для лучшего теплообмена двигаются сверху вниз, а вода – снизу вверх. Экономайзер повышает КПД котельной установки. Область применения экономайзеров – нагрев питательной воды паровых котлов и воды систем теплоснабжения. Экономайзеры котла выполняют либо из гладких, либо из ребристых чугунных труб; на более высокие температуру и давление – из стальных гладких труб.
Различают поверхностные и контактные экономайзеры. Поверхностные экономайзеры в свою очередь бывают – питательные (нагрев воды для питания котлов) и теплофикационные (нагрев воды для систем отопления).
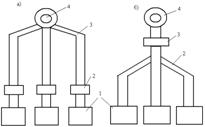
По материалу конструкции различают чугунные и стальные экономайзеры. К основным характеристикам оборудования также относятся: схема присоединения и степень нагрева воды – экономайзеры «кипящего» и «некипящего» типа; размещение относительно котлов – групповое (б) и индивидуальное (а).
1-котел; 2-экономайзер; 3-газоход; 4-дымовая труба.
Устанавливаются контактные экономайзеры непосредственно за котлами или после поверхностных экономайзеров. Чугунные экономайзеры собираются из чугунных ребристых труб длиной 2-3 метра, соединенных между собой чугунными коленами. Несколько горизонтальных рядов труб (до восьми) образуют группу, группы компонуют в колонны, разделенные металлическими перегородками. Группы собирают в каркасе с глухими стенками с теплоизоляционной обшивкой. Торцы экономайзеров закрывают съемными металлическими щитами. Экономайзеры оборудуются стационарными обдувочными устройствами, встроенными в блоки. Количество горизонтальных рядов, которые обдуваются одним устройством, не должно превышать четырех.Преимуществом чугунных экономайзеров является их повышенное сопротивление к химическому и механическому разрушению. Использование чугуна значительно увеличивает срок службы оборудования по сравнению со стальными экономайзерами. Чугунные экономайзеры бывают только «некипящего» типа. Стальные экономайзеры представляют собой несколько секций змеевиков, изготовленных из труб определенной длины и радиуса гиба. Отдельные пакеты змеевиков не должны иметь более 25 рядов и высоту более 1,5 м. Между пакетами должны быть предусмотрены разрывы для размещения обдувочных устройств.Стальные экономайзеры бывают «некипящего» и «кипящего» типа. Водяные экономайзеры рассчитывают следующим образом. Сначала по известным энтальпиям газов на входе в экономайзер ( (кДж/кг)) и на выходе из него (
(кДж/кг)) и на выходе из него (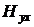 ) определяют тепловосприятие экономайзера по уравнению теплового баланса
) определяют тепловосприятие экономайзера по уравнению теплового баланса  , кВт, где BР - расчетный расход топлива, кг/с; φ - коэффициент сохранения теплоты; ΔHB -энтальпия, кДж/кг. Температуру воды на выходе из экономайзера
, кВт, где BР - расчетный расход топлива, кг/с; φ - коэффициент сохранения теплоты; ΔHB -энтальпия, кДж/кг. Температуру воды на выходе из экономайзера  , кВт, где
, кВт, где 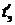 – температура воды на входе в экономайзер; св – теплоемкость воды, кДж/кг×оС; Dвэ - количество воды, проходящей через экономайзер, кг/с. Dвэ=Dнп+Dпр, где Dнп - расход насыщенного пара кг/с; Dпр - расход продувочной воды, кг/с. Для чугунного экономайзера
– температура воды на входе в экономайзер; св – теплоемкость воды, кДж/кг×оС; Dвэ - количество воды, проходящей через экономайзер, кг/с. Dвэ=Dнп+Dпр, где Dнп - расход насыщенного пара кг/с; Dпр - расход продувочной воды, кг/с. Для чугунного экономайзера  должна быть не менее чем на двадцать градусов ниже температуры насыщения для избежания кавитации.Среднюю разность температур с достаточной степенью точности можно определить как среднеарифметическую величину
должна быть не менее чем на двадцать градусов ниже температуры насыщения для избежания кавитации.Среднюю разность температур с достаточной степенью точности можно определить как среднеарифметическую величину 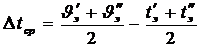 , оС, где
, оС, где 
 - температура газов до и после экономайзера Среднюю скорость газов в экономайзере подсчитывают по выражению
- температура газов до и после экономайзера Среднюю скорость газов в экономайзере подсчитывают по выражению
 , м/с. При этом живое сечение экономайзера Fэ=fэ×m выбирают таким образом (набирая различное количество труб в горизонтальном ряду), чтобы Wср была в пределах 6…9 м/с. Здесь m – число труб в горизонтальном ряду.kэ - коэффициент теплопередачи, Вт/м2×оС; Vг- объем газов.
, м/с. При этом живое сечение экономайзера Fэ=fэ×m выбирают таким образом (набирая различное количество труб в горизонтальном ряду), чтобы Wср была в пределах 6…9 м/с. Здесь m – число труб в горизонтальном ряду.kэ - коэффициент теплопередачи, Вт/м2×оС; Vг- объем газов.
После этого определяют расчетную поверхность нагрева экономайзера  , м2. Число горизонтальных рядов определяется как n=Hвэ/hэ×m, где hэ - поверхность нагрева одной трубы, м2.
, м2. Число горизонтальных рядов определяется как n=Hвэ/hэ×m, где hэ - поверхность нагрева одной трубы, м2.
23,24. Принципиальная тепловая схема паровой производственно-отопительной котельной. Основное и вспомогательное оборудованиеПроизводственно-отопительные котельные установкивырабатывают пар не только для производственных нужд, но и для целей отопления, вентиляции и горячего водоснабжения.
 Принципиальная схема котельной со стальными паровыми котлами, отпускающей пар на технологические нужды и горячую воду на теплоснабжение:
Принципиальная схема котельной со стальными паровыми котлами, отпускающей пар на технологические нужды и горячую воду на теплоснабжение:
1-котлы; 2-РОУ; 3-регулирующий клапан; 4-пароводяной теплообменник; 5-конденсатоотводчик; 6-сетевой насос; 7-фильтр; 8-регулятор подпитки; 9-деаэратор; 10-питательный насос; 11-аппараты химводоочистки; 12-подпиточный насос.
Выраб-й в котлах 1 пар по паропров-м напрвл-ся к технологич-м потреб-м и в пароводяной теплообм-к 4 для подогрева воды, циркул-ей в системе теплоснабжения. Конденсат от технологич-х потреб-й и после пароводяного теплообм-ка поступает в деаэратор 9, для работы которого использ-ся редуцированный пар от котлов. Для восполнения потерь конденсата в деаэратор с помощью подпиточного насоса 12 подается также подпиточная вода после ХВО 11. Из деаэратора вода подается питательным насосом 10 в котлы. Циркуляция воды в системе теплоснабжения осущ-ся с помощью сетевых насосов 6. Отпуск тепла на теплоснабжение регул-ся путем измен-я расхода пара с помощью регуляторов 3 в соотв-ии с требуемым темпер-м графиком. Подпитка воды в тепловую сеть производится подпиточным насосом 12 после ХВО 11 на всасывание сетевого насоса. Производится выбор котлоагрегата, турбогенератора подогревателя, и подпиточного насоса. Котлоагрегат подбирается по расчетному расходу пара
 h′′- энтальпия перегретого пара, h′ - насыщенного пара Турбогенератор подбирается по расходу пара
h′′- энтальпия перегретого пара, h′ - насыщенного пара Турбогенератор подбирается по расходу пара
 , Кзагр=0,6 (т/ч) Подогреватель сетевой воды и охладитель конденсата выбираются согласно расчету требуемые данные: t0, τ1, Gсет, Qгвmax, Насосы подбираются по требуемому напору и расходу воды
, Кзагр=0,6 (т/ч) Подогреватель сетевой воды и охладитель конденсата выбираются согласно расчету требуемые данные: t0, τ1, Gсет, Qгвmax, Насосы подбираются по требуемому напору и расходу воды
 (к Вт)
(к Вт)
25. Термические (p,v,т) и калорические (u,i,s) параметры состояния тела. Физический смысл, единицы измерения. Уравнение состояния К термическим параметрам состояния относятся давление (p), объем (v), температура(T). К калорическим: энтропия (s), внутренняя энергия (u) и энтальпия(i). Давление — сила, действ-щая на ед.площади. Р=F/S. Единицей давления в СИ является паскаль — давление, вызываемое силой в 1 Н, равномерно распределенной по поверхности площадью 1 м2 (1Па=1 Н/м2). Различают атмосферное (барометрическое); абсолютное давление; манометрическое (избыточное); разрежение (вакуум). Давление атмосферного воздуха измеряется барометрами, избыточное давление — манометрами, а давление разрежения — вакуумметрами. Температура тела есть мера его нагретости. Температура определяет направление передачи теплоты. Если два тела А и В имеют соотв-но температуру Т1 и Т2 и Т1>Т2, то теплота переходит от тела А к телу В. При этом темп-ра тела А умен-ся, а В – увел-ся. За основную единицу измерения температуры принимают градус. В настоящее время прим-ся различные темпер-ные шкалы: Цельсия, Фаренгейта, Реомюра, Ранкина. Наиболее универсальной шкалой тем-тур является абсолютная термодинамическая шкала тем-тур - шкала Кельвина. За нормальные физические условия принимают давление, равное 101,325 кПа (760 мм рт. ст.), и температуру, равную О °С. Удельный объем вещества — это объем, занимаемый единицей массы данного вещества Vуд=V/m. Плотность вещества r — величина, обратная удельному объему и определяющая -во вещ-ва, заключенное в единице объема. Измер-ся в кг/м3. Внутренняя энергия. (Дж/кг) Любая термодинамическая система в каждом состоянии обладает запасом полной энергии, кот-я состоит из внутренней энергии, зависящей от внутр-го состояния тела, и внешней энергии, связанной с движением тела как целого и положением его в каком-либо внешнем поле сил. Если тело не движется, а влиянием внеш-го поля сил можно пренебречь, то полная энергия будет представлять собой только внутреннюю энергию. Удел. внутр. энергия рабочего тела зависит от его температуры и удел. объема, являясь однозначной функцией этих параметров состояния. ΔU = CvΔT. Изменение уд.вн.эн. не зависит от характера процесса, а определяется лишь начальным и конечным состояниями рабочего тела. Δu = u2 − u1. u=q-pV Энтальпия (Дж/кг), также тепловая функция и теплосодержание — термодинамический потенциал, характеризующий состояние системы в термодинамическом равновесии при выборе в качестве независимых переменных давления, энтропии и числа частиц. Энтальпия равна сумме внутренней энергии газа и потенциальной энергии поршня с грузом i= u + pV. Энтальпия аналогично вн.эн. является функцией состояния. Следовательно, в процессе изменения состояния Δi = i2 − i1. Если система каким-либо путём возвращается в исходное состояние (замкнутый цикл), то изменение любого её параметра равно нулю, а отсюда ΔU = 0 и Δi = 0. di=TdS+Vdp Энтропия Дж/(кг • К) - параметр состояния, дифференциал которого равен отношению бесконечно малого количества теплоты в элементарном обратимом процессе к абсолютной температуре, постоянной на бесконечно малом участке процесса. 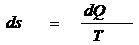 Ур-е состояния идеального газа или ур-ем Клапейрона - Менделеева pv = RTm/µ. Здесь р - давление газа, v - объем, занимаемый m килограммами (граммами) газа, µ - килограмм-моль (грамм-моль), R - универсальная газовая постоянная, T –температура. Килограмм-моль (грамм-моль) - число килограммов (граммов) вещества, численно равное молекулярному весу. Из уравнения (1) получаются законы Гей-Люссака, Шарля и Бойля-Мариотта. При постоянных p и m (так как R =const, а µ постоянно для данного вещества) v1=v0T1/T2,где v0 и T0 - объем и температура газа при 0°C. Отсюда следует закон Гей-Люссака (уравнение изобарического процесса): v = v0(1+t/273). При постоянных v и m получается закон Шарля (уравнение изохорического процесса): p = p0(1+t/273). При постоянных T и m (изотермический процесс) получается закон Бойля-Мариотта: p1v1 = p2v2. Величина 1/273 (1/град) называется коэффициентом объемного расширения или термическим коэффициентом давления идеального газа. Для реальных газов при давлениях, близких к атмосферному или больших, соответствующие коэффициенты несколько отличаются от этой величины.
Ур-е состояния идеального газа или ур-ем Клапейрона - Менделеева pv = RTm/µ. Здесь р - давление газа, v - объем, занимаемый m килограммами (граммами) газа, µ - килограмм-моль (грамм-моль), R - универсальная газовая постоянная, T –температура. Килограмм-моль (грамм-моль) - число килограммов (граммов) вещества, численно равное молекулярному весу. Из уравнения (1) получаются законы Гей-Люссака, Шарля и Бойля-Мариотта. При постоянных p и m (так как R =const, а µ постоянно для данного вещества) v1=v0T1/T2,где v0 и T0 - объем и температура газа при 0°C. Отсюда следует закон Гей-Люссака (уравнение изобарического процесса): v = v0(1+t/273). При постоянных v и m получается закон Шарля (уравнение изохорического процесса): p = p0(1+t/273). При постоянных T и m (изотермический процесс) получается закон Бойля-Мариотта: p1v1 = p2v2. Величина 1/273 (1/град) называется коэффициентом объемного расширения или термическим коэффициентом давления идеального газа. Для реальных газов при давлениях, близких к атмосферному или больших, соответствующие коэффициенты несколько отличаются от этой величины.

26. Теплота, работа, мощность. Определение, единицы измерения. 1-й закон термодинамики (через внутреннюю энергию и энтальпию). 2-й закон термодинамики. Энтропия. Работа-параметр, характеризующий процесс передачи энергии(упорядоченный), Дж.Количество теплоты- параметр, характеризующий процесс передачи энергии (хаотично). Энергия- характеристика системы, форма материи, характеристика состояния вещества.Мощность- энергия, затраченная в единицу времени
1-й закон является законом сохранения и взаимного превращения других видов энергии. Он показывает эквивалентность количества теплоты и работы.1-й закон запрещает построение вечного двигателя 1-го рода, такой машины, которая повторяя процессы производила бы работу в большом количестве чем потребляемая энергия. Через внутреннюю энергию  pdv- работа расширения
pdv- работа расширения  vdp –техническая работа d(pv)= p2; v2-p1 v1 =
vdp –техническая работа d(pv)= p2; v2-p1 v1 = 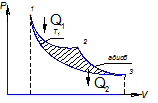 pdv+vdp – работа проталкивания l′=l-l0 Энтальпия- параметр, характеризующий состояние системы.
pdv+vdp – работа проталкивания l′=l-l0 Энтальпия- параметр, характеризующий состояние системы.
Й закон термодинамики

2-й закон термодинамики показывает направленность самопроизвольно протекающих в природе процессов. Система стремится к состоянию равновесия. dS≥0 Знак = для обратимых процессов знак > для необратимых реальных процессов
2-й закон констатирует неэквивалентность количества теплоты и работы в смысле их взаимопревращений. Работу можно полностью превратить в теплоту, а теплоту нельзя превратить в работу. Поэтому в процесс необратимого энергообмена качество энергии ухудшается, т.е снижается ее работоспособность. 2-й закон запрещает невозможность вечного двигателя 2-го рода, только двигателя превращающего полностью теплоту в работу. цикл карно  Энтопия – физическая величина изменение которой происходит при обмене энергии в форме теплоты в равновесном процессе
Энтопия – физическая величина изменение которой происходит при обмене энергии в форме теплоты в равновесном процессе  (Дж/К)
(Дж/К)
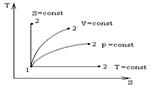
27. Изобарный и адиабатный процессы. Уравнение процессов для идеального газа. Политропный процесс – PV n – const Изохорный процесс – V=const, n=∞. Работа расширения в изохорном процессе l=0 dq=du. Вся теплота идет на увеличение внутренней энергии газа. Количество теплоты сообщаемое системе при нагреве от состояния 1 до состояния 2 равно q1,2=cv (T2-T1) Изобарный процесс – P=const n=0. Работа процесса lр=p(V2-V1) = R (T2-T1)? Теплота изобарного процесса qp=cp(T2-T1) Изотермический процесс n=1 T=const, pv=RT=const. Работа расширения системы l1,2=pdv=(RT/v)dv=RT*ln v2/v1, теплота подводимая к системе dq=Tds, q1,2=T(S2-S1) Адиабатный процесс – n=k, pvk=const – это процесс в котором от системы не отводится и не подводится теплота dq=0, ds=dq/T=0. Удельная работа в равновесном адиабатном процессе производится только за счет изменения внутренней энергии газа и при c=const lp= Δu=cp(T1-T2)

Х-степень сухости показывает массовую долюпара в смеси при t=00C, U0=0
q`=U`-U`o=òpdV q`=U` i`=U`pV i`=U`=q`
S`=C`lnTн/273 r =r+y
r =теплота фазового превращения r=внутренняя теплота парообразованияy=внешняя теплота парообразования
 ix =i’+xr U’’=U’+r, i”=i’+r,
ix =i’+xr U’’=U’+r, i”=i’+r,

Калорический
параметр «энтальпия» воды и водяного пара. Различные состояния воды и пара, их название, иллюстрация состояния в p-v, Энтальпия – параметр, характеризующий состояние системы, равный сумме внутренней энергии системы и произведения давления системы на объем системы. H = U + pV Энтальпия измеряется в тех же единицах, что и теплота, работа и внутренняя энергия, Дж, ккал. В термодинамике внутренняя энергия, энтальпия, теплоемкость называются калорическими свойствами вещества, а удельный объем, давление, температура – термическими свойствами. Образование пара из одноименной жидкости происходит посредством ее испарения или кипения. Испарение жидкости может происходить лишь с открытой поверхности, кипение жидкости может происходить и при отсутствии открытой поверхности. Пар какого-либо вещества, находящийся в динамическом равновесии с одноименной жидкостью, называется насыщенным паром. Пар какого-либо вещества, не содержащий в себе одноименной жидкости и имеющий температуру кипения при данном давлении, называется сухим насыщенным паром. Состояние сухого насыщенного пара является переходным и неустойчивым в тепловом отношении. Пар какого-либо вещества, температура которого превышает температуру кипения при данном давлении, называется перегретым паром. Насыщенный пар какого-либо вещества, содержащий в себе одноименную жидкость в виде взвешенных в нем мелкодисперсных частиц, называется влажным паром. Поскольку до полного превращения в жидкость температура влажного пара остается неизменной и не может быть использована для характеристики его состояния, вместо нее применяется другой параметр, специфичный для этого случая — степень сухости х. Процесс парообразования при постоянном давлении в рv-диаграмме изображается горизонтальной линией а-b-c-d (рис.1), у которой участок а-b соответствует подогреву жидкости от 0°С до температуры кипения, участок b-с — превращению кипящей воды в сухой насыщенный пар и участок c-d — перегреву пара до заданной температуры. Таким образом, на графике величины vо и v' и v" соответствуют удельным объемам жидкости при 0°С, кипящей жидкости и сухого насыщенного пара.
 Рис.1
Рис.1 
Рис.2
Рис3
 При подогреве жидкости удельный объем ее несколько увеличивается вследствие температурного расширения, процесс же парообразования характеризуется резким увеличением удельного объема. Построив в рv-диаграмме аналогичные графики для нескольких различных давлений и соединив одноименные точки плавными линиями (рис. 2), можно заметить, что в связи с очень малой сжимаемостью жидкости линия a-a1-а..., выражающая зависимость v0=f(p), практически вертикальна; в связи с тем, что при увеличении давления возрастает температура кипения, от которой зависит v', линия b-b1-b2..., выражающая зависимость v' = f(p), идет круто вверх с наклоном в правую сторону; наконец, линия c-с1-с2..., выражающая зависимость v" = f(p), имеет гиперболический характер. T-S диаграмма(рис.3): Все точки, соответствующие состоянию кипящей воды, в такой диаграмме размещаются на линии АК, т. е. на изобаре pкр, которая, следовательно, является и нижней пограничной кривой. Более того, на этой же изобаре лежат и все без исключения точки, соответствующие состоянию некипящей воды при разных давлениях, т.е. линия отражает состояние насыщенной жидкости. Степень сухости х = 0. i-s-диаграмма: Построение этой диаграммы, общий вид которой приведен на рис.4, осуществляется таким образом. По табличным значениям i', s', i" и s" строятся нижняя и верхняя пограничные кривые OK и KL, затем точки на этих кривых соответствующие одинаковым давлениям, соединяются прямыми линиями, образующими в области влажного пара пучок начинающихся в начале координат и расходящихся кверху изобар. Одновременно эти линии являются и изотермами.
При подогреве жидкости удельный объем ее несколько увеличивается вследствие температурного расширения, процесс же парообразования характеризуется резким увеличением удельного объема. Построив в рv-диаграмме аналогичные графики для нескольких различных давлений и соединив одноименные точки плавными линиями (рис. 2), можно заметить, что в связи с очень малой сжимаемостью жидкости линия a-a1-а..., выражающая зависимость v0=f(p), практически вертикальна; в связи с тем, что при увеличении давления возрастает температура кипения, от которой зависит v', линия b-b1-b2..., выражающая зависимость v' = f(p), идет круто вверх с наклоном в правую сторону; наконец, линия c-с1-с2..., выражающая зависимость v" = f(p), имеет гиперболический характер. T-S диаграмма(рис.3): Все точки, соответствующие состоянию кипящей воды, в такой диаграмме размещаются на линии АК, т. е. на изобаре pкр, которая, следовательно, является и нижней пограничной кривой. Более того, на этой же изобаре лежат и все без исключения точки, соответствующие состоянию некипящей воды при разных давлениях, т.е. линия отражает состояние насыщенной жидкости. Степень сухости х = 0. i-s-диаграмма: Построение этой диаграммы, общий вид которой приведен на рис.4, осуществляется таким образом. По табличным значениям i', s', i" и s" строятся нижняя и верхняя пограничные кривые OK и KL, затем точки на этих кривых соответствующие одинаковым давлениям, соединяются прямыми линиями, образующими в области влажного пара пучок начинающихся в начале координат и расходящихся кверху изобар. Одновременно эти линии являются и изотермами.
Рис.4
 В области влажного пара наносится система линий постоянной степени сухости (x=const). Построение их основано на том, что каждая из этих линий делит все изобары влажного пара на пропорциональные отрезки. Обычно на i-s диаграмму наносится и система изохор u=const, которые по своему характеру близки к изобарам, но идут несколько круче и в области влажного пара не прямолинейны.
В области влажного пара наносится система линий постоянной степени сухости (x=const). Построение их основано на том, что каждая из этих линий делит все изобары влажного пара на пропорциональные отрезки. Обычно на i-s диаграмму наносится и система изохор u=const, которые по своему характеру близки к изобарам, но идут несколько круче и в области влажного пара не прямолинейны.
29. Схемы и циклы Карно для тепловых и холодильных машин. Т-s и p-v диаграммы циклов. Показатели эффективности.
В большинстве случаев производство искусственного холода основано на совершении холодильным агентом обратного цикла. Наиболее экономичным из обратных циклов является обратный цикл Карно.
Ts-диаграмма этого цикла 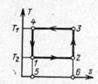
При изотермическом расширении по линии 1-2 холодильный агент получает от охлаждаемого объекта тепло q2= пл. 1-2-6-5-1 при температуре Т2. Затем холодильный агент подвергается сжатию по линии 2-3, в результате чего его температура повышается до T 1, которую имеет теплоприемник, т. е. окружающая среда. Вступив в контакт с ней, холодильный агент в процессе 3-4 отдает ей тепло q1= пл. 3-4-5-6-3, после чего он адиабатно расширяется по линии 4-1 с понижением температуры до T2, чем цикл и завершается. Для осуществления этого цикла необходимо затратить работу l0, измеряемую площадью, которая ограничена линией цикла 1-2-3-4-1 и равна разности работ расширения и сжатия холодильного агента. Затраченная работа превращается в тепло и передается вместе с теплом охлаждаемого объекта теплоприемнику, т. е. q1= q2+ l0. Согласно 2-му закону термодинамики переход тепла от менее нагретого тела к более нагретому возможен только при дополнительной затрате и осуществляется путем совершения обратного цикла.

Основное уравнение Т.Б. идеального обратимого цикла: qв= qн + l. Где qн - количество теплоты, забираемое из камеры, l – работа. Эффективность обратного цикла определяется холодильным коэффициентом: ε = qн / l = qн / qв - qн = Tн·∆S /(T0 - Tн)·∆S = Tн /(T0 - Tн). Холодильный коэффициент не зависит от свойств рабочего тела и определяется лишь температурой охлаждаемой среды и воспринимаемой среды. l = qн / Tн·(T0 - Tн); соответственноудельная затрата работы на единицу получаемого холода: Эк= l / qн = (T0 - Tн) / Tн =(T0 / Tн) – 1. Тепловой насос работает аналогично, но при более высоких температурах. Эффективность теплового насоса характеризуется коэффициентом преобразования φ (отношением тепла, полученного телом с Тв к затраченной механической работе).
φ = qв / l = qв / qв – qо.
1. Газовые холодильные машины:


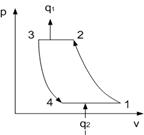
В воздушных холодильных машинах получение низкой температуры осуществля



 1.Ручные слоевые топки: схема топки.
1.Ручные слоевые топки: схема топки. 21. Горелочные устройства для твердого, жидкого и газообразного топлива. Виды горелок, особенности работы и конструкции. 1. Газовые горелки. Для сжигания газообразного топлива используются горелки различных типов. По давлению газа перед горелками они делятся на два основных типа - горелки низкого давления и горелки среднего давления Либо используется газ второй категории высокого давления В зависимости от конструкции горелки, используемые в котельных, бывают: 1) диффузионные н/давления и с/давления, 2) инжекционные н/давления и с/давления, 3) вихревые н/давления и с/давления.1) Диффузионные горелки – это горелки без предварительного смешения воздуха с топливом. Через горелку в топку подается газ, а воздух поступает по отдельным каналам. Примером дифф-й горелки является подовая щелевая горелка. Дост-во: 1.Простота. 2.Эти горелки дают меньший выход азота. Инжек-е горелки Устанавливаются на котлах малой производительности. Эти горелки используют энергию газовой струи для подсоса или инжектирования воздуха необходимого для горения горелки. Эти горелки при повышенной производительности имеют большие размеры. Дост-во: не требуют вентиляторов.
21. Горелочные устройства для твердого, жидкого и газообразного топлива. Виды горелок, особенности работы и конструкции. 1. Газовые горелки. Для сжигания газообразного топлива используются горелки различных типов. По давлению газа перед горелками они делятся на два основных типа - горелки низкого давления и горелки среднего давления Либо используется газ второй категории высокого давления В зависимости от конструкции горелки, используемые в котельных, бывают: 1) диффузионные н/давления и с/давления, 2) инжекционные н/давления и с/давления, 3) вихревые н/давления и с/давления.1) Диффузионные горелки – это горелки без предварительного смешения воздуха с топливом. Через горелку в топку подается газ, а воздух поступает по отдельным каналам. Примером дифф-й горелки является подовая щелевая горелка. Дост-во: 1.Простота. 2.Эти горелки дают меньший выход азота. Инжек-е горелки Устанавливаются на котлах малой производительности. Эти горелки используют энергию газовой струи для подсоса или инжектирования воздуха необходимого для горения горелки. Эти горелки при повышенной производительности имеют большие размеры. Дост-во: не требуют вентиляторов. 
 3
3 Экономайзеры – устройства, предназначенные для подогрева воды или воздуха в котельной установке с помощью тепла уходящих продуктов сгорания топлива, которые для лучшего теплообмена двигаются сверху вниз, а вода – снизу вверх. Экономайзер повышает КПД котельной установки. Область применения экономайзеров – нагрев питательной воды паровых котлов и воды систем теплоснабжения. Экономайзеры котла выполняют либо из гладких, либо из ребристых чугунных труб; на более высокие температуру и давление – из стальных гладких труб.
Экономайзеры – устройства, предназначенные для подогрева воды или воздуха в котельной установке с помощью тепла уходящих продуктов сгорания топлива, которые для лучшего теплообмена двигаются сверху вниз, а вода – снизу вверх. Экономайзер повышает КПД котельной установки. Область применения экономайзеров – нагрев питательной воды паровых котлов и воды систем теплоснабжения. Экономайзеры котла выполняют либо из гладких, либо из ребристых чугунных труб; на более высокие температуру и давление – из стальных гладких труб. (кДж/кг)) и на выходе из него (
(кДж/кг)) и на выходе из него (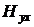 ) определяют тепловосприятие экономайзера по уравнению теплового баланса
) определяют тепловосприятие экономайзера по уравнению теплового баланса  , кВт, где BР - расчетный расход топлива, кг/с; φ - коэффициент сохранения теплоты; ΔHB -энтальпия, кДж/кг. Температуру воды на выходе из экономайзера
, кВт, где BР - расчетный расход топлива, кг/с; φ - коэффициент сохранения теплоты; ΔHB -энтальпия, кДж/кг. Температуру воды на выходе из экономайзера  , кВт, где
, кВт, где 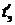 – температура воды на входе в экономайзер; св – теплоемкость воды, кДж/кг×оС; Dвэ - количество воды, проходящей через экономайзер, кг/с. Dвэ=Dнп+Dпр, где Dнп - расход насыщенного пара кг/с; Dпр - расход продувочной воды, кг/с. Для чугунного экономайзера
– температура воды на входе в экономайзер; св – теплоемкость воды, кДж/кг×оС; Dвэ - количество воды, проходящей через экономайзер, кг/с. Dвэ=Dнп+Dпр, где Dнп - расход насыщенного пара кг/с; Dпр - расход продувочной воды, кг/с. Для чугунного экономайзера  должна быть не менее чем на двадцать градусов ниже температуры насыщения для избежания кавитации.Среднюю разность температур с достаточной степенью точности можно определить как среднеарифметическую величину
должна быть не менее чем на двадцать градусов ниже температуры насыщения для избежания кавитации.Среднюю разность температур с достаточной степенью точности можно определить как среднеарифметическую величину 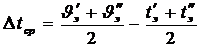 , оС, где
, оС, где 
 - температура газов до и после экономайзера Среднюю скорость газов в экономайзере подсчитывают по выражению
- температура газов до и после экономайзера Среднюю скорость газов в экономайзере подсчитывают по выражению , м/с. При этом живое сечение экономайзера Fэ=fэ×m выбирают таким образом (набирая различное количество труб в горизонтальном ряду), чтобы Wср была в пределах 6…9 м/с. Здесь m – число труб в горизонтальном ряду.kэ - коэффициент теплопередачи, Вт/м2×оС; Vг- объем газов.
, м/с. При этом живое сечение экономайзера Fэ=fэ×m выбирают таким образом (набирая различное количество труб в горизонтальном ряду), чтобы Wср была в пределах 6…9 м/с. Здесь m – число труб в горизонтальном ряду.kэ - коэффициент теплопередачи, Вт/м2×оС; Vг- объем газов. , м2. Число горизонтальных рядов определяется как n=Hвэ/hэ×m, где hэ - поверхность нагрева одной трубы, м2.
, м2. Число горизонтальных рядов определяется как n=Hвэ/hэ×m, где hэ - поверхность нагрева одной трубы, м2. Принципиальная схема котельной со стальными паровыми котлами, отпускающей пар на технологические нужды и горячую воду на теплоснабжение:
Принципиальная схема котельной со стальными паровыми котлами, отпускающей пар на технологические нужды и горячую воду на теплоснабжение: h′′- энтальпия перегретого пара, h′ - насыщенного пара Турбогенератор подбирается по расходу пара
h′′- энтальпия перегретого пара, h′ - насыщенного пара Турбогенератор подбирается по расходу пара , Кзагр=0,6 (т/ч) Подогреватель сетевой воды и охладитель конденсата выбираются согласно расчету требуемые данные: t0, τ1, Gсет, Qгвmax, Насосы подбираются по требуемому напору и расходу воды
, Кзагр=0,6 (т/ч) Подогреватель сетевой воды и охладитель конденсата выбираются согласно расчету требуемые данные: t0, τ1, Gсет, Qгвmax, Насосы подбираются по требуемому напору и расходу воды (к Вт)
(к Вт)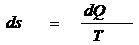 Ур-е состояния идеального газа или ур-ем Клапейрона - Менделеева pv = RTm/µ. Здесь р - давление газа, v - объем, занимаемый m килограммами (граммами) газа, µ - килограмм-моль (грамм-моль), R - универсальная газовая постоянная, T –температура. Килограмм-моль (грамм-моль) - число килограммов (граммов) вещества, численно равное молекулярному весу. Из уравнения (1) получаются законы Гей-Люссака, Шарля и Бойля-Мариотта. При постоянных p и m (так как R =const, а µ постоянно для данного вещества) v1=v0T1/T2,где v0 и T0 - объем и температура газа при 0°C. Отсюда следует закон Гей-Люссака (уравнение изобарического процесса): v = v0(1+t/273). При постоянных v и m получается закон Шарля (уравнение изохорического процесса): p = p0(1+t/273). При постоянных T и m (изотермический процесс) получается закон Бойля-Мариотта: p1v1 = p2v2. Величина 1/273 (1/град) называется коэффициентом объемного расширения или термическим коэффициентом давления идеального газа. Для реальных газов при давлениях, близких к атмосферному или больших, соответствующие коэффициенты несколько отличаются от этой величины.
Ур-е состояния идеального газа или ур-ем Клапейрона - Менделеева pv = RTm/µ. Здесь р - давление газа, v - объем, занимаемый m килограммами (граммами) газа, µ - килограмм-моль (грамм-моль), R - универсальная газовая постоянная, T –температура. Килограмм-моль (грамм-моль) - число килограммов (граммов) вещества, численно равное молекулярному весу. Из уравнения (1) получаются законы Гей-Люссака, Шарля и Бойля-Мариотта. При постоянных p и m (так как R =const, а µ постоянно для данного вещества) v1=v0T1/T2,где v0 и T0 - объем и температура газа при 0°C. Отсюда следует закон Гей-Люссака (уравнение изобарического процесса): v = v0(1+t/273). При постоянных v и m получается закон Шарля (уравнение изохорического процесса): p = p0(1+t/273). При постоянных T и m (изотермический процесс) получается закон Бойля-Мариотта: p1v1 = p2v2. Величина 1/273 (1/град) называется коэффициентом объемного расширения или термическим коэффициентом давления идеального газа. Для реальных газов при давлениях, близких к атмосферному или больших, соответствующие коэффициенты несколько отличаются от этой величины.

 pdv- работа расширения
pdv- работа расширения  vdp –техническая работа d(pv)= p2; v2-p1 v1 =
vdp –техническая работа d(pv)= p2; v2-p1 v1 =  pdv+vdp – работа проталкивания l′=l-l0 Энтальпия- параметр, характеризующий состояние системы.
pdv+vdp – работа проталкивания l′=l-l0 Энтальпия- параметр, характеризующий состояние системы.
 Энтопия – физическая величина изменение которой происходит при обмене энергии в форме теплоты в равновесном процессе
Энтопия – физическая величина изменение которой происходит при обмене энергии в форме теплоты в равновесном процессе  (Дж/К)
(Дж/К)
 ix =i’+xr U’’=U’+r, i”=i’+r,
ix =i’+xr U’’=U’+r, i”=i’+r,
 Рис.1
Рис.1 
 При подогреве жидкости удельный объем ее несколько увеличивается вследствие температурного расширения, процесс же парообразования характеризуется резким увеличением удельного объема. Построив в рv-диаграмме аналогичные графики для нескольких различных давлений и соединив одноименные точки плавными линиями (рис. 2), можно заметить, что в связи с очень малой сжимаемостью жидкости линия a-a1-а..., выражающая зависимость v0=f(p), практически вертикальна; в связи с тем, что при увеличении давления возрастает температура кипения, от которой зависит v', линия b-b1-b2..., выражающая зависимость v' = f(p), идет круто вверх с наклоном в правую сторону; наконец, линия c-с1-с2..., выражающая зависимость v" = f(p), имеет гиперболический характер. T-S диаграмма(рис.3): Все точки, соответствующие состоянию кипящей воды, в такой диаграмме размещаются на линии АК, т. е. на изобаре pкр, которая, следовательно, является и нижней пограничной кривой. Более того, на этой же изобаре лежат и все без исключения точки, соответствующие состоянию некипящей воды при разных давлениях, т.е. линия отражает состояние насыщенной жидкости. Степень сухости х = 0. i-s-диаграмма: Построение этой диаграммы, общий вид которой приведен на рис.4, осуществляется таким образом. По табличным значениям i', s', i" и s" строятся нижняя и верхняя пограничные кривые OK и KL, затем точки на этих кривых соответствующие одинаковым давлениям, соединяются прямыми линиями, образующими в области влажного пара пучок начинающихся в начале координат и расходящихся кверху изобар. Одновременно эти линии являются и изотермами.
При подогреве жидкости удельный объем ее несколько увеличивается вследствие температурного расширения, процесс же парообразования характеризуется резким увеличением удельного объема. Построив в рv-диаграмме аналогичные графики для нескольких различных давлений и соединив одноименные точки плавными линиями (рис. 2), можно заметить, что в связи с очень малой сжимаемостью жидкости линия a-a1-а..., выражающая зависимость v0=f(p), практически вертикальна; в связи с тем, что при увеличении давления возрастает температура кипения, от которой зависит v', линия b-b1-b2..., выражающая зависимость v' = f(p), идет круто вверх с наклоном в правую сторону; наконец, линия c-с1-с2..., выражающая зависимость v" = f(p), имеет гиперболический характер. T-S диаграмма(рис.3): Все точки, соответствующие состоянию кипящей воды, в такой диаграмме размещаются на линии АК, т. е. на изобаре pкр, которая, следовательно, является и нижней пограничной кривой. Более того, на этой же изобаре лежат и все без исключения точки, соответствующие состоянию некипящей воды при разных давлениях, т.е. линия отражает состояние насыщенной жидкости. Степень сухости х = 0. i-s-диаграмма: Построение этой диаграммы, общий вид которой приведен на рис.4, осуществляется таким образом. По табличным значениям i', s', i" и s" строятся нижняя и верхняя пограничные кривые OK и KL, затем точки на этих кривых соответствующие одинаковым давлениям, соединяются прямыми линиями, образующими в области влажного пара пучок начинающихся в начале координат и расходящихся кверху изобар. Одновременно эти линии являются и изотермами. В области влажного пара наносится система линий постоянной степени сухости (x=const). Построение их основано на том, что каждая из этих линий делит все изобары влажного пара на пропорциональные отрезки. Обычно на i-s диаграмму наносится и система изохор u=const, которые по своему характеру близки к изобарам, но идут несколько круче и в области влажного пара не прямолинейны.
В области влажного пара наносится система линий постоянной степени сухости (x=const). Построение их основано на том, что каждая из этих линий делит все изобары влажного пара на пропорциональные отрезки. Обычно на i-s диаграмму наносится и система изохор u=const, которые по своему характеру близки к изобарам, но идут несколько круче и в области влажного пара не прямолинейны.







