

Эмиссия газов от очистных сооружений канализации: В последние годы внимание мирового сообщества сосредоточено на экологических проблемах...

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...

Эмиссия газов от очистных сооружений канализации: В последние годы внимание мирового сообщества сосредоточено на экологических проблемах...

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...
Топ:
Когда производится ограждение поезда, остановившегося на перегоне: Во всех случаях немедленно должно быть ограждено место препятствия для движения поездов на смежном пути двухпутного...
Устройство и оснащение процедурного кабинета: Решающая роль в обеспечении правильного лечения пациентов отводится процедурной медсестре...
Интересное:
Как мы говорим и как мы слушаем: общение можно сравнить с огромным зонтиком, под которым скрыто все...
Наиболее распространенные виды рака: Раковая опухоль — это самостоятельное новообразование, которое может возникнуть и от повышенного давления...
Мероприятия для защиты от морозного пучения грунтов: Инженерная защита от морозного (криогенного) пучения грунтов необходима для легких малоэтажных зданий и других сооружений...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Пример 1. 0,1 моль спирта распределяется между 300 мл воды и 500 мл CCl4. Найдите концентрации спирта (моль/л) в равновесных растворах. Коэффициент распределения этилового спирта между четырёххлористым углеродом и водой равен 0,0244.
Решение: По закону распределения: 
где С1 – концентрация растворённого вещества в первом растворителе (CCl4);
С2 – концентрация растворённого вещества во втором растворителе (Н2О).
К – коэффициент распределения
Число молей спирта, перешедшего в четырёххлористый углерод обозначим через Х, тогда: 
В воду перейдет оставшееся количество спирта, равное (0,1 – Х) моль, следовательно: 
Подставив С1 и С2 в уравнение получим 
Откуда Х = 0,0039 моль
 моль/л
моль/л  моль/л
моль/л
Пример 2. 0,3 г кристаллического йода растворено в 1 л воды. Рассчитайте эффективное число ступеней экстракции этого раствора сероуглеродом, если сероуглерод берётся порциями по 100 мл. Конечная концентрация йода в воде составляет 1×10-6 г/л? Коэффициент распределения йода между водой и сероуглеродом равен 0,0017.
Решение:
Формула расчёта процесса экстракции: 
где g0 – исходное количество вещества, подвергающееся экстрагированию;
V0 – объём раствора, в котором находится экстрагируемое вещество;
Vэ – объём растворителя (экстрагента), израсходованный на одно экстрагирование;
n – общее число ступеней экстракции; К – коэффициент распределения.

 lg gn = lg g0 + n lg KV0 , откуда
lg gn = lg g0 + n lg KV0 , откуда
Vэ + KV0
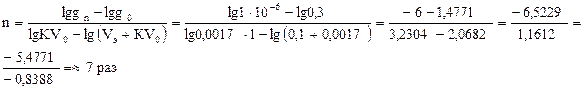
Задачи для самостоятельного решения
91 - 100. Cмешалиn1 моля спирта с объёмом V1 мл четыреххлористого углерода и объёмом V2 мл воды. Определитеконцентрации растворов этилового спирта в четыреххлористом углероде и воде. Коэффициент распределения этилового спирта между четыреххлористым углеродом и водой равен 0,0244.
|
|
| параметры | № задачи | |||||||||
| n1, моль | 0,2 | 0,22 | 0,24 | 0,26 | 0,28 | 0,3 | 0,32 | 0,34 | 0,36 | 0,38 |
| V1, мл | ||||||||||
| V2, мл |
101 - 110. Необходимо извлечьопределённое количество%(масс.) кислоты из V1 мл раствора кислоты в эфире. Сколько для этого необходимо взять воды в качестве экстрагента при числе ступеней экстракции равном n, если коэффициент распределения кислоты между водой и эфиром равен К?
| параметры | № задачи | |||||||||
| % (масс.) кислоты | ||||||||||
| V1, мл | ||||||||||
| n | ||||||||||
| К |
111 - 120. Рассчитайте, какое количество HgBr2 можно извлечь из объёма V1 мл концентрацией См моль/л водного раствора с помощью объёма V2 мл бензола n -кратной экстракцией. Коэффициент распределения HgBr2 между водой и бензолом равен 0,893.
| параметры | № задачи | |||||||||
| V1, мл | ||||||||||
| См, моль/л | 0,01 | 0,02 | 0,03 | 0,04 | 0,05 | 0,06 | 0,07 | 0,08 | 0,09 | 0,1 |
| V2, мл | ||||||||||
| n |
Тема 2.
Растворы – физико-химические системы.
Коллигативные свойства растворов.
Растворимость
Пример 1. Определение массы газа в растворе по его растворимости.
Сколько хлороводорода HCI растворится в 100 л воды при 40ºС и давлении 98625 Па, если растворимость HCI при этой температуре и давлении 1,0133×105 Па составляет 386 м3 на 1 м3 воды?
Решение.
Растворимость (или коэффициент растворимости) выражают массой вещества (г), которое можно растворить в 100 г растворителя при данной температуре.
Определяем объём HCI, содержащегося в 100 л воды при 40ºС и давлении 1,0133×105 Па:
1000 л H2O — 386 м3
|
|
100 л H2O — х м3 х =  м3
м3
Массу HCI вычисляем по уравнению Менделеева – Клайперона;
М (HCI) = 36,46 г/моль. Тогда:
m = 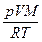 =
=  53,4 кг.
53,4 кг.
Пример 2. Определение состава газовой смеси по растворимости газов.
Газовая смесь, содержащая 21% O2 и 79% N2, пропущена через воду при 0ºС и давлении 1,0133×105 Па. Вычислите объёмные доли φ газовой смеси, растворённой в воде, если растворимость кислорода и азота в воде при этой температуре и давлении соответственно равна 0,048 и 0,0236 м3 на 1 м3 воды.
Решение.
Согласно закону Генри растворимость (Р) газа в воде пропорциональна его парциальному давлению в смеси. Определим парциальное давление газов в смеси:
p О2 = 1,0133 × 105 × 0,21 = 0,2128 × 105 Па;
p  = 1,0133 × 105 × 0,79 = 0,8005 × 105 Па.
= 1,0133 × 105 × 0,79 = 0,8005 × 105 Па.
Учитывая парциальные давления, определяем растворимость газов:
Р 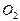 =
=  = 0,0104 м3;
= 0,0104 м3;
Р  =
=  = 0,0189 м3.
= 0,0189 м3.
Общий объём азота и кислорода; 0,0104 + 0,0189 = 0,0293 м3. Тогда объёмная доля газов и смеси составит (%):
φ 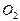 = 0,0104×100/0,0293 = 35,49; φ
= 0,0104×100/0,0293 = 35,49; φ  = 100,00 – 35,49 = 64,51.
= 100,00 – 35,49 = 64,51.
Задачи для самостоятельного решения
121 - 130. В воде при 20ºС и общем давлении 2,5×105 Па растворена газовая смесь, состоящая из О2, N2 и Cl2. Объёмные доли этих газов в смеси соответственно равны ω (О2), ω (N2) и ω (Cl2) %. Растворимость газов в 1 м3 воды (м3): РО2 = 0,031; РN2 = 0,016; РCl2 = 2,299. Определите объёмные доли газов в газовой смеси, растворённой в воде.
| параметры | № задачи | |||||||||
| ω (О2) % | ||||||||||
| ω (N2) % | ||||||||||
| ω (Cl2) % |
131 - 140. В некотором объёме V1 л воды растворен объём V2 л вещества А при температуре t ºС и давлении Р Па. Определите массовую долю вещества А в полученном растворе.
| параметры | № задачи | |||||||||
| V1, л (вода) | 0,05 | 0,09 | 0,3 | 1,2 | 1,4 | 1,5 | 1,9 | 2,6 | 5,7 | 3,5 |
| V2, л (в-во А) | 4,9 | 6,3 | 10,5 | 2,7 | 3,1 | 9,7 | 8,5 | 10,2 | 11,6 | 13,4 |
| в-во А | HCl | HCl | HCl | HBr | HBr | NH3 | NH3 | H2S | H2S | H2S |
| t, ºС | ||||||||||
| Р, Па×105 | 1,0 | 1,03 | 1,06 | 1,09 | 1,1 | 1,12 | 1,14 | 1,16 | 1,18 | 1,2 |
Физико-химические свойства
|
|
|

Типы оградительных сооружений в морском порту: По расположению оградительных сооружений в плане различают волноломы, обе оконечности...

Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов (88‰)...

Биохимия спиртового брожения: Основу технологии получения пива составляет спиртовое брожение, - при котором сахар превращается...

Опора деревянной одностоечной и способы укрепление угловых опор: Опоры ВЛ - конструкции, предназначенные для поддерживания проводов на необходимой высоте над землей, водой...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!