В зависимости от взаимной растворимости компонентов
1. Компоненты с неограниченной взаимной растворимостью
А) идеальные (подчиняются закону Рауля)
Б) не идеальные (с положительным или отрицательным отклонением от закона Рауля).
2. Взаимно не растворимые.
3. Ограниченно растворимые друг в друге.
Идеальные смеси.
Если смесь бинарная, то при изменении трех параметров ( можно построить фазовую диаграмму типа:
можно построить фазовую диаграмму типа:
1. При постоянной температуре 
2. 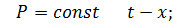
3. 
Идеальные смеси – такие бинарные смеси, которые подчиняются закону Рауля.
При постоянной температуре парциальное давление компонента в паре пропорционально мольной доле этого компонента в жидкости. Коэффициент пропорциональности – это давление насыщенного пара данного компонента при этой температуре.
а – НК
в – ВК

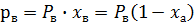
В процессах перегонки и ректификации все расчеты выполняются в мольных долях по НК. Закон Рауля выражают графически в виде  , зафиксировав постоянную температуру.
, зафиксировав постоянную температуру.

Пользуясь диаграммой  (при
(при  ) можно определить температуры кипения смеси различного состава.
) можно определить температуры кипения смеси различного состава.
 парциальное давление ВК.
парциальное давление ВК.
Если построить так же линии для более высоких температур. То соответственно 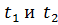 будут выглядеть:
будут выглядеть:
Отмечаем на оси  внешнее давление и проводим на оси х горизонтальную линию MN – линия внешнего давления в системе. Жидкость состава
внешнее давление и проводим на оси х горизонтальную линию MN – линия внешнего давления в системе. Жидкость состава 
В точке А сумма парциальных давлений равна общему давлению в системе, эта точка при которой система данного состава будет кипеть. 


По кипению жидкой фазы можно определить температуру кипения – это позволит построить еще одну диаграмму ( .
.

 - смесь, обогащенная по НК,
- смесь, обогащенная по НК,
 - смесь, обогащенная по ВК.
- смесь, обогащенная по ВК.
На этой же диаграмме построим зависимость  , т.е. состав пара – температура конденсации пара.
, т.е. состав пара – температура конденсации пара.



где  давление насыщенного пара компонента
давление насыщенного пара компонента  ;
;
 - мольная доля компонента
- мольная доля компонента  в жидкой фазе;
в жидкой фазе;
 - общее давление в системе (внешнее);
- общее давление в системе (внешнее);
 - мольная доля компонента
- мольная доля компонента  в паровой фазе.
в паровой фазе.
Эта диаграмма позволяет найти по составу жидкой фазы при ее температуре кипения состав пара при этой же температуре.

Мольная доля НК в паре больше чем в кипящей жидкости, т.е. пар обогащается по НК компоненту.

Диаграмма х-у (состав жидкости – состав пара).

Эта диаграмма строится при 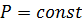 . Линия равновесия определяется уравнением:
. Линия равновесия определяется уравнением:

Где  -коэффициент летучести (определяется экспериментально). Поэтому линию равновесия и строят исходя из экспериментальных данных. Расположение
-коэффициент летучести (определяется экспериментально). Поэтому линию равновесия и строят исходя из экспериментальных данных. Расположение  и
и  определяется первым законом Коновалова: пар обогащается тем компонентом, при добавлении которого к жидкости, повышается давление пара над ней, т.е. снижается ее температура кипения.
определяется первым законом Коновалова: пар обогащается тем компонентом, при добавлении которого к жидкости, повышается давление пара над ней, т.е. снижается ее температура кипения.
Для идеальной жидкости линия равновесия – парабола.
Закон Коновалова дополняется первым законом Вревского, согласно которому при повышении температуры кипения раствора двух жидкостей, в парах возрастает относительное содержание того компонента, переход которого в парообразную фазу потребует большей затраты тепла.
Реальные смеси (РС).

1. С неограниченной взаимной растворимостью (спирт-вода);
2. С ограниченной взаимной растворимостью (20-30%);
3. Взаимно не растворимые (бензол-вода).
РС имеют отклонение от закона Рауля.
Если линия выпуклая по отношению к прямой, то такие смеси с положительным отклонением от закона Рауля. Если вогнутая - с отрицательным отклонением от закона Рауля.
Для  диаграмма х-Р, ху-t и ху строится по опытным данным.
диаграмма х-Р, ху-t и ху строится по опытным данным.
Для ряда смесей количественное отклонение от закона Рауля настолько велики, что приводят к качественным изменениям в свойствах этой смеси: при определенном составе жидкой фазы такие смеси имеют определенную температуру кипения. Причем эта температура может быть либо выше температуры кипения ВК, либо ниже температуры кипения НК. Такие смеси называют азеотропными.


Сдвинуть азеотропную точку в ту или иную сторону можно путем изменения внешнего давления в системе.
Направление сдвига определяется вторым законом Вревского: при повышении температуры азеотропной смеси, обладающей максимумом давления пара, в смеси увеличивается относительное содержание того компонента, парциально-мольная теплота которого больше - ВК. Для смеси с минимумом давления пара возрастет содержание того компонента, парциально-мольная теплота которого меньше – НК.



 можно построить фазовую диаграмму типа:
можно построить фазовую диаграмму типа:
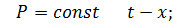


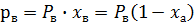
 , зафиксировав постоянную температуру.
, зафиксировав постоянную температуру.
 ) можно определить температуры кипения смеси различного состава.
) можно определить температуры кипения смеси различного состава. парциальное давление ВК.
парциальное давление ВК.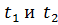 будут выглядеть:
будут выглядеть: внешнее давление и проводим на оси х горизонтальную линию MN – линия внешнего давления в системе. Жидкость состава
внешнее давление и проводим на оси х горизонтальную линию MN – линия внешнего давления в системе. Жидкость состава 



 .
.
 - смесь, обогащенная по НК,
- смесь, обогащенная по НК, - смесь, обогащенная по ВК.
- смесь, обогащенная по ВК. , т.е. состав пара – температура конденсации пара.
, т.е. состав пара – температура конденсации пара.

 давление насыщенного пара компонента
давление насыщенного пара компонента  ;
; - мольная доля компонента
- мольная доля компонента  - мольная доля компонента
- мольная доля компонента 


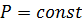 . Линия равновесия определяется уравнением:
. Линия равновесия определяется уравнением:
 -коэффициент летучести (определяется экспериментально). Поэтому линию равновесия и строят исходя из экспериментальных данных. Расположение
-коэффициент летучести (определяется экспериментально). Поэтому линию равновесия и строят исходя из экспериментальных данных. Расположение  и
и  определяется первым законом Коновалова: пар обогащается тем компонентом, при добавлении которого к жидкости, повышается давление пара над ней, т.е. снижается ее температура кипения.
определяется первым законом Коновалова: пар обогащается тем компонентом, при добавлении которого к жидкости, повышается давление пара над ней, т.е. снижается ее температура кипения.
 диаграмма х-Р, ху-t и ху строится по опытным данным.
диаграмма х-Р, ху-t и ху строится по опытным данным.



