Гетеротрофные и аутотрофные организмы: различия по питанию и источникам энергии; катаболизм и анаболизм.
Гетеротрофы – организмы, использующие для своего питания готовые органические вещества.
Автотрофы – организмы, использующие углекислый газ в качестве исходного питательного материала для построения других углеродсодержащих веществ. (автотрофы синтезируют из СО2 восстановленные органические вещества (н-р: глюкоза), содержащие большой запас энергии)
По способу получения энергии автотрофы подразделяются на фотоавтотрофы и хемоавтотрофы.
Фотоавтотрофные бактерии используют энергию солнечных лучей при синтезе органических веществ из двуокиси углерода по типу фотосинтеза у растений.
Хемотрофы – потребляют энергию ОВР.
Метаболизм – процесс из 2-х фаз: катаболизм (энергетический обмен) и анаболизм (пластический обмен).
Катаболизм(диссимиляция) – расщепление сложных органических молекул до более простых конечных продуктов. Углеводы, жиры, белки распадаются в ходе последовательных реакций до углекислого газа (СО2), воды (Н2О), аммиака (NН3). На определенных этапах соответствующих катаболических путей значительная часть свободной энергии запасается благодаря сопряженным ферментативным реакциям в форме высокоэнергетического соединения АТФ (аденозинтрифосфата). Часть запасается также в богатых энергией водородных атомов НАДН или НАДФН.
Анаболизм(ассимиляция) – биосинтез – фаза метаболизма, в которой из малых молекул – предшественников (аминокислот, моносахаридов, жирных кислот, азотистых оснований) синтезируются белки, полисахариды, нуклеиновые кислоты и др. макромолекулы. Анаболизм требует затраты свободной энергии. Источник этой энергии – АТФ и НАДФН.
2. Пентозофосфатный путь превращения глюкозы – прямое окисление глюкозы.
Состоит из 2-х стадий:
1)Окислительная (до образования рибозо-5-Ф)
2)Неокислительная

3. Распад гемма. Образование билирубина и билирубинглюкуронидов. Пути выведения  желчных пигментов. Желтухи.
желчных пигментов. Желтухи. 
Желтухи:
1)Гемолитическая – связана с массовым разрушением эритроцитов, при этом образуется небольшое количество билирубина, который печень не успевает конъюгировать.
В крови повышается содержание непрямого билирубина.
2)Механическая (обтурационная) – при наличии препятствия в желчевыводящих путях (камень, опухоль, отек)
В крови возрастает уровень прямого билирубина.
3)Печеночно-клеточная – воспалительные процессы (инфекционные гепатиты), токсические поражения печени, цирроз, жировая инфильтрация, рак печени.
Нарушены все три стадии: элиминация из крови, конъюгация (недостаток глюкуронил ТФ), выведение.
В крови повышены обе фракции билирубина.
Задача. Больной жалуется на снижение остроты зрения, плохое сумеречное зрение. При осмотре отмечается шелушение кожных покровов. Из анамнеза выявлено, что больной страдает хронической желчно-каменной болезнью. С недостаточностью какого витамина вы столкнулись? Каков механизм действия этого витамина? Какие меры необходимо предпринять?
Недостаточность витамина А. Механизм действия! Ретинол, поступающий с пищей в организм (человека), может быть в свободном и эстерифицированном виде: всасывание происходит в тонкой кишке. После всасывания эстерифицированный ретинол поступает преимущественно в лимфу, а также непосредственно в кровь и оттуда — в ткани. Накапливается главным образом в печени, почках, сетчатке глаза в виде эфиров с высшими жирными кислотами (стеариновой, пальмитиновой и др.) Ретинол принимает участие в регуляции трофических процессов и повышении сопротивляемости организма к инфекциям. Применение ретинола повышает барьерную функцию слизистых оболочек, в первую очередь дыхательных путей, пищеварительного тракта и мочевых путей, препятствуя замещению мукопротеидов эпителиальных клеток кератином, увеличивает фагоцитарную активность лейкоцитов и других факторов не специфической сопротивляемости организма. Ретинол оказывает стимулирующее воздействие на окислительные процессы в организме, способствует нормализации различных видов обмена. Активно воздействуя на работу зрительных пигментов, сенсибилизирующих сетчатку глаза к свету, он соединяется с белком опсином и образует родопсин, который на свету разлагается на ряд соединений, при этом происходит серия реакций, приводящих к генерации нервных импульсов. Таким образом, значение витамина А для зрения неоценимо и естественно, что одним из проявлений авитаминоза А является плохая адаптация глаз к темноте, прогрессирующая до ночной слепоты. Витамин А также участвует и в других физиологических процессах. Он необходим для нормального развития костей, поэтому одно из проявлений его дефицита — прекращение роста костей. Ретинол также необходим для нормального эмбрионального развития, для поддержания эпителиальных тканей, процесса сперматогенеза и внутриутробного развития плода. Принимая участие в синтезе стероидных гормонов, сперматогенезе, он является антагонистом тироксина — гормона щитовидной железы.
Действия:
Диета: в ежедневном рационе обязательно должны быть продукты с высоким содержанием витамина А – сливочное масло, сыр, сливки, желток, рыбий жир, говяжья печень, печень трески и богатые каротином – болгарский перец, морковь, шиповник, облепиха, черная смородина, зеленные культуры, абрикосы.
Применение витамина а: врач может назначить применение витамина А на период до двух до четырех недель. Дозировка и способы применения подбираются врачом, так как существует опасность гипервитаминоза А.
При поражениях глаз возможно применение рибофлавина по назначению врача.
2билет.
Процессинг пре-мРНК
1) Вырезание неинфомативных участков (интронов) пре-мРНК с помощью рибонуклеаз:
они гидролизуют фосфодиэфирные связи,начиная с 5-конца,и оставляют от пре-мРНК необходимую часть готовой мРНК.
2) Экзоны сращиваются в единую цепь с помощью РНК-лигаз.
3) Модификация 5- и 3-концов обр-ся мРНК:
К 5-концу присоединяется олигонуклеотид, который состоит из 2х или 3х метилированных нуклеотидов.
К 3-концу (у эукариот) присоединяется полиадениловый фрагмент – поли(А) с помощью поли(А)-полимеразы.
Процессинг пре-рРНК
Пре-рРНК обр-ся в ядрышке,где находятся транскриптоны рРНК. В ДНК ядрышка гены 18S и 28S рРНК входят в один транскриптон,где расположены попарно друг за другом. В пре-РНК их расположение такое же.
Размеры пре-рРНК достигают 45S. А в ходе процессинга остается чуть больше половины пре-рРНК и освобождаются зрелые 18S и 28S рРНК.
Часть нуклеотидов РНК подвергается модофикации (метилирование основанией метилтрансферазами).
Зрелые рРНК соединяются в ядре с белками рибосом и образуют малую и большую субъединицы рибосом.
Процессинг пре-тРНК.
Пре-тРНК содержит излишки примерно в 40 нуклеотидов. Они удаляются рибонуклеазами.
Затем происходит метилирование оснований тРНК.
Окончастельно зрелая тРНК образуется путем присоединения акцепторного конца (ЦЦА) с помощью спец-й РНК-полимеразы.
- Задача. Объясните, почему при употреблении в пищу преимущественно кукурузы и малого количества мяса возникает пеллагра? Напишите формулу соединения для лечения.
Пелла́гра — заболевание, один из авитаминозов, который является следствием длительного неполноценного питания (недостаток витамина PP и белков, в особенности содержащих незаменимую аминокислоту триптофан).
Для лечения применяется никотинамид, близкий по строению к никотиновой к-те (ликвидирует недостаток витамина ПП). 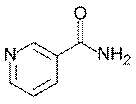
5билет.
- Охарактеризуйте четвертый класс ферментов: тип катализируемых реакций и назовите важнейшие группы ферментов внутри класса. Назовите несколько представителей и напишите химизм реакций.
Лиазы – ферменты, катализирующие разрыв С-О, С-С, C-N и других связей, а также обратимые реакции отщепления различных групп негидролитическим путем. Выделяют 7 подклассов. Эти реакции сопровождаются образованием двойной связи или присоединением групп к месту двойной связи. Лиазы являются сложными ферментами. Коферментами служат: пиридоксальфосфат, тиаминдифосфат, участвует магний, кобальт.
Ферменты делятся на подклассы в зависимости от природы атакуемой связи. Примером являются ферменты, действующие на углерод-углеродные связи, углерод-кислородные связи, углерод-азотные связи.
Если рассматривать все подклассы, то в них выделяются:
4.1. углерод-углерод лиазы;
4.2. углерод-кислород лиазы;
4.3. углерод-азот лиазы;
4.4. углерод-сера лиазы;
4.5. фосфор-кислород лиазы.
Среди подподклассов выделяют, например, карбокси-лиазы (4.1.1.), гидро-лиазы 4.2.1.).
Систематическое название образуется: Расщепляемый субстрат: отделяемая группа – лиаза
| Систематическое название
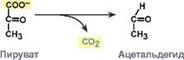
| 2-оксокислота:карбокси-лиаза
|
| Рабочее название
| Пируватдекарбоксилаза
|
| Систематическое название
| АТФ:дифосфат-лиаза (циклизующая)
|
| Рабочее название
| Аденилатциклаза
|

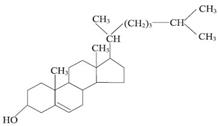
- Представление о биосинтезе холестерина.
Углеродный скелет холестерина целиком состоит из углерода уксусной кислоты.
Биосинтез холестерина из ацетил-КоА происходит с участием ферментов ЭПС и гиалоплазмы многих тканей и органов. Наиболее активен этот процесс в печени взрослого человека.
Происходит в 3 этапа:
- Образование мевалоновой кислоты из ацетил-КоА
- Образование б-гидрокси-б-метилглутарил-КоА из ацетил-КоА


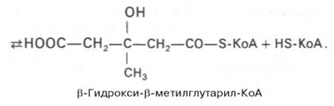
Далее б-гидрокси-б-метилглутарил-КоА под д-ем гидроксиметилглутарил-КоА-редуктазы превращается в мевалоновую кислоту:

Эта реакция необратима.
- Синтез из мевалоновой кислоты «активного изопрена» с конденсацией последнего в сквален;
Мевалоновая кислота в ходе нескольких ферментных реакций, в которых расходуется АТФ, превращается в изопентилпирофосфат и его изомер 3,3-диметилаллилпирофосфат. Эти оба в-ва и есть «активный изопрен», который используется на обр-е сквалена.
- Превращение сквалена в холестерин.
Сквален à Ланостерин à Холестерин
Гидроксилирование стероидного кольца протекает с участием монооксигеназной цепи мембран ЭПС.
Эфиры холестерина обр-ся (особенно активно в слизистой кишечника и печени) путем переноса ацила с ацил-КоА или с фосфатидилхолина на гидроксильную группу холестерина.
Фосфатидилхолин + Холестерин àЛизофосфатидилхолин + Эфир холестерина
(кат-ся фосфатидилхолин-холестерин-ацилтрансферазой).
Т.о., холестерин в тканях может синтезироваться из любых в-в,при распаде к-х обр-ся ацетил-КоА (углеводы, АК, ЖК, глицерин).
- Глюкозо-аланиновый цикл и его биологическая роль.
В условиях голодания часть белков мышечной ткани распадается до аминокислот, которые далее включаются в процесс катаболизма. Аминокислоты, которые при катаболизме превращаются в пируват или метаболиты цитратного цикла, могут рассматриваться как потенциальные предшественники глюкозы и гликогена и носят название гликогенных. Например, окса-лоацетат, образующийся из аспарагиновой кислоты, является промежуточным продуктом как цитратногр цикла, так и глюконеогенеза.
Из всех аминокислот, поступающих в печень, примерно 30% приходится на долю аланина. Это объясняется тем, что при расщеплении мышечных белков образуются аминокислоты, многие из которых превращаются сразу в пируват или сначала в оксалоацетат, а затем в пируват. Последний превращается в аланин, приобретая аминогруппу от других аминокислот. Аланин из мышц переносится кровью в печень, где снова преобразуется в пируват, который частично окисляется и частично включается в глюкозонеогенез. Следовательно, существует следующая последовательность событий (глюкозо-аланиновый цикл): глюкоза в мышцах → пируват в мышцах → аланин в мышцах → аланин в печени → глюкоза в печени → глюкоза в мышцах (рис. 7-52). Весь цикл не приводит к увеличению количества глюкозы в мышцах, но он решает проблемы транспорта аминного азота из мышц в печень и предотвращает лактоацидоз.
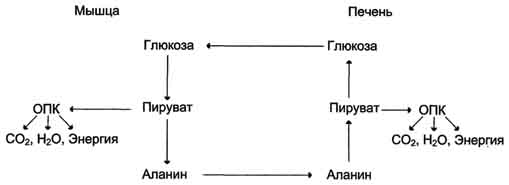
- Задача. Больной недавно приехал с Севера. Жалуется на сильные головные боли, недомогание. Под кожей заметны точечные кровоизлияния. При опросе оказалось, что больной часто употреблял в пищу печень белого медведя. С каким гипервитаминозом вы имеете дело? Каков механизм действия этого витамина?
Гипервитаминоз А – это состояние, развивающееся при чрезмерном поступлении и накоплении в организме витамина А (ретинол).
Ретинол является жирорастворимым витамином, поэтому его избыток плохо выделяется с мочой, что приводит к накоплению витамина в организме. В обычных дозах ретинол участвует в световосприятии (чувствительность глаз к свету), обновлении кожи (регенерации) и созревании сперматозоидов (мужских половых клеток). В повышенных дозах действует токсически (оказывает отравляющее действие на организм), особенно на печень.

6билет.
Задача. Больная страдает частыми носовыми кровотечениями. При сборе анамнеза было установлено, что она систематически принимает препараты салициловой кислоты. О каком гиповитаминозе может идти речь? В чем состоит действие этого витамина, его биологическая роль?
Гиповитаминоз витамина С. Витамин С – кофермент пролингидроксилазы. Гидроксипролин содержится в коллагене, который является основным веществом соединительной ткани.
Участвует в окислительно-восстановительных процессах. В р-ях гидроксилирования пролина и лизина при синтезе коллагена, синтезе гормонов надпочечников(кортикостероидов), АК триптофана.Участие в окислительном распаде тирозина и гемоглобина в тканях.
7билет
Связанные с ДНК
Гистоны — обширный класс ядерных белков, выполняющих две основные функции: они участвуют в упаковке нитей ДНК в ядре и в эпигенетической регуляции таких ядерных процессов, как транскрипция, репликация и репарация. Существует пять различных типов гистонов H1/Н5, H2A, H2B, H3, H4. Гистоны H2A, H2B, H3, H4, называемых кóровыми гистонами, формируют нуклеосому, представляющую собой белковую глобулу, вокруг которой накручена нить ДНК. Гистон H1/H5, называемый линкерным гистоном, связывается с внешней стороной нуклеосомы, фиксируя на ней нить ДНК. В хроматине гистоны составляют 25-40 % сухого веса.
Негистоновые (кислые) белки. В хромосомах их количество приблизительно вдвое меньше гистоновых. Существует более 100 видов негистоновых белков. Они разнообразны по молекулярному весу, структуре, видоспецифичны. Эти белки могут быть ответственны за репликацию, репарацию, транскрипцию, возможно, играют роль и в активации генов. К ним относят актин, миозин, тубулин, ферменты синтеза РНК и ДНК - полимеразы и другие.
Связанные с РНК
Белки РНП участвуют в упаковке нитей РНК и влияют на ее регуляцию.
2. Субстратное фосфорилирование, Напишите реакцию с участием фосфоенолпирувата.
Субстратное фосфорилирование –синтез АТФ из АДФ и фосфорной кислоты с использованием энергии высокоэнергетического субстрата. Этот способ синтеза АТФ не требует присутствия кислорода, т.е. происходит в анаэробных условиях. Реакции субстратного фосфорилирования происходят: 1) в процессе гликолиза (макроэргические субстраты - 3-фосфо-глицерат и фосфоенолпируват); 2) с использованием креатинфосфата; 3) в одной реакции ЦТК, с использованием макроэргического субстрата – сукцинил-КоА.
Фосфоенолпируват превращается в пируват под действием пируваткиназы.

Классификация углеводов
Согласно современной классификации углеводы подразделяются на три основные группы: моносахариды, олигосахариды и полисахариды.

Моносахариды подразделяются на альдозы и кетозы в зависимости от наличия альдегидной или кетогруппы. Альдозы и кетозы, в свою очередь, разделяются в соответствии с числом атомов углерода в молекуле: триозы, тетрозы, пентозы, гексозы и т.д.
Олигосахариды делятся по числу моносахаридов в молекуле: дисахариды, трисахариды и т.д.
Полисахариды подразделяют на гомополисахариды, т.е. состоящие из одинаковых моносахаров, и гетерополисахариды, состоящие из различных моносахаров.
Потребность в углеводах взрослого организма составляет 350-400 г в сутки, при этом целлюлозы и других пищевых волокон должно быть не менее 30-40 г. С пищей в основном поступают крахмал, гликоген, целлюлоза, сахароза, лактоза, мальтоза, глюкоза и фруктоза, рибоза.
Переваривание углеводов.
РОТОВАЯ ПОЛОСТЬ. Слюна (pH=6,8) сдержит гликолитический фермент альфа-амилазу, которая расщепляет крахмал и гликоген до дисахаридов и мальтозы. Альф-амилаза не гидролизует связи в дисахаридах.
ЖЕЛУДОК. Нет ферментов, расщепляющих У. Из-за низкой рН амилаза инактивируется, хотя некоторое время расщепление углеводов продолжается внутри пищевого комка.
Тонкий КИШЕЧНИК. В верхних отделах кишечника с секретовм подж. железы поступает панкреатическая альфа-амилаза. Гидролиз крахмала и декстрина идёт до мальтоза, изомальтозы и олигосахаридов (3-8 молекулы глюкозы в цепи).
В тонком кишечнике ферменты действуют на поверхности ворсинок, покрытых эптелиальными клетками. Здесь идёт дальнейшее переваривание промежуточных продуктов, а также гидролиз дисахаридов пищи (сахарозы и лактозы) под действием ферментативных комплексов:
1) сахаразо-изомальтазный – имеет 2 каталитические субъединицы: сахарази и изомальтаза.
Сахараза – гидролизует сахарозу до глюкозы и фруктозы. Изомальтаза гидролизует изомаьтозу до глюкозы.
2) Гликоамилазный комплекс:
Гидролизует альфа-1,4 связь в олигосахаридах и мальтозе с образованием глюкозы.
3) бета-гликозидазный комплекс (лактаза)
Расщепляет бета-1,4 гликозидную связь в лактозе с образованием галактозы и глюкозы.
Транспорт моносахаридов в клетки слизистой оболочки кишечника может осуществляться разными способами: путём облегчённой диффузии и активного транспорта.
1) Активный транспорт. Глюкоза и Na+ проходят через мембраны, связываясь с разными участками белка-переносчика. При этом Na+ поступает в клетку по градиенту концентрации, и одновременно глюкоза транспортируется против градиента концентрации. Градиент концентрации Na+, являющийся движущей силой активного симпорта, создаётся работой Nа+,К+-АТФ-азы. Перенос в клетки слизистой оболочки кишечника по механизму вторично-активного транспорта характерен также для галактозы. Благодаря активному транспорту эпителиальные клетки кишечника могут поглощать глюкозу при её очень низкой концентрации в просвете кишечника.
2) Облегчённая диффузия. Если же концентрация глюкозы в просвете кишечника велика, то она может транспортироваться в клетку путём облегчённой диффузии. Таким же способом может всасываться и фруктоза.
После всасывания моносахариды (главным образом, глюкоза) покидают клетки слизистой оболочки кишечника через мембрану, обращённую к кровеносному капилляру, с помощью облегчённой диффузии. Часть глюкозы (более половины) через капилляры кишечных ворсинок попадает в кровеносную систему и по воротной вене доставляется в печень. Остальное количество глюкозы поступает в клетки других тканей.
Основные пути катаболизма глюкозы: аэробный и анаэробный распады с высвобождением энергии. Поскольку в кишечнике всасываются все поступающие с пищей моносахариды (фруктоза, галактоза, манноза и т.п.), то перед организмом встает задача превратить полученные гексозы в глюкозу для ее дальнейшего использования в реакциях метаболизма – происходит взаимопревращение сахаров.
2. Окислительное фосфорилирование. Коэффициент Р/О.
Молекулы НАДН и ФАДН2, образуемые в реакциях окисления углеводов, жирных кислот, спиртов и аминокислот, далее поступают в митохондрии, где ферментами дыхательной цепи осуществляется процесс окислительного фосфорилирования.
Окислительное фосфорилирование – синтез АТФ из АДФ и фосфорной кислоты за счёт энергии, освобождающейся при окислении веществ, синтез которых сопряжён с переносом электронов по ДЦ.
Перенос электронов, происходящий на внутренней митохондриальной мембране, вызывает выкачивание ионов Н+ из матрикса митохондрий в межмембранное пространство. Это создает градиент концентрации ионов Н+ между цитозолем и замкнутым внутримитохондриальным пространством. Ионы водорода в норме способны возвращаться в матрикс митохондрий только одним способом – через специальный фермент, образующий АТФ – АТФ-синтазу.
ЦПЭ состоит из комплексов, каждый из которых осуществляет определённую стадию ОФ.
ДЦ включает в сея следующие комплексы:
I-НАДН-дг
II-Сукцинат-дг
III-убихинон-цитохром-с-редуктаза
IV-цитохромоксидаза

Электроны поступают в ДЦ двумя разными путями:
1 - если субстратами служат а-гидрокси-кислоты малат, изоцитрат, 3-гидроксибутират, водород переносится на NAD+. Образовавшийся NADH в дыхательной цепи, в свою очередь, окисляется NADH-дегидрогеназой (комплекс I).
2 - если субстратом служат такие соединения, как сукцинат или глицерол-3-фосфат, акцептором водорода служат FAD-зависимые дегидрогеназы (комплекс II).
Комплекс I переносит электроны через ФМН и железо-серные центры на убихинон.
Комплекс II также восстанавливает убихинон.
Восстановленный убихинонQH2 переносит электроны в комплекс III - QН2-дегидрогеназу (коэнзим Q-цитохром с-реуктаза), которая состоит из 2 типов цитохромов (b1 и b2) и цитохрома с1. Внутри комплекса III электроны передаются от цитохромов b на FeS-центры, на цитохром с1.
Затем комплекс III переносит электроны на цитохром с.
Цитохром С переносит электроны на комплекс IV – цитохромоксидазу, которая состоит из 2 цитохромов типа аа3. Комплекс цитохромов а-а3 непосредственно реагирует с молекулярным кислородом.
При восстановлении О2 образуется сильный основной анион О2-.
Реакции, сопровождающиеся образованием протонов, протекают на внутренней МХ мембране. Протоны переносятся с внутренней стороны мембраны на внешнюю. Таким образом, протоны водорода накапливаются в межмембранном пространстве, так как внутренняя мембрана для них непроницаема. Создаётся разность потенциалов: отрицательный заряд на внутренней стороне, положительный – на внешней. Повышение концентрации протонов в межмембранном пространстве активирует АТФ-синтазу. Электрохимический потенциал ΔμH+ заставляет протоны двигаться по каналу АТФ-синтазы в матрикс. Там они соединяются с анионом О2- и образуют воду. Параллельно под действием ΔμH+ происходят конформационные изменения в парах α, β-субъединиц белка F1, в результате чего из АДФ и неорганического фосфата образуется АТФ. Электрохимический потенциал, генерируемый в каждом из 3 пунктов сопряжения в ЦПЭ, используют для синтеза одной молекулы АТФ.
При окислении НАДН2 электроны проходят через три точки сопряжения: комплекс I, комплекс III и комплекс IV. Поэтому окисление молекулы NADH в ЦПЭ сопровождается накоплением большего электрохимического потенциала, и, как следствие, образованием 3 молекул АТФ. Электроны от FAD-зависимых дегидрогеназ поступают в ЦПЭ на KoQ, минуя первый пункт сопряжения. Электрохимический потенциал при этом меньше, и поэтому образуются только 2 молекулы АТФ.

Отношение количества фосфорной кислоты (Р), использованной на фосфорилирование АДФ, к атому кислорода (О), поглощённого в процессе дыхания, называют коэффициентом окислительного фосфорилирования и обозначают Р/О. Следовательно, для NADH Р/О = 3, для сукцината Р/О - 2. Эти величины отражают теоретический максимум синтеза АТФ, фактически эта величина меньше.
Таким образом, восстановленные формы НАД и ФАД окисляются ферментами дыхательной цепи, благодаря этому происходит присоединение фосфата к АДФ, т.е. фосфорилирование. Поэтому весь процесс целиком получил название окислительное фосфорилирование.
3. Механизм возникновения гипергликемии при сахарном диабете.
Содержание сахара в крови в норме до 5,5 ммоль/л. Гипергликемическим является состояние, при котором концентрация глюкозы в крови более 6 ммоль/л.
Сахарный диабет – заболевание, которое наблюдается при относительном или абсолютном дефиците инсулина. Существует два типа с. Диабета. Первый тип характеризуется гибелью инсулинсинтезирующих клеток (т.е. глюкоза не поступает в клетки из-за отсутствия инсулина), второй – нарушение рецепторных функций клеток тканей (т.е. глюкоза не поступает в клетки из-за отсутствия в них белков-транспортёров).
Из-за того, что глюкоза не потребляется тканями, её содержание в крови увеличивается. Возникает гипергликемия.
Кроме того, при снижении инсулинглюкагонового индекса активируется глюконеогенез из аминокислот, глицерола и лактата, что ведёт к ещё большему повышению содержания глюкозы в крови.
4. Задача. У больного резко повышено кровяное давление, основной обмен, содержание глюкозы, уровень свободных жирных кислот в крови, количество адреналина и норадреналина в плазме крови повышено в 500 раз, имеется глюкозурия. О патологии какого органа можно думать? Напишите химические формулы соединений, вызывающих подобные сдвиги.
Основная патология мозгового вещества надпочечников - феохромоцитома, опухоль, образованная хромаффинными клетками и продуцирующая катехоламины.

10билет
Гипертиреоз: причины
Гипертиреоз может быть врожденным и приобретенным. Врожденный гипертиреоз возникает в результате того, что при беременности женщина перенесла это заболевание или же быть наследственным фактором.
Гипертиреоз возникает в результате ряда заболеваний, связанных с щитовидной железой. Основной причиной является аутоиммунная реакция на фолликулы железы. Такую реакцию провоцируют следующие заболевания: диффузно-токсический зоб или Базедова болезнь, многоузловой зоб и аутоиммунный тиреоидит. Бывали случаи, когда гипотиреоз щитовидной железы диагностировался на фоне аденомы гипофиза. Так как гипофиз производит гормон ТТГ, то при возникновении опухоли, секреция увеличивается, что приводит к увеличению выработки Т3 и Т4.
Гипотиреоз
Причины врожденной формы
При диагнозе врожденный гипотиреоз причины возникновения могут возникнуть как в периоде формирования органов и систем ребенка (в сроке 8−12 недель беременности), так и на протяжении всей беременности, после формирования систем.
Основные причины возникновения врожденного гипотиреоза:
- Нарушение структуры щитовидной железы.
- Нарушение структур гипоталамуса и гипофиза.
- Наличие антител у матери при различных аутоиммунных заболеваниях.
- Прием медикаментов во время беременности (тиреостатики).
- Вирусные, грибковые и бактериальные процессы во время беременности.
- Врожденный дефицит ферментов, которые участвуют в синтезе тиреоидных гормонов.
- Рождение ребенка раньше положенного срока и незрелость щитовидной железы.
Во время формирования нервной системы ребенка дефицит тиреоидных гормонов является основной причиной умственного недоразвития плода, что не определяется при рождении, а выявляется гораздо позже, когда ребенок начинает взаимодействовать с окружающими людьми.
Больная обратилась в клинику с жалобами на сухость во рту, жажду, обильные и частые мочеиспускания, слабость, похудание. Для каких заболеваний характерны эти симптомы? Какие лабораторные исследования необходимо провести для уточнения диагноза?
СД 1 типа. У больной необходимо взять на анализ кровь и мочу.
11билет
1. Изоферменты. Клиническое значение определения активности изоферментов на примере лактатдегидрогеназы и креатинкиназы.
Изоферменты – это множественные формы одного фермента, катализирующие одну и ту же реакцию, но отличающие по физическим и химическим свойствам (сродству к субстрату, максимальной скорости катализируемой реакции, электрофоретической подвижности, разной чувствительности к ингибиторам и активаторам, оптимуму рН и термостабильности). Изоферменты имеют четвертичную структуру, которая образована четным количеством субъединиц (2, 4, 6 и т.д.). Изоформы фермента образуются в результате различных комбинаций субъединиц.
В качестве примера можно рассмотреть лактатдегидрогеназу (ЛДГ), фермент, который катализирует обратимую реакцию:

ЛДГ существует в виде 5 изоформ, каждая из которых состоит из 4-х протомеров (субъединиц) 2 типов М (muscle) и Н (heart). Синтез протомеров М и Н типа кодируется двумя разными генетическими локусами. Изоферменты ЛДГ различаются на уровне четвертичной структуры: ЛДГ1 (НННН), ЛДГ2 (НННМ), ЛДГ3 (ННММ), ЛДГ4 (НМММ), ЛДГ5(ММММ).
Полипептидные цепи Н и М типа имеют одинаковую молекулярную массу, но в составе первых преобладают карбоновые аминокислоты, последних – диаминокислоты, поэтому они несут разный заряд и могут быть разделены методом электрофореза.
Кислородный обмен в тканях влияет на изоферментный состав ЛДГ. Где доминирует аэробный обмен, там преобладают ЛДГ1, ЛДГ2 (миокард, надпочечники), где анаэробный обмен - ЛДГ4, ЛДГ5 (скелетная мускулатура, печень). В процессе индивидуального развития организма в тканях происходит изменение содержания кислорода и изоформ ЛДГ. У зародыша преобладают ЛДГ4, ЛДГ5. После рождения в некоторых тканях происходит увеличение содержания ЛДГ1, ЛДГ2. Эти обстоятельства широко используют в клинической практике, поскольку изучение появления изоферментов ЛДГ в сыворотке крови может представлять интерес для дифференциальной диагностики органических и функциональных поражениях органов и тканей. В норме активность ЛДГ составляет 170-520 ЕД/л. Повышение активности наблюдают при острых поражениях сердца, печени, почек, а также при мегалобластных и гемолитических анемиях. Однако это указывает на повреждение лишь одной из перечисленных тканей.
Креатинкиназа (КК) катализирует реакцию образования креатинфосфата:

Молекула КК - димер, состоящий из субъединиц двух типов: М (от англ, muscle - мышца) и В (от англ, brain - мозг). Из этих субъединиц образуются 3 изофермента - ВВ, MB, MM. Изофермент ВВ находится преимущественно в головном мозге, ММ - в скелетных мышцах и MB - в сердечной мышце.
Активность КК в норме не должна превышать 90 МЕ/л. Определение активности КК в плазме крови имеет диагностическое значение при инфаркте миокарда (происходит повышение уровня МВ-изоформы). Количество изоформы ММ может повышаться при травмах и повреждениях скелетных мышц. Изоформа ВВ не может проникнуть через гематоэнцефалический барьер, поэтому в крови практически не определяется даже при инсультах и диагностического значения не имеет.
Репликация ДНК
Репликацию ДНК осуществляют ДНК-зависимые ДНК-полимеразы.
ДНК-полимеразы
Используют в качестве шаблона одну из цепей двойной спирали ДНК – матрицу.
На матрице, начиная с праймера ферменты синтезируют комплементарную цепь и воспроизводят в итоге исходную двухтяжевую ДНК.
Субстратами ДНК-полимераз являются четыре дНТФ:
дАТФ-, дГТФ-, дТТФ- и дЦТФаты.
Полуконсервативный механизм репликации:
Дочерние клетки 1 поколения получают одну цепь от родителей, а 2-я - является вновь синтезированной.
В клетках прокариот и эукариот имеется несколько различных ДНК-полимераз. Для E. coli известно три ДНК-полимераз: I, II и III.
У эукариот пять типов ДНК-полимераз: альфа, бета, дельта, гамма, эпсилон. В репликации ДНК участвует ДНК-полимераза aльфа, ДНК-полимераза бета катализирует процессы репарации, а ДНК-полимераза гамма — процессы репликации ДНК митохондрий.
Праймер
Для начала синтеза ДНК-полимеразой необходимо наличие связанного с ДНК короткого олигонуклеотида, называемого затравкой или праймером.
Начало репликации
Участок, в котором происходят основные события репликации, называют репликативной вилкой.
Раскручивание ДНК
Для считывания информации цепи ДНК должны быть разведены. При движении репликативной вилки нереплицированная часть ДНК должна раскручиваться.
Раскручивание двойной спирали ДНК и удержание двух цепей на расстоянии осуществляют ДНК-связывающие белки.
Хеликазы расплетают участки ДНК непосредственно перед репликативной вилкой.
Синтез растущей цепи непрерывно идет только вдоль одной из цепей матрицы. Эту цепь называют ведущей.
Синтез по второй цепи, запаздывающей, носит прерывистый характер.
Короткие фрагменты, синтезируемые на запаздывающей цепи, называют фрагментами Оказаки.
Роль процесса:
• Репликация обеспечивает хранение и передачу генетической информации в процессе деления клетки.
• Генетическая информация реализуется через транскрипцию и затем трансляцию.
15 билет
Задача. В больницу доставлен ребенок с явлениями отсталости в физическом и умственном развитии. В моче обнаружен фенилаланин и фенилпировиноградная кислота. Какой фермент неактивен? Напишите химизм и предложите лечение данного случая.
Фенилкетонурия. Неактивен фермент фенилаланин-4-гидроксилаза. Лечение: ограничить поступление в организм фенилаланина с пищей.
17 билет
Лечение
В основе лечения стеатореи лежит лечение заболевания, которое вызвало стеаторею (например, прием ферментных препаратов (способствующих перевариванию пищи) вместе с едой при хроническом панкреатите (воспалении поджелудочной железы длительностью более 6 месяцев), хирургическое удаление опухоли кишечника и др.)
- диета должна быть подобранна индивидуально, в зависимости от заболевания, вызвавшего стеат




 желчных пигментов. Желтухи.
желчных пигментов. Желтухи. 




















