Атомность спиртов определяется количеством гидроксильных групп. Двухатомные спирты содержат две гидроксильные группы и носят общее название диолы или гликоли. Трехатомные спирты называют триолами или глицеринами. Простейшие и наиболее важные представители диолов и триолов – этиленгликоль и глицерин. Этиленгликоль (этандиол-1,2).. Химические свойства этиленгликоля аналогичны свойствам одноатомных спиртов. Однако есть ряд специфических свойств, обусловленных присутствием двух гидроксильных групп.Этиленгликоль является более сильной кислотой, чем одноатомные спирты (рКа=15,1) и образует в водных растворах комплексные алкоголяты с ионами тяжелых металлов.
.При дегидратации этиленгликоля в зависимости от условий реакции образуются разные продукты. При нагревании в присутствии серной кислоты происходит межмолекулярная дегидратация с образованием циклического простого эфира – диоксана. Нагревание с хлоридом цинка дает продукт внутримолекулярной дегидратации – ацетальдегид.Этиленгликоль легко окисляется. В зависимости от природы окислителя могут образоваться гликолевый альдегид, глиоксаль, глиоксиловая кислота, щавелевая кислота.Этиленгликоль используется для приготовления антифризов; для получения растворителей (простые эфиры этиленгликоля, диоксан) и полимеров (полиэфиров). Глицерин получают гидролизом жиров, но в основном синтетическим путем из пропилена.Глицерин дает все реакции, известные для спиртов. Наличие трех гидроксильных групп обуславливает некоторые специфические свойства.Глицерин является более сильной кислотой, чем одноатомные спирты (рКа=14).При дегидратации глицерина образуется ненасыщенный альдегид акролеин.Мягкое окисление глицерина дает смесь глицеринового альдегида и дигидроксиацетона.Важное значение имеют сложные эфиры глицерина. При действии на глицерин азотной кислоты в присутствии серной кислоты образуется тринитрат глицерина (нитроглицерин).Нитроглицерин используется в производстве взрывчатых веществ. В малых концентрациях нитроглицерин применяется как сосудорасширяющее средство.При действии на глицерин фосфорной кислоты образуется смесь a - и b -глицерофосфатов.Глицерофосфаты являются структурными компонентами фосфолипидов.Сложные эфиры глицерина и высших жирных кислот – основная составная часть природных жиров и масел Примерами многоатомных спиртов, содержащих четыре, пять и шесть гидроксильных групп, могут служить соответственно эритриты, пентиты и гекситы.
45. Простейшие представители: фенол, крезолы, пирокатехин, резорцин, гидрохинон, флороглюцин, пирогаллол. Соединения, содержащие более одной гидроксильной группы в ароматическом ядре относятся к многоатомным фенолам.Двухатомные фенолы. Простейшими двухатомными фенолами являются:Пирокатехин Резорцин Гидрохинон. Все три изомера являются кристаллическими веществами; легче растворимы в воде, чем фенолы, по свойствам похожи на одноатомные фенолы. Пирокатехин и гидрохинон - сильные восстановители, легко окисляются до бензохинонов. Резорцин более устойчив к окислению. В лабораторных условиях их получают сплавлением соответствующих сульфокислот со щелочами.Пирокатехин, гидрохинон применяют в фотографии в качестве проявителя. Пирокатехин является селективным собирателем ниобиевых минералов и улучшает действие обычных собирателей при pH=5-7, а также применяется в аналитической химии в колориметрических определениях ниобия, тантала, ванадия, вольфрама. Трехатомные фенолы. Важнейшими представителями трехатомных фенолов являются:Пирогаллол Оксигидрохинон Флороглюцин.Все они твердые вещества, растворимые в воде. Это сильные восстановители. Применяют их в производстве красителей, в фотографии.Пирогаллол используют в аналитической химии для обнаружения молибдена, ниобия, тантала, висмута, германия, серебра, ванадия и железа. Применение фенолов. Большое количество фенолов идет на изготовление красителей, лекарств, взрывчатых веществ, пластических масс, синтетических волокон (капрон, нейлон), гербицидов, флотореагентов.Фенолы, крезолы, ксиленолы входят в состав некоторых смол, креозотовых масел, пенообразователей. Так, основной частью древесно-смоляного тяжелого флотационного масла, полученного при переработке древесины, являются фенолы.
46. Электронное строение фенола. Кислотность фенолов. Образование простых и сложных эфиров фенолов. Реакции электрофильного замещения в ряду фенолов (галогенирование, сульфирование, нитрование, алкилирование). Пикриновая кислота. Электронное строение фенола. гидроксильная группа -OH является заместителем I рода, то есть она способствует повышению электронной плотности в бензольном кольце (особенно в орто- и пара -положениях). Это обусловлено тем, что одна из неподелённых пар электронов атома кислорода OH-группы вступает в сопряжение с π-системой бензольного кольца. Смещение неподелённой пары электронов атома кислорода в сторону бензольного кольца приводит к увеличению полярности связи O-H. Таким образом, имеет место взаимное влияние атомов и атомных групп в молекуле фенола. Это взаимное влияние отражается в свойствах фенола.Фенол является слабой кислотой. В этом состоит главное отличие фенолов от спиртов, которые являются неэлектролитами. Галогенирование: В отличие от бензола галогенирование фенола не требует катализа и протекает при действии молекулярного галогена. При бромировании фенола в водном растворе остановить реакцию на стадии образования монобромпроизводного невозможно..Для того чтобы осуществить моногалогенирование фенола, необходимо проводить реакцию в условиях, где диссоциация фенола полностью подавлена. Например, п -бромфенол синтезируют при действии на фенол бромом в среде бромоводородной кислоты, сероугрерода или реакцией фенола с диоксандибромидом в хлороформе. Нитрование. Нитрование фенола протекает при действии разбавленной азотной кислоты и приводит к двум изомерам – орто - и пара -нитрофенолам. Дальнейшее взаимодействие с концентрированной азотной кислотой дает сначала динитрофенолы и затем 2,4,6-тринитрофенол (пикриновую кислоту). Этот процесс сопровождается значительным смолообразованием из-за окислительного действия азотной кислоты.Поэтому для синтеза пикриновой кислоты преимущественно применяют нитрование 4-гидроксибензол-1,3-дисульфокислоты, основанное на ипсо-замещении сульфогрупп на нитрогруппы.

Сульфирование
Сульфирование фенола осуществляют путем нагревания с концентрированной серной кислотой. Температура проведения реакции решающим образом определяет строение образующихся оксибензолсульфокислот. орто -Изомер, скорость образования которого выше, чем пара -изомера, является доминирующим продуктом, если температура проведения реакции не превышает 100 °С. Его называют кинетическим продуктом. Напротив, при более высоких температурах основным продуктом является пара -изомер, скорость образования которого ниже, но он обладает высокой термодинамической устойчивостью Реакция электрофильного ароматического сульфирования обратима и при нагревании орто -оксибензолсульфокислоты, с серной кислотой выше 100 °С получают пара -изомер – продукт термодинамического контроля реакции. Алкилирование. В отличие от алкилирования фенола по гидроксигруппе, которое идет в щелочной среде, введение алкильных заместителей в ароматическое кольцо фенола протекает при действии галогеналканов, спиртов или алкенов в присутствии катализаторов – минеральных кислот или кислот Льюиса (реакция Фриделя-Крафтса). Пикриновая кислота. Наличие в ядре трех нитрогрупп резко увеличивает кислотность фенольной группы. Пикриновая кислота является, в отличие от фенола, уже довольно сильной кислотой. Наличие трех нитрогрупп делает пикриновую кислоту взрывчатой, она используется для приготовления мелинита. Для получения мононитрофенолов необходимо использовать разбавленную азотную кислоту и проводить реакцию при низких температурах:Получается смесь о- и п-нитрофенолов с преобладанием о-изомера. Эта смесь легко разделяется благодаря тому, что только о-изомер обладает летучестью с водяным паром. Большая летучесть о-нитрофенола объясняется образованием внутримолекулярной водородной связи, в то время как в случае.п-нитрофенола возникает межмолекулярная водородная связь.
47. Карбоксилирование фенолятов щелочных металлов. Салициловая кислота. Фенолокарбоновые кислоты получают при взаимодействии фенолятов щелочных металлов с углерода (IV) оксидом.Салициловая (о-гидроксибензойная) кислота является одной из важнейших фенолокарбоновых кислот. Она используется для получения лекарственных препаратов (натрия салицилата, ацетилсалициловой кислоты, фенилсалицилата, метилсалицилата), в синтезе красителей, в производстве душистых веществ (сложных эфиров), для получения кумарина и др.Стадии производства салициловой кислоты:1) получение безводного натрия фенолята:

2) карбоксилирование натрия фенолята углерода (IV) оксидом:

Фенол как побочный продукт отгоняют; 3) разложение сырого натрия салицилата:

Труднорастворимая салициловая кислота выпадает в осадок;
4) отделение и очистка салициловой кислоты.Получаемая техническая салициловая кислота содержит до 99 \% чистого продукта. Салициловая кислота, предназначенная для получения лекарственных веществ, должна быть очищена возгонкой.
48. Окисление фенолов. Повышенная электронная плотность в ядре фенола делает его чувствительным к воздействию окислителей.В зависимости от природы окислителя и условий проведения реакции образуются различные продукты окисления фенола.1) При окислении фенола пероксидом водорода в прис
утствии железного катализатора получается орто-бензохинон через промежуточное образование пирокатехина:
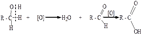
2) Сильные окислители, такие как хромовая смесь (K2Cr2O7 + H2SO4), броматы (KBrO3, H2SO4) окисляют фенол до пара-бензохинона через промежуточное образование гидрохинона:

3) При более энергичном действии окислителей происходит разрушение бензольного ядра.Благодаря склонности к окислению фенолы могут окрашиваться при хранении на воздухе.
49. Хиноны и их биологическая роль. Хинонами называются шестичленные циклические дикетоны с двумя двойными связями.Наибольшее практическое значение из них имеет парахинон, получаемый окислением гидрохинона или анилина. Парахинон – исходный продукт при синтезе гидрохинона. Характерное для хинона расположение двойных связей обусловливает окраску ряда соединений.Нафтохиноны – производные нафталина, содержащие хиноидное ядро. Наибольшее значение имеет 1,4-нафтохинон, который можно получить при окислении нафталина.По ряду своих свойств 1,4-нафтохинон сходен с п-бензохиноном. Он кристаллизуется в виде желтых игл, летуч, обладает острым раздражающим запахом.Ядро 1,4-нафтохинона лежит в основе витамина К, или антигеморрагического витамина (препятствующего появлению кровоизлияний). Витамин К представляет собой 2-метил-3-фитил-1,4-нафтохинон. Витамин К содержится в зеленых травах, листьях, овощах. Предст. собой желтое масло, нераствор. в воде; перегоняется в высоком вакууме. Некоторые производные хинонов играют важную роль в промежуточных процессах биологического окисления.Антрахиноны – производные антрацена, содержащие хиноидное ядро. Антрахинон можно легко получить при окислении антрацена азотной кислотой или хромовой смесью. При этом в молекуле образуются две кето-группы и среднее кольцо приобретает строение хинона. Антрахинон представляет собой кристаллическое вещество желтого цвета, в отличие от обычных хинонов довольно стойкое к ряду химических воздействий, в частности к окислению. Антрагидрохинон является промежуточным продуктом при восстановлении антрахинона в антрацен. Антрагидрохинон в свободном виде представляет собой кристаллы коричневого цвета. Имея два фенольных гидроксила, антрагидрохинон растворяется в щелочах; образующееся вещество типа фенолята обладает ярко-красным цветом. Антрахинон способен бромироваться, нитроваться и сульфироваться.Ализарин представляет собой 1,2-диоксиантрахинон.Эмодины. В медицинской практике в качестве слабительных средств часто пользуются препаратами (настойками, отварами и т. д.) из алоэ, ревеня, крушины, листьев сенны и т. д. Действующими веществами этих растений, как оказалось, являются производные антрахинона, а именно – замещенные ди– и триокси-антрахинонов, содержащиеся в растениях частью в свободном виде, частью в виде эфиров и гликози-дов. Эти производные ди– и триоксиантрахинонов часто объединяют в группу эмодинов. Примером эмодинов может служить франгулоэмодин, являющийся 3-метил-1,6,8-триоксиантрахиноном. Франгулоэмо-дин содержится в крушине
50. Представление о фенольных антиоксидантах. Фенольные соединения в природе. Витамин Е. Флавоноиды. Антиоксидантами (АО) или антиокислителями принято называть соединения различной химической природы, способные тормозить или устранять свободно-радикальное окисление органических веществ молекулярным кислородом. В течение многих лет антиоксиданты широко используются для продления срока службы и улучшения эксплуатационных качеств полимерных и горюче-смазочных материалов, предотвращения окислительной порчи пищевых продуктов, жирорастворимых витаминов, кормов и косметических средств. Применение АО в этих областях дает огромный экономический эффект и позволяет сберегать значительные сырьевые ресурсы. Среди синтетических АО широкое распространение получили алкилированные фенолы, что обусловлено как сравнительной простотой их производства, так и комплексом ценных свойств: высокой эффективностью, малой токсичностью, универсальностью действия и возможностью изменять их свойства в широких пределах варьированием заместителей. Под фенольными антиоксидантами (ФАО) понимают любые соединения вида Ar(OH)n, в которых одна или несколько гидроксильных групп соединены с ароматическим ядром, причем молекула АО может содержать несколько фрагментов Ar(OH)n. Фенольные соединения способны оказывать влияние на многие физиологические процессы, проходящие в организме человека. Например, в составе растительных препаратов эти вещества (такие как кумарин, свойства которого еще мало изучены, рутин, флавоноиды) стимулируют деятельность коры надпочечников, благодаря чему надпочечники начинают активнее выделять гормоны группы глюкокортикоидов (вид гормонов выделяемых надпочечниками). Они обладают самыми разнообразными биологическими свойствами. Например, фенольные соединения листьев толокнянки, груши, брусники проявляют себя как антисептики.
Фенолокарбоновые кислоты- производные ароматических углеводородов, в молекуле которых атомы Н бензольного кольца замещаются на карбо(-СООН) или гидроксильные группы(-ОН) Фенольные соединения давно нашли свое применение в медицине, их применяют при лечении неврозов и коронарной недостаточности. Фенольные соединения обладают мочегонным, седативным, желчегонным и кровоостанавливающим действием. Флаваноиды, биофлавоноиды относятся к фенолам, это желто-красные пигменты растений. Их много и в пищевых, и в лекарственных растениях. Биофлавоноиды укрепляют капилляры, выступают как онкопротекторы, участвуют в выведении из организма солей тяжелых металлов, радионуклидов. В группу биофлавоноидов входят особые вещества, также проявляющие Р-витаминную активность и прочие свойства биофлавоноидов, которые называются антоцианы. По химической структуре антоцианы - это флавоновые гликозиды.Дубильные вещества- это полимерные фенольные соединения. В медицине они используются как вяжущие, противовоспалительные желудочно-кишечные средства.Самым известным дубильным веществом является танин.Его не стоит принимать внутрь: это вызовет расстройство пищеварения.Катехины (их также относят к биофлавоноидам) являются производными флавонолов и антоцианов. Кумарины - это ароматические вещества с запахом свежего сена. Кумарины - антикоагулянты, то есть препятствуют быстрому сворачиванию крови, как, например, производное кумарина дикумарол. Он является антивитамином К и применяется для профилактики и лечения тромбозов и тромбофлебитов.
51. Простые эфиры. Номенклатура, классификация. Расщепление кислотами. Простые эфиры - органические вещества, в которых молекулы содержат углеводородные радикалы, соединенные атомом кислорода. Записать это можно следующим образом: R–O–R’, где R и R' являются одинаковыми или различными радикалами. Простые эфиры рассматриваются в качестве производных спиртов. Эти соединения имеют составные названия. При этом используется название радикалов (по возрастанию молекулярной массы) и, собственно, слово "эфир" (диметиловый эфир СН3ОСН3, метилэтиловый эфир С2Н5ОСН3 и так далее)
Номенклатура простых эфиров Согласно тривиальной номенклатуре простые эфиры называют по радикалам, связанным с атомом кислорода, добавляя слово "эфир".

По номенклатуре ИЮПАК эфиры рассматривают как алкоксиалканы. Корень слова определяет самая длинная алкильная группа.

Простые эфиры относятся к числу малореакционноспособных веществ и стабильны по отношению ко многим реагентам, но они чувствительны по отношению к кислороду и легко образуют взрывчатые гидроперекиси, которые являются причиной взрыва при неосторожном обращении.
1. Кислотное расщепление простых эфиров
Простые эфиры расщепляются при нагревании до 120-150о с концентр. водной 48% HBr или HI. В столь же жестких условиях расщепляются простые эфиры фенолов.

Однако эфиры, содержащие третичную алкильную группу, расщепляются очень легко.

Кислотное расщепление простых эфиров следует рассматривать как реакцию нуклеофильного замещения у насыщенного атома углерода. В зависимости от природы алкильных групп, связанных с кислородом, реализуется либо SN1, либо SN2- механизмы. Если эфир содержит первичные или вторичные алкильные группы, реализуется SN2- механизм, в котором бромид- или иодид-ион атакует протонированную форму эфира по менее замещенному атому углерода. В этом случае расщепление отличается высокой региоселективностью и, как правило, образуется только один их двух возможных спиртов (вторичный) и первичный алкилгалогенид.

Хлорид- и фторид-ионы в воде сильно сольватированы за счет водородных связей и обладают недостаточной нуклеофильностью для кислотного расщепления простых эфиров по SN2- механизму.
Простые эфиры с третичной алкильной, бензильной или аллильной группами реагируют по SN1- механизму с образованием карбокатиона в качестве интермедиата. Эти реакции идут в мягких условиях, а в качестве кислотного агента можно использовать трифторуксусную кислоту.

В препаративном отношении гораздо более удобными реагентами для расщепления эфиров являются BCl3 или BBr3. В этих случаях расщепление проходит уже при -20оС. Это особенно необходимо при наличии других функциональных групп или тогда, когда возможна изомеризация углеродного скелета.

Образование гидропероксидов, их обнаружение и разложение.
Гидропероксиды — это первые молекулярные продукты окисления углеводородов. Звено цепи при их образовании имеет вид:
 взаимодействие пероксидного радикала с углеводородом — определяет строение образующегося гидропероксида и последующих продуктов окисления. При этом соблюдается обычный для радикальных реакций порядок изменения реакционной способности атомов водорода, определяемый относительной стабильностью промежуточного радикала
взаимодействие пероксидного радикала с углеводородом — определяет строение образующегося гидропероксида и последующих продуктов окисления. При этом соблюдается обычный для радикальных реакций порядок изменения реакционной способности атомов водорода, определяемый относительной стабильностью промежуточного радикала  . Вследствие этого преимущественным местом атаки молекулы при окислении алканов становится -положение боковой цепи по отношению к ароматическому ядру, а для олефинов — алкильное положение. Кроме того, для углеводородов всех классов справедлива известная последовательность в изменении способности к замещению атомов водорода, находящихся при разных углеродных атомах (третичный вторичный первичный).
. Вследствие этого преимущественным местом атаки молекулы при окислении алканов становится -положение боковой цепи по отношению к ароматическому ядру, а для олефинов — алкильное положение. Кроме того, для углеводородов всех классов справедлива известная последовательность в изменении способности к замещению атомов водорода, находящихся при разных углеродных атомах (третичный вторичный первичный).
Гидропероксиды относятся к числу довольно нестабильных соединений, превращающихся при окислении в другие продукты. Гидропероксиды при разложении под действием повышенной температуры или катализаторов окисления дают спирты и карбонильные соединения. Это разложение может иметь молекулярный механизм, однако в развившемся процессе окисления продукты образуются главным образом цепным путем. При получении спиртов звено цепи таково:


Кетоны образуются из вторичных гидропероксидов через стадию радикал-гидропероксидов:

Третичные гидропероксиды при цепном превращении дают кроме спирта с тем же числом углеродных атомов также спирт и кетон с меньшим числом атомов углерода за счет деструкции углерод-углеродной связи:









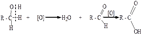








 взаимодействие пероксидного радикала с углеводородом — определяет строение образующегося гидропероксида и последующих продуктов окисления. При этом соблюдается обычный для радикальных реакций порядок изменения реакционной способности атомов водорода, определяемый относительной стабильностью промежуточного радикала
взаимодействие пероксидного радикала с углеводородом — определяет строение образующегося гидропероксида и последующих продуктов окисления. При этом соблюдается обычный для радикальных реакций порядок изменения реакционной способности атомов водорода, определяемый относительной стабильностью промежуточного радикала  . Вследствие этого преимущественным местом атаки молекулы при окислении алканов становится -положение боковой цепи по отношению к ароматическому ядру, а для олефинов — алкильное положение. Кроме того, для углеводородов всех классов справедлива известная последовательность в изменении способности к замещению атомов водорода, находящихся при разных углеродных атомах (третичный вторичный первичный).
. Вследствие этого преимущественным местом атаки молекулы при окислении алканов становится -положение боковой цепи по отношению к ароматическому ядру, а для олефинов — алкильное положение. Кроме того, для углеводородов всех классов справедлива известная последовательность в изменении способности к замещению атомов водорода, находящихся при разных углеродных атомах (третичный вторичный первичный).







