Удерживаемый объем можно рассчитать, зная коэффициент распределения Dc и характеристики колонки.
Количество вещества после элюирования = 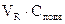
До окончательного элюирования количество вещества = 

 - объем подвижной фазы, равный рабочему объему колонки V0. Его определяют измеряя удерживаемый объем несорбируемого вещества;
- объем подвижной фазы, равный рабочему объему колонки V0. Его определяют измеряя удерживаемый объем несорбируемого вещества; 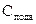 - концентрация вещества в подвижной фазе;
- концентрация вещества в подвижной фазе;  - объем неподвижной фазы;
- объем неподвижной фазы; 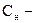 концентрация вещества в неподвижной фазе.
концентрация вещества в неподвижной фазе.
Поскольку элюируется все вещество, присутствовавшее в колонке:
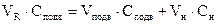 (1)
(1)
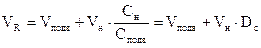 (2)
(2)
Часто используют приведенный удерживаемый объем 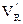 , скорректированный с учетом рабочего объема колонки
, скорректированный с учетом рабочего объема колонки  :
:
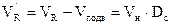 (3)
(3)
Уравнение 3 представляет собой основное уравнение хроматографии. Оно показывает, что чем больше коэффициент распределения Dc, тем больше VR и чем больше объем неподвижной фазы Vн, тем больше VR. В свою очередь Vн зависит от длины и диаметра колонки.
Эффективность разделения пропорциональна длине колонки, но при увеличении ее длины происходит размывание зоны каждого компонента и, следовательно, расширение пиков (ширина пика пропорциональна времени нахождения вещества в колонке), поэтому длину колонки необходимо ограничивать.
Газовая хроматография
Колоночная газовая хроматография является методом разделения летучих веществ: газов (при нормальной температуре) или паров (при повышенной температуре). В качестве неподвижной фазы в газовой хроматографии используются твердые материалы (насадочные или набивные колонки), твердые материалы, покрытые слоем жидкости, или же капилляры с нанесенным на внутреннюю поверхность слоем жидкости (капиллярные колонки). В качестве подвижной фазы используют газ-носитель, переносящий разделяемые вещества через колонку. Разделение анализируемой смеси осуществляется за счет различного времени удерживания компонентов пробы в неподвижной фазе.
Основные группы органических веществ, которые могут быть определены методом газовой хроматографии, включают газы, летучие жидкие соединения, твердые частицы, жидкие аэрозоли и главным требованием для веществ, разделяемых газовой хроматографией, является их достаточная устойчивость при температурах, которые необходимы для поддержания биопробы в газообразном состоянии.
Между жидкостной и газовой хроматографией не существует принципиальной разницы. Газовая хроматография отличается лишь свойствами подвижной фазы: высокой скоростью диффузии газа-носителя и его способностью сжиматься. Достоинствами газовой хроматографии являются:
· возможность идентификации и количественного определения индивидуальных компонентов сложных смесей;
· возможность анализа широкого круга объектов — от легких газов до органических соединений и некоторых металлов;
· высокая четкость разделения и быстрота процесса, обусловленная низкой вязкостью подвижной фазы;
· возможность исследования микропроб и автоматизация записи
получаемых результатов, обусловленная наличием чувствительных и
малоинерционных детекторов;
· возможность выделения чистых веществ в промышленных масштабах;
· пригодность для исследования малых объемов жидких биопроб (0,01...50 мкл).
Максимальная разделяющая способность колонки в ГХ зависит от:
· количества НФ, качества упаковки, толщины слоя;
· размера (диапазона размеров) частиц материала-носителя;
· размеров колонки;
· вязкости газа-носителя (следовательно, и температуры в колонке).
В газоадсорбционной в качестве неподвижной фазы используется адсорбент, а в основе разделения лежит механизм адсорбции; в газожидкостной неподвижной фазой является жидкость, нанесенная на инертный материал-носитель, а в основе разделения лежит распределительный механизм. Растворимость анализируемых веществ в неподвижной фазе определяется зависимостью давления паров растворенного вещества от его концентрации в жидкой фазе.
Вид хроматограммы, полученной в изотермических условиях, представлен на рис.7. Время удерживания конкретного компонента в колонке зависит от вероятности попадания молекул вещества в подвижной фазе. При этом компоненты с высоким давлением паров и соответственно низкой растворимостью в неподвижной фазе удерживаются слабее и, наоборот, вещества с низким давлением пара и высокой растворимостью элюируются позже.
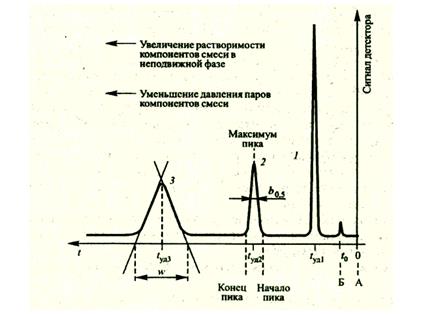
Рис.7. Хроматограмма, полученная в изотермических условиях.
В газовом хроматографе (рис. 8) газ-носитель из баллона 1 через регуляторы расхода и давления непрерывно с постоянной или переменной скоростью подается в хроматографическую трубку-колонку 3, заполненную сорбентом и помещённую в термостат 4, позволяющий поддерживать заданную температуру [1]. Ввод газообразной или жидкой пробы осуществляется дозаторами 2, регулирующими объём пробы с помощью электромагнитных клапанов (ЭМК).
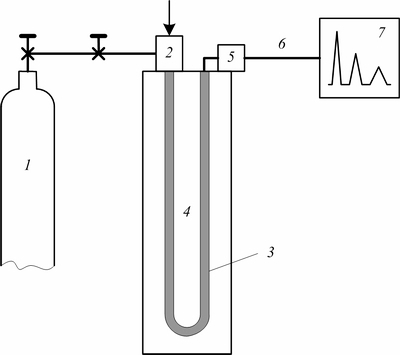
Рис. 8. Структурная схема газового хроматографа
1 – баллон с газом-носителем; 2 – дозатор пробы; 3 – хроматографическая трубка-колонка; 4 – термостат; 5 – детектор; 6 – электрический сигнал; 7 – хроматограмма
В газовой хроматографии применяют три типа колонок:
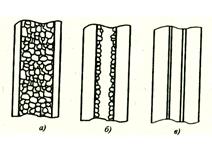
Рис.9. Типы колонок для газовой хроматографии: а – насадочная колонка; б – тонкослойная капиллярная колонка (SCOT - колонка); в – классическая капиллярная колонка.
1. Насадочные колонки. Такие колонки изготовливаются из стеклянных или металлических трубок (нержавеющая сталь) U-образной или спиралевидной формы. Они характеризуются большой поверхностью и высокой разделяющей способностью, однако обладают большим сопротивлением, что ведет к неравномерности потока газа-носителя. Хотя теоретически разделяющая способность растет с увеличением длины колонки, на практике преимущество длинных колонок сводится на нет из-за увеличения сопротивления. Оптимальной длиной насадочной колонки является 0,5...10 м при внутреннем диаметре 1...5 мм.
2. Тонкослойные капиллярные колонки. Этот тип колонок занимает промежуточное место между насадочными и классическими капиллярными колонками. Их внутренняя поверхность покрыта тонким слоем мелкодисперсного сорбента, пропитанного жидкой фазой. По разделяющей способности они превосходят насадочные, так как обладают меньшим сопротивлением.
3. Капиллярные колонки из стекла или нержавеющей стали. При равной длине с насадочными колонками такие колонки обладают существенно меньшим сопротивлением, имеют длину до 200 м при внутреннем диаметре 0,3...0,5 мм. Эффективность капиллярных колонок в 100 раз выше, чем насадочных. Преимуществом их является возможность изготовления из кварцевого стекла, что придает им свойство гибкости — их можно даже завязывать в узел или придавать любую форму. Однако такие колонки предъявляют жесткие требования к устройствам ввода пробы и к выбору детектора.
Основные характеристики колонок для газовой хроматографии представлены в табл.2.
Таблица 2. Характеристики колонок для газовой хроматографии.
| Параметр
| Тип колонки
|
насадочные
| Капиллярные
|
| Длина, м
| 1...6
| 10... 100
|
| Внутренний диаметр, мм
| 2...4
| 0,25...0,3555
|
| Емкость
| 10мкг/пик
| 50 нг/пик
|
| Толщина пленки НФ, мкл
| 1...10
| 0,05...0,5
|
| Скорость газа-носителя, мл/мин
| 10...60
| 0,5…10
|
| Перепад давления по колонке, атм
| 0,6...2,4
| 0,18...2,4
|
Устройства ввода пробы. Способ ввода биопробы зависит от ее вида (жидкая или газообразная) и типа колонки. При разделении жидкостей в насадочных колонках биопробу вводят шприцем, прокалывая иглой мембрану (пробку из силиконовой резины), при этом биопроба потоком газа-носителя уносится в колонку. При введении газовых и невязких жидких биопроб область ввода иглы нагревают, чтобы она сразу испарилась. Твердую биопробу предварительно переводят в раствор.
При работе на капиллярных колонках биопробу вводят при помощи делителя потока, в котором она попадает сначала в канал испарения, после чего разбавляется газом-носителем. Большая часть газовой смеси уходит на сброс, меньшая - в колонку. При автоматизированном анализе газовых смесей биопробу вводят при помощи дозирующей петли.
Материалы-носители. Газоадсорбционную хроматографию применяют с целью разделения газов или низкокипящих веществ и обнаружения газообразных примесей в воздухе. В качестве адсорбентов применяют:
· активированные угли или графитированные сажи;
· пористые синтетические полимеры;
· пористые неорганические материалы (молекулярные сита).
Нанесенная жидкая фаза в колонках для газоадсорбционной хроматографии не применяется.
В газожидкостной хроматографии сорбенты выполняют функцию носителей жидкой неподвижной фазы и не оказывают влияния на процесс разделения.
Технологическая процедура подготовки пробы может осуществляться различными способами. Для анализа паров над жидкой или твердой фазой (например, при определении спирта в пробе крови) разработана специальная методика Неаd-Sрасе-Аnаlуsе (из объема над жидкостью). Необходимое количество пробы газа отбирают с помощью пробоотборника непосредственно из емкости для хранения. По другой методике биопробу потоком воздуха направляют в охлаждаемую ловушку и замораживают. Третий вариант заключается в том, что газ при пониженной температуре адсорбируют на короткой колонке, затем при повышении температуры десорбируют и направляют в рабочую колонку. При анализе влажных биопроб не допускается конденсация воды в колонке, для этого биопробу осушают. Твердые частицы в аэрозолях отделяют с помощью бумажных салфеток или фильтрующих патронов. При анализе жидких биопроб, содержащих компоненты с различной температурой кипения, исключают возможность конденсации компонентов в дозирующем шприце, для этого шприц нагревают, не допуская разложения биопробы.
Основные стадии технологической процедуры анализав газовой хроматографии несколько отличаются от рассмотренных ранее.
1. Подготовка колонки. Колонку промывают специальным раствором, а затем высушивают в потоке воздуха, очищенного от пыли и капель масла.



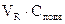


 - объем подвижной фазы, равный рабочему объему колонки V0. Его определяют измеряя удерживаемый объем несорбируемого вещества;
- объем подвижной фазы, равный рабочему объему колонки V0. Его определяют измеряя удерживаемый объем несорбируемого вещества; 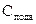 - концентрация вещества в подвижной фазе;
- концентрация вещества в подвижной фазе;  - объем неподвижной фазы;
- объем неподвижной фазы; 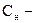 концентрация вещества в неподвижной фазе.
концентрация вещества в неподвижной фазе.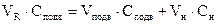 (1)
(1)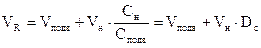 (2)
(2)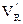 , скорректированный с учетом рабочего объема колонки
, скорректированный с учетом рабочего объема колонки 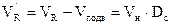 (3)
(3)




