

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

История развития пистолетов-пулеметов: Предпосылкой для возникновения пистолетов-пулеметов послужила давняя тенденция тяготения винтовок...

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

История развития пистолетов-пулеметов: Предпосылкой для возникновения пистолетов-пулеметов послужила давняя тенденция тяготения винтовок...
Топ:
Техника безопасности при работе на пароконвектомате: К обслуживанию пароконвектомата допускаются лица, прошедшие технический минимум по эксплуатации оборудования...
Процедура выполнения команд. Рабочий цикл процессора: Функционирование процессора в основном состоит из повторяющихся рабочих циклов, каждый из которых соответствует...
Интересное:
Искусственное повышение поверхности территории: Варианты искусственного повышения поверхности территории необходимо выбирать на основе анализа следующих характеристик защищаемой территории...
Влияние предпринимательской среды на эффективное функционирование предприятия: Предпринимательская среда – это совокупность внешних и внутренних факторов, оказывающих влияние на функционирование фирмы...
Средства для ингаляционного наркоза: Наркоз наступает в результате вдыхания (ингаляции) средств, которое осуществляют или с помощью маски...
Дисциплины:
|
из
5.00
|
Заказать работу |
Кластер П(c041, 7 шт)
1. [Уд3] (ВОМ) Момент инерции однородного тела зависит от:
1) момента приложенных к телу сил при заданной оси вращения
2) выбора оси вращения
3) формы тела
4) массы тела
5) углового ускорения
:2,3,4
2. [Уд1] (ВО1)  Из жести вырезали три одинаковые детали в виде эллипса. Две детали разрезали на четыре одинаковые части. Затем все части отодвинули друг от друга на одинаковое расстояние и расставили симметрично относительно оси ОО. Для моментов инерции относительно оси ОО справедливо соотношение
Из жести вырезали три одинаковые детали в виде эллипса. Две детали разрезали на четыре одинаковые части. Затем все части отодвинули друг от друга на одинаковое расстояние и расставили симметрично относительно оси ОО. Для моментов инерции относительно оси ОО справедливо соотношение
1) I1< I2 < I3
2) I1= I2 = I3
3) I1< I2 = I3
4)I1> I2 > I3
:1
 3. [Уд1] (ВО1) Тонкостенная трубка и кольцо имеют одинаковые массы и радиусы (рис.). Для их моментов инерции справедливо соотношение
3. [Уд1] (ВО1) Тонкостенная трубка и кольцо имеют одинаковые массы и радиусы (рис.). Для их моментов инерции справедливо соотношение
1) Iк = IТ
2) Iк > IТ
3) Iк < IТ
:1
4. [Уд1] (ВО1) Четыре шарика расположены вдоль прямой а. Расстояния между соседними шариками одинаковы. Массы шариков слева направо: 1 г, 2 г, 3 г, 4 г. Если поменять местами шарики 2 и 3, то то момент инерции этой системы относительно оси О, перпендикулярной прямой а и проходящей через середину системы
1) увеличится
2) не изменится
3) уменьшится
:2
5. [Уд1] (ВО1) Момент импульса  твердого тела относительно оси вращения рассчитывается по формуле
твердого тела относительно оси вращения рассчитывается по формуле
1) 
2) 
3) 
4) 
:1
6. [Уд1 (ВО1)Направление момента силы, вызывающего вращение тела, совпадает с направлением вектора
1) силы
2) изменения момента импульса
3) момента импульса тела в начальный момент времени
4) момента импульса тела в конечный момент времени
:2
7. [Уд1] (ВО1)Направление изменения момента импульса вращающегося тела всегда совпадает с направлением вектора
1) момента силы
2) угловой скорости
3) момента импульса тела в начальный момент времени
4) момента импульса тела в конечный момент времени
:1
Синглы П(s041, 15 шт)
 1. [Уд1] (О) На рисунке приведена зависимость модуля моментов приложенных к телу сил от модуля углового ускорения тел. Наибольший момент инерции имеет тело под номером …
1. [Уд1] (О) На рисунке приведена зависимость модуля моментов приложенных к телу сил от модуля углового ускорения тел. Наибольший момент инерции имеет тело под номером …
:1
2. [Уд1] (ВО1) Векторная форма основного закона динамики вращательного движения абсолютно твердого тела в импульсном виде –
1) 
2) 
3) 
4) 
:2
2. [Уд1] (ВО1) Формула, отражающая связь момента сил, действующих на тело, с моментом импульса этого тела –
1) 
2) 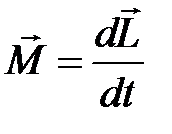
3) 
4) 
:2
3. [Уд1] (ВО1) На рисунке приведен график зависимости модуля результирующего момента сил, действующих на вращающееся твердое тело, от времени. Тело вращалось равномерно на интервале времени
1) от 0 до t1
2) от t1 до t2
 3) от t2 до t3
3) от t2 до t3
4) от t3 до t4
:4
 4. [Уд1] (ВО1) На рисунке приведен график зависимости модуля результирующего момента сил, действующих на вращающееся твердое тело, от времени. Тело вращалось с постоянным угловым ускорением на интервале времени
4. [Уд1] (ВО1) На рисунке приведен график зависимости модуля результирующего момента сил, действующих на вращающееся твердое тело, от времени. Тело вращалось с постоянным угловым ускорением на интервале времени
1) от 0 до t1
2) от t1 до t2
3) от t2 до t3
4) от t3 до t4
:2
 5. [Уд3] (ВО) На рисунках стрелками показаны направления вращения дисков и указано, как изменяется угловая скорость со временем. Вращающий момент сил, направленный вниз, приложен к дискам, приведенным под номерами: …
5. [Уд3] (ВО) На рисунках стрелками показаны направления вращения дисков и указано, как изменяется угловая скорость со временем. Вращающий момент сил, направленный вниз, приложен к дискам, приведенным под номерами: …
1) 1 и 2
2) 1 и 3
3) 1 и 4
4) 2 и 3
5) 2 и 4
6) 3 и 4
:4
 6. [Уд1] (О) На рисунке приведен график зависимости от времени проекции угловой скорости вращающегося тела на ось вращения.
6. [Уд1] (О) На рисунке приведен график зависимости от времени проекции угловой скорости вращающегося тела на ось вращения.
Момент действующих на тело сил был постоянным и не равным нулю на участке …
:2
 7. [Уд1] (О) На рисунке приведен график зависимости от времени проекции угловой скорости вращающегося тела на ось вращения.
7. [Уд1] (О) На рисунке приведен график зависимости от времени проекции угловой скорости вращающегося тела на ось вращения.
Момент импульса тела убывал на участках: …
:4,5
8. [Уд1] (О) На рисунке приведен график зависимости от времени проекции угловой скорости вращающегося тела на ось вращения. Максимальное по модулю угловое ускорение соответствует участку …
 :4
:4
9. [Уд1] (ВО1) Четыре шарика, размеры которых пренебрежимо малы, движутся по окружностям с одинаковой угловой скоростью. Массы шариков  и радиусы окружностей
и радиусы окружностей  указаны на рисунках. Момент импульса относительно оси, проходящей через центр окружности, максимален у шарика …
указаны на рисунках. Момент импульса относительно оси, проходящей через центр окружности, максимален у шарика …

:4
10. [Уд1] (ВО1) На тело действует постоянный вращающий момент. Из ниже перечисленных характеристик вращательного движения в этом случае изменяется с течением времени пропорциональна квадрату времени следующая величина –
1) угол поворота
2) угловая скорость
3) угловое ускорение
4) момент импульса
:1
11. [Уд1] (ВО1) На тело действует постоянный вращающий момент.
Из перечисленных ниже величин изменяется со временем по линейному закону величина –
1) момент инерции
2) угловое ускорение
3) угловая скорость
4) кинетическая энергия вращения
:3
12. [Уд1] (ВО1) Основное уравнение динамики вращательного движения –
1) 
2) 
3) 
4) 
:1
13. [Уд1] (ВО1) Формула, выражающая второй закон Ньютона для вращательного движения –
1) 
2) 
3) 
4) 
:3
 14. [Уд1] (О) На рисунке приведены различные виды графиков. Основному закону вращательного движения соответствует график….
14. [Уд1] (О) На рисунке приведены различные виды графиков. Основному закону вращательного движения соответствует график….
:1
15. [Уд1] (О) Верно указано направление момента силы для тела, совершающего равнозамедленное вращение, на рисунке …

:1
Тема: 110 Физические основы молекулярной физики
V114 – П Распределения Максвелла и Больцмана
S114 – П Распределение Больцмана (3 задания)
1. [Уд1] (ВО1).  На рисунке представлены зависимости давления от высоты для изотермической атмосферы, которые описываются барометрической формулой
На рисунке представлены зависимости давления от высоты для изотермической атмосферы, которые описываются барометрической формулой  . Температуры связаны между собой соотношением
. Температуры связаны между собой соотношением
1) T1 = T2
2) T1 > T2
3) T1 < T2
:3
2. [Уд1] (ВО1). Воздух у поверхности Земли находится при нормальных условиях (100 кПа и 00 С) и его температура и ускорение свободного падения g = 9,8 м/с2 не зависит от высоты. Молярная масса равна M = 29×10-3 кг/моль. Тогда отношение давления P 1 воздуха на высоте 1 км к давлению P 2 на дне скважины глубиной 1 км составляет
1) 0,5
2) 0,8
3) 1,2
4) 1,5
:2
3. [Уд1] (ВО1). Если температуру воздуха и ускорение силы тяжести считать не зависящими от высоты(t = 100 С, g = 9,8 м/с2, и M = 29×10-3 кг/моль), то плотность воздуха в e раз (e - основание натурального логарифма) меньше по сравнению с его плотностью на уровне моря на высоте … км.
1) 8,3
2) 6,5
3) 1,2
4) 4,7
:1
 C114 – П Распределение Максвелла – 13 заданий
C114 – П Распределение Максвелла – 13 заданий
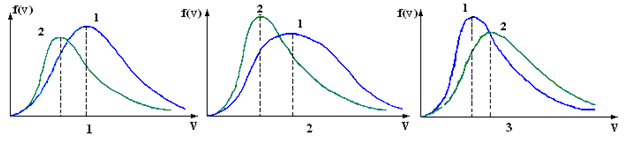
1. [Уд1] (ВОМ). Для распределения Максвелла по модулям скоростей молекул для разных газов при одинаковой температуре верны утверждения:
1) График 1 соответствует газу с большей массой молекул
2) График 2 соответствует газу с большей молярной массой.
3) Площадь под этими кривыми тем больше, чем больше молярная масса газа
4) Площади под этими кривыми одинаковы.
:1,4
2. [Уд1] (ВОМ). Верные утверждения:
1) функция распределения Максвелла f (v) зависит от массы молекулы газа
2) функция распределения Максвелла f (v) не зависит от температуры
3) f (v) является величиной размерной
4) f (v) носит экстремальный характер
:1,3,4
3. [Уд1] (ВО1). При изменении температуры Т газа средняя квадратичная скорость молекул этого газа увеличилась в 3 раза. Тогда максимальное значение функции распределения Максвелла  (e - основание натурального логарифма, V B - наиболее вероятная скорость молекул) … раз(а).
(e - основание натурального логарифма, V B - наиболее вероятная скорость молекул) … раз(а).
1) увеличится в 
2) уменьшится в 9
3) уменьшится в 3
4) увеличится в 
: 3
4. [Уд1] (ВОМ). Правильные утверждения о средней квадратичной скорости ( ) частиц системы, подчиняющейся распределению Максвелла:
) частиц системы, подчиняющейся распределению Максвелла:
1) При одинаковой температуре  молекул различных идеальных газов одинакова.
молекул различных идеальных газов одинакова.
2) Средняя квадратичная скорость  молекул газа при любой температуре меньше наиболее вероятной скорости.
молекул газа при любой температуре меньше наиболее вероятной скорости.
3) Чем больше масса молекулы газа, тем меньше  .
.
4) При возрастании температуры системы в четыре раза средняя квадратичная скорость  молекул увеличивается в два раза.
молекул увеличивается в два раза.
:3,4
5. [Уд1] (ВО1). Если средняя квадратичная скорость молекул водорода (M = 2×10-3 кг/моль) больше наиболее вероятной на D V = 400 м/с, то температура газа равна … К.
1) 180
2) 381
3) 230
4) 450
:2
6. [Уд1] (ВО1). Если средняя квадратичная скорость молекул некоторого газа равна 500 м/с, то наиболее вероятная скорость составляет … м/с.
1) 327
2) 250
3) 630
4) 408
:4
7. [Уд1] (ВО1). Если при нагревании некоторого газа наиболее вероятная скорость молекул газа увеличилась в 2 раза, то средняя квадратичная скорость … раз(а).
1) увеличится в 4
2) уменьшится в 
3) уменьшится в 8
4) увеличится в 2
:4
8. [Уд1] (ВО1). Если при нагревании некоторого газа средняя квадратичная скорость молекул газа увеличилась в 4 раза, при этом наиболее вероятная скорость … раз(а).
1) увеличится в 4
2) уменьшится в 
3) уменьшится в 8
4) увеличится в 2
:1
9. [Уд1] (ВО1). Три газа: водород, гелий и кислород находятся при одинаковой температуре T. Тогда значение f (Vвер) функции распределения Максвелла, соответствующее наиболее вероятной скорости молекул,..
1)одинаково для всех газов
2) максимально для водорода
3) минимально для гелия
4) максимально для кислорода
:4
10. [Уд1] (ВО1). Три газа: водород, гелий и кислород находятся при одинаковой температуре T. Тогда наиболее вероятная скорость Vвер …
1) у всех газов одинакова
2) у кислорода наибольшая
3) у гелия наименьшая
4) у водорода наибольшая
: 4
11. В статистике Максвелла функция распределения имеет вид  . НЕВЕРНОЕ утверждение о функции Максвелла –
. НЕВЕРНОЕ утверждение о функции Максвелла –
1) f (V) - вероятность того, что скорость данной молекулы находится в единичном интервале скоростей вблизи заданной скорости V.
2) f (V) dV - вероятность того, что скорость данной молекулы заключена в интервале скоростей от V до V+dV.
3) f (V) - относительное число молекул, скорости которых заключены в интервале скоростей от V до V+dV.
4) f (V) NdV - абсолютное число молекул, скорости которых заключены в интервале скоростей от V до V+dV.
:4
12.Правильные утверждения о наиболее вероятной скорости Vвер частиц системы, подчиняющейся распределению Максвелла:
1) Наиболее вероятная скорость Vвер зависит от температуры и молярной массы идеального газа.
2) Скорость Vвер можно найти, приравняв нулю производную функции распределения Максвелла по скоростям:  .
.
3) Чем больше молярная масса газа, тем меньше при данной температуре значение Vвер.
4) Vвер линейно возрастает с увеличением температуры.
:1,2,3
13. [Уд1] (ВО1). На рисунке представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где  - доля молекул, скорости которых заключены в интервале от
- доля молекул, скорости которых заключены в интервале от  до
до  в расчете на единицу этого интервала. Если, не меняя температуры, взять другой газ с большей молярной массой и таким же числом молекул, то
в расчете на единицу этого интервала. Если, не меняя температуры, взять другой газ с большей молярной массой и таким же числом молекул, то
1) величина максимума уменьшится
2) площадь под кривой увеличится
3) максимум кривой сместится влево, в сторону меньших скоростей
4) максимум кривой сместится вправо, в сторону больших скоростей
:3
S115 – М Распределение Больцмана -5 заданий
1. [Уд1] (ВОМ). Распределение Больцмана характеризует:
1) равновесное распределение частиц по координатам в стационарном потенциальном поле.
2) системы, состоящие как электронейтральных, так и заряженных классических частиц.
3) системы частиц со скоростями близкими к скорости света.
:1,2
2. [Уд1] (ВОМ). Формула  описывает распределение одинаковых молекул массой
описывает распределение одинаковых молекул массой  по высоте в изотермической атмосфере; здесь
по высоте в изотермической атмосфере; здесь  – концентрация молекул при
– концентрация молекул при  , n – их концентрация на высоте h. Для этой зависимости справедливы следующие утверждения:
, n – их концентрация на высоте h. Для этой зависимости справедливы следующие утверждения:
1) приведенные на рисунке кривые соответствуют распределениям для одного и того же газа при T2 > T1

2) приведенные на рисунке кривые соответствуют распределениям для двух разных газов при одинаковой температуре, причем m1 > m2

3) приведенные на рисунке кривые соответствуют распределениям для одного и того же газа, причем T2 < T1

4) приведенные на рисунке кривые соответствуют распределениям для двух разных газов при одинаковой температуре, причем массы молекул удовлетворяют соотношению m1 < m2

:1,2
3. [Уд1] (ВО1). Отношение концентрации  молекул водорода (M1 = 2×10-3 кг/моль) к концентрации
молекул водорода (M1 = 2×10-3 кг/моль) к концентрации  молекул азота (M2 = 28×10-3 кг/моль) равно h0, а на высоте h соответствующее составляет hh. Если температура Т = 380 Ки ускорение свободного падения g = 9,8 м/с2 не зависят от высоты, а отношение составляет
молекул азота (M2 = 28×10-3 кг/моль) равно h0, а на высоте h соответствующее составляет hh. Если температура Т = 380 Ки ускорение свободного падения g = 9,8 м/с2 не зависят от высоты, а отношение составляет  , то высота h равна … км.
, то высота h равна … км.
1) 3
2) 6
3) 4,5
4) 8,7
:1
4. [Уд1] (ВО1). Отношение концентрации  молекул водорода (M1 = 2×10-3 кг/моль) к концентрации
молекул водорода (M1 = 2×10-3 кг/моль) к концентрации  молекул азота (M2 = 28×10-3 кг/моль) равно h0, а на высоте h = 3000 м соответствующее составляет hh. Если температура Т и ускорение свободного падения g = 9,8 м/с2 не зависят от высоты, а отношение составляет
молекул азота (M2 = 28×10-3 кг/моль) равно h0, а на высоте h = 3000 м соответствующее составляет hh. Если температура Т и ускорение свободного падения g = 9,8 м/с2 не зависят от высоты, а отношение составляет  , то температура равна … К.
, то температура равна … К.
1) 380
2) 250
3) 540
4) 410
:1
5. [Уд1] (ВО1). Плотность водорода rh на высоте h на 10% меньше его плотности r0 на уровне моря. Если температура Т = 273 Ки ускорение свободного падения g = 9,8 м/с2 не зависят от высоты, то высота h равна … км.
1) 6,8
2) 9,4
3) 12,2
4) 15,7
:3
C115 – М Распределение Максвелла – 13 заданий
1. [Уд1] (ВО1). Функция распределения Максвелла для молекул газа имеет вид
1) 
2) 
3) 
4) 
:3
2. [Уд1] (ВО1). Если давление и плотность молекул газа соответственно составляют Р = 40 кПа и r = 0,35 кг/м3, то наиболее вероятная скорость равна … м/с.
1) 478
2) 630
3) 250
4) 346
:1
3. [Уд1] (ВО1). Если плотность газа r = 0,35 кг/м3, наиболее вероятная скорость его молекул 630 м/с, то давление равно … кПа.
1) 23,4
2) 69,5
3) 47,8
4) 53,6
:2
4. [Уд1] (ВО1). При нагревании некоторого газа средняя арифметическая скорость молекул этого газа увеличилась в 2 раза. При этом наиболее вероятная скорость … раз(а).
1) увеличилась в 
2) увеличилась в 4
3) уменьшилась в 8
4) увеличилась в 2
:4
5. [Уд1] (ВО1). В сосуде находятся одинаковые количества азота N2 и водорода H2. Распределение скоростей молекул газа в сосуде будет описываться кривыми, изображенными на рисунке под номером

1) 1
2) 2
3) 3
4) правильного рисунка нет
 :4
:4
6. [Уд1] (ВО1). На (Р,V) – диаграмме показан процесс, производимый идеальным газом в изолированной сосуде. Начальное и конечное состояния будут соответствовать распределениям скоростей, изображенным на рисунке
1) 1
2) 2
3) 3
:2
 7. [Уд1] (ВО1). В трех одинаковых сосудах находится одинаковое количество газа при разных температурах. Распределение скоростей молекул в сосуде с максимальной температурой будет описывать кривая, обозначенная номером
7. [Уд1] (ВО1). В трех одинаковых сосудах находится одинаковое количество газа при разных температурах. Распределение скоростей молекул в сосуде с максимальной температурой будет описывать кривая, обозначенная номером
1) 1
2) 2
3) 3
:3
8. [Уд1] (ВО1). Максимальное значение функции распределения Максвелла при данной температуре Т равно  (e - основание натурального логарифма, V B - наиболее вероятная скорость). Если при изменении температуры газа f (V B) уменьшится в 2 раза, то средняя квадратичная скорость молекул газа … раза.
(e - основание натурального логарифма, V B - наиболее вероятная скорость). Если при изменении температуры газа f (V B) уменьшится в 2 раза, то средняя квадратичная скорость молекул газа … раза.
1) увеличится в 4
2) уменьшится в 
3) уменьшится в 2
4) увеличится в 2
:4
9. [Уд1] (ВОМ). Правильные утверждения, относящиеся к функциям распределения Максвелла и Больцмана:
1) Функция распределения Максвелла позволяет найти распределение молекул по значениям потенциальной энергии.
2) Распределение Больцмана справедливо только в потенциальном поле силы тяжести.
3) Распределение молекул в пространстве устанавливается в результате совместного действия теплового движения и потенциального поля.
4) Распределение Больцмана характеризует распределение частиц классической системы по координатам после установления в системе равновесия.
:3,4
10. [Уд1] (ВО1). Если молярные массы азота и кислорода соответственно равны M1 = 28×10-3 кг/мольи M2 = 32×10-3 кг/моль, а наиболее вероятные скорости молекул азота и кислорода будут отличаться друг от друга на D V = 30 м/c, то температура смеси газов равна … К.
1) 180
2) 256
3) 363
4) 450
:3
11. [Уд1] (ВО1). При некоторой температуре распределение молекул газа по модулям скоростей оказалось таким, что скоростям V 1 = 200 м/с и V 2 = 800 м/с соответствует одинаковое значение функции распределения Максвелла f (v).
Тогда наиболее вероятная скорость молекул этого газа равна … м/с.
1) 250
2) 346
3) 465
4) 630
:3
12. [Уд1] (ВО1). При скорости V1 = 800 м/с значения функции распределения Максвелла по модулям скоростей f (V) одинаковы для кислорода и азота (см. рисунок). Молярные массы газов равны, соответственно, M 1 = 32×10-3 кг/моль и M 2 = 28×10-3 кг/моль. Тогда смесь газов находится при температуре … К.
1) 258
2) 471
3) 650
4) 769
:4
 13. [Уд1] (ВО1). На рисунке представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где
13. [Уд1] (ВО1). На рисунке представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где  - доля молекул, скорости которых заключены в интервале от
- доля молекул, скорости которых заключены в интервале от  до
до  в расчете на единицу этого интервала. Если, не меняя температуры, взять другой газ с меньшей молярной массой и таким же числом молекул, то
в расчете на единицу этого интервала. Если, не меняя температуры, взять другой газ с меньшей молярной массой и таким же числом молекул, то
1) высота максимума увеличится
2) площадь под кривой уменьшится
3) максимум кривой сместится вправо, в сторону больших скоростей
4) максимум кривой сместится влево, в сторону меньших скоростей
:4
S116 – МУО+КЗ Распределение Больцмана – 4 задания
1. [Уд1] (ВО1). Распределение Больцмана описывает распределение частиц по
1) координатам
2) кинетическим энергиям
3) импульсам
4) скоростям
:1
2. [Уд1] (ВОМ). Распределение Больцмана можно использовать, если справедливы утверждения:
1) температура в разных частях системы одинакова
2) температура в разных частях системы неодинакова
3) импульсы всех молекул системы одинаковы
4) система находится в состоянии равновесия
:1,4
3. [Уд1] (ВО1). Установленная вертикально закрытая с обоих концов труба наполнена газообразным кислородом M = 32×10-3 кг/моль. Высота трубы h = 200 м, ускорение силы тяжести g = 9,8 м/с2. Стенки трубы имеют всюду одинаковую температуру Т = 293 К. Давление газа внутри трубы вблизи ее основания равно Р 0 = 105 Па. Давление Р h в трубе вблизи верхнего его конца равно … кПа.
1) 87
2) 110
3) 97
4) 100
:3
4. [Уд1] (ВО1). На взлетной площадке барометр показывает давление P 0 = 100 кПа, а в кабине вертолета барометр показывает давление P = 90 кПа. Если температура воздуха (Т = 293 К) и ускорение силы тяжести (g = 9,8 м/с2) не изменяются с высотой и, молярная масса воздуха равна M = 29×10-3 кг/моль, то высота h, на которойлетит вертолет, равна … м.
1) 800
2) 900
3) 1000
4) 750
:2
C116 – МУО+КЗ Распределение Максвелла – 4 задания
1. [Уд1] (ВОМ) Абсолютное число dN молекул идеального газа, скорости которых при данной температуре T заключены в интервале от V до V + dV, зависит от:
1) температуры газа
2) от общего числа N молекул этого газа
3) от объема, занимаемого газом
4) от значения скорости V, в окрестности которой выбран рассматриваемый интервал dV
:1,2,4
2. [Уд1] (ВО1). Функция распределения Максвелла
1) не имеет экстремальный вид
2) является величиной безразмерной
3) может быть величиной отрицательной
4) при заданной температуре может соответствовать двум различным скоростям молекул газа
:4
3. [Уд1] (ВОМ). В статистике Максвелла функция распределения имеет вид  . Верные утверждения:
. Верные утверждения:
1) f (V) - относительное число молекул, скорости которых лежат в единичном интервале скоростей вблизи заданного значения скорости V.
2) f(V)dV - относительное число молекул, скорости которых заключены в интервале скоростей от V до V+dV.
3) f(V)NdV - число молекул, скорости которых заключены в интервале скоростей от V до V+dV.
4)  - абсолютное число молекул, скорости которых заключены в интервале от скорости V 1 до скорости V 2.
- абсолютное число молекул, скорости которых заключены в интервале от скорости V 1 до скорости V 2.
:1,2,3
4. [Уд1] (ВОМ). На рисунке изображен график функции распределения Максвелла молекул идеального газа по модулю скоростей.
Тогда площадь заштрихованной полоски есть:
1) относительное число молекул  , скорости которых заключены в интервале от V до V + dV.
, скорости которых заключены в интервале от V до V + dV.
2) вероятность того, что скорость данной молекулы имеет значение, заключенное в интервале от V до V + dV.
 3) доля молекул, скорости которых заключены в интервале от V до V + dV.
3) доля молекул, скорости которых заключены в интервале от V до V + dV.
4) число частиц, скорости которых заключены в интервале от V до V + dV.
:1,2,3
Дисциплина: Физика
Тема: 120 Термодинамика
V124 – П Энтропия и второе начало термодинамики.
S124 –П Энтропия и второе начало термодинамики (10 заданий).
 1. [Уд1] (ВОМ). Система может перейти из состояния 0 в состояния 1,2,3,4 (см. рисунок). Энтропия системы уменьшается в процессах:
1. [Уд1] (ВОМ). Система может перейти из состояния 0 в состояния 1,2,3,4 (см. рисунок). Энтропия системы уменьшается в процессах:
1) 0 ® 1
2) 0 ® 2
3) 0 ® 3
4) 0 ® 4
:1, 4
2. [Уд1] (ВОМ). Система может перейти из состояния 0 в состояния 1,2,3,4 (см. рисунок). Энтропия системы возрастает в процессах:
1) 0 ® 1
2) 0 ® 2
3) 0 ® 3
4) 0 ® 4
:3, 4
3. [Уд1] (ВОМ). Один моль гелия и один моль азота, находящиеся в закрытых сосудах, нагрели от температуры Т 1 до температуры Т 2. Тогда
1) изменения энтропий этих газов не зависят от объемов сосудов
2) изменения энтропий этих газов не зависят от скорости нагрева
3) Δ S N2 =Δ S He
4) ΔSN2 >ΔSHe
:2, 4
4. [Уд1] (ВО1). Изотермическое расширение одного моля азота проведено до удвоения объема. Такое же увеличение объема осуществлено для моля гелия. Тогда
1) ΔSN2 >ΔSHe
2) ΔSN2 <ΔSHe
3).Δ SN2 =Δ SHe
4) изменения энтропий этих газов зависят от скорости нагрева
:3
5. [Уд1] (ВОМ). Правильные утверждения:
1) равновесие термодинамическое состояние – это такое состояние термодинамической системы, при котором все ее термодинамические параметры остаются постоянными сколь угодно долго.
2) термодинамический процесс – это любое изменение термодинамического состояния системы.
3) неравновесный процесс – процесс, состоящий из ряда следующих друг за другом равновесных состояний.
4) обратимый процесс всегда является равновесным процессом.
: 1, 2, 4
6. [Уд1] (ВО1). Воду массой m = 0,1 кг нагревают от 0°С до 100°С и превращают в пар. Удельная теплоемкость воды c УД = 4,19×103 Дж/кг×К. Изменение энтропии при нагревании равно … Дж/К.
1) 131
2) 250
3) 347
4) 589
:1
7. [Уд1] (ВО1). При изобарическом расширении массы m = 8 г гелия от объема V 1 = 10 л до объема V 2 = 25 л приращение D S энтропии равно … Дж/К.
1) 14,9
2) 38,1
3) 37,6
4) 43,5
:2
8. [Уд1] (ВО1). При изотермическом расширении массы m = 6 г водорода от давления p 1 = 100 кПа до давления p 2 = 50 кПа приращение D S энтропии равно … Дж/К.
1) 17,3
2) 52,8
3) 87,6
4) 46,5
:1
9. [Уд1] (ВО1). Масса m = 10 г кислорода изохорически нагревается от температуры t 1 = 500 C до температуры t 2 = 1500 С, приращение D S энтропии равно … Дж/К.
1) 1,75
2) 2,45
3) 8,76
4) 4,96
:1
10. [Уд1] (ВО1). Масса m = 10 г кислорода изобарически нагревается от температуры t 1 = 500 C до температуры t 2 = 1500 С, приращение DS энтропии равно… Дж/К.
1) 1,75
2) 2,45
3) 7,63
4) 6,58
:2
C124 –П Тепловые двигатели (4 задания).
1. [Уд1] (ВО1).  На рисунке изображен цикл Карно в координатах (Т,S), где S – энтропия. Адиабатное расширение происходит на этапе
На рисунке изображен цикл Карно в координатах (Т,S), где S – энтропия. Адиабатное расширение происходит на этапе
1) 4 – 1
2) 2 – 3
3) 1 – 2
4) 3 - 4
:2.
2. [Уд1] (ВО1).  На рисунке изображен цикл Карно в координатах (Т,S), где S – энтропия. Адиабатное сжатие происходит на этапе
На рисунке изображен цикл Карно в координатах (Т,S), где S – энтропия. Адиабатное сжатие происходит на этапе
1) 4 – 1
2) 2 – 3
3) 1 – 2
4) 3 - 4
:1.
3. [Уд1] (ВО1).  На рисунке изображен цикл Карно в координатах (Т,S), где S – энтропия. Изотермическое расширение происходит на этапе
На рисунке изображен цикл Карно в координатах (Т,S), где S – энтропия. Изотермическое расширение происходит на этапе
1) 4 – 1
2) 2 – 3
3) 1 – 2
4) 3 - 4
:3.
4. [Уд1] (ВО1).  На рисунке изображен цикл Карно в координатах (Т,S), где S – энтропия. Изотермическое сжатие происходит на этапе
На рисунке изображен цикл Карно в координатах (Т,S), где S – энтропия. Изотермическое сжатие происходит на этапе
1) 4 – 1
2) 2 – 3
3) 1 – 2
4) 3 - 4
:4.
V125 – М Энтропия и второе начало термодинамики.
S125 –М Энтропия и второе начало термодинамики (17 заданий).
1. [Уд1] (ВО1). В изотермическом процессе изменение энтропии идеального газа рассчитывается по формуле
1) 
2) 
3) 
4) 
:3.
2. [Уд1] (ВО1). В изобарическом процессе изменение энтропии идеального газа рассчитывается по формуле
1) 
2) 
3) 
4) 
:4.
3. [Уд1] (ВО1). В изохорическом процессе изменение энтропии идеального газа рассчитывается по формуле
1) 
2) 
3) 
4) 
:2.
4. [Уд1] (ВО1). В адиабатическом процессе изменение энтропии рассчитывается по формуле
1) 
2) 
3) 
4) 
:1.
5. [Уд1] (ВО1). При поступлении в термодинамическую систему тепла δQ в ходе необратимого процесса приращение ее энтропии
1) 
2) 
3) 
4) 
:2
6. [Уд1] (ВОМ). Правильные утверждения о свойствах термодинамической вероятности:
1) термодинамическая вероятность – однозначная функция состояния системы
2) в равновесном состоянии термодинамическая вероятность максимальна
3) термодинамическая вероятность – величина мультипликативная
4) термодинамическая вероятность – величина аддитивная.
: 1, 2, 3
7. [Уд1] (ВОМ). Правильные утверждения:
1) Энтропия замкнутой системы c течением времени не убывает
2) Нельзя передать тепло от менее нагретого тела к более нагретому без изменений в окружающих телах.
3) Для адиабатически замкнутой системы Δ S ³ 0.
4) Энтропия замкнутой системы стремится к минимуму.
:1, 2, 3
8. [Уд1] (ВОМ). Формулировкой второго начала термодинамики могут служить утверждения:
1) Невозможно периодически действующее устройство, которое превращало бы тепло в работу полностью.
2) Энтропия замкнутой системы стремится к минимуму.
3) Всякая система, предоставленная сама себе, стремится перейти в наиболее вероятное макросостояние.
4) Наиболее вероятным изменением энтропии адиабатически замкнутой неравновесной системы является ее возрастание.
:1, 3, 4
9. [Уд1] (ВО1). Формулировкой второго начала термодинамики может служить утверждение
1) Энтропия – мера атомного (молекулярного) беспорядка в системе.
2) Количество тепла, подведенное к системе, затрачивается на изменение ее внутренней энергии и на совершение системой работы против внешних сил.
3) S = ln W, где W – термодинамическая вероятность системы
4) В адиабатически замкнутой системе энтропия при любом процессе не может убывать.
:4
10. [Уд1] (ВО1). Воду массой m = 0,1 кг, находящуюся при температуре кипения, превращают в пар. Удельная теплота парообразования воды l = 2,26×106 Дж/К. Изменение энтропии при парообразовании равно … Дж/К.
1) 231
2) 606
3) 347
4) 589
:2
11. [Уд1] (ВО1). Один моль кислорода занимающий при температуре Т 1 = 200 К объем V 1 = 10-2 м3 при нагревании до температуры Т 2 = 400 К расширяется до объема V 2 = 4×10-2 м3. Изменение энтропии равно … Дж/К.
1) 25,9
2) 61,7
3) 34,7
4) 85,9
:1
12. [Уд1] (ВО1). При переходе массы m = 8 г кислорода от объема V 1 = 10 л при температуре t 1 = 80°С к объему V 2 =40 л при температуре t 2 = 300°С приращение D S энтропии равно … Дж/К.
1) 1,9
2) 4,8
3) 5,4
4) 6,9
:3
13. [Уд1] (ВО1). При переходе массы m = 6 г водорода от объема V 1 = 20 л под давлением p 1 = 150 кПа к объему V 2 = 60 л под давлением p 2 = 100 кПа приращение D S энтропии равно … Дж/К.
1) 14,9
2) 53,4
3) 65,9
4) 70,6
:4
14. [Уд1] (ВО1). Масса m = 10,5 г азота изотермически расширяется от объема V 1 = 2 л до объема V 2 = 5 л, приращение D S энтропии при этом процессе равно … Дж/К.
1) 2,9
2) 5,8
3) 8,6
4) 4,5
:1
15. [Уд1] (ВО1). В результате нагревания массы m = 22 г азота его термодинамическая температура увеличилась от T 1 до T 2 = 1,2 T1, а энтропия увеличилась на D S = 4,16 Дж/К. Данный процесс производился при
1) постоянном объеме
2) постоянном давлении
3) адиабатическом расширении
4) адиабатическом сжатии
:2
16. [Уд1] (ВО1). Масса m = 6,6 г водорода расширяется изобарически от объема V 1 до объема V 2 = 2 V 1 приращение D S энтропии равно … Дж/К.
1) 14,9
2) 53,4
3) 70,6
4) 66,5
:4
17. [Уд1] (ВОМ). Правильные утверждения о свойствах энтропии:
1) энтропия – многозначная функция состояния системы
2) в равновесном состоянии энтропия максимальна
3) в равновесном состоянии энтропия минимальна
4) энтропия – величина аддитивная.
: 2, 4
C125 –М Тепловые двигатели (12 заданий).
1. [Уд1] (ВО1). На рисунке изображен цикл Карно в координатах (Т,S), где S – энтропия. Количество теплоты, полученной от нагревателя, определяется по формуле
 1)
1) 
2) 
3) 
4) 
:1.
2. [Уд1] (ВО1). На рисунке изображен цикл Карно в координатах (Т,S), где S – энтропия. Количество теплоты, отданное холодильнику, определяется по формуле
 1)
1) 
2) 
3) 
4) 
:3.
 3. [Уд1] (ВО1) КПД термодинамических циклов, работающих по циклам 1-2-3-4-1 и 1-2-3-1 соотносятся следующим образом –
3. [Уд1] (ВО1) КПД термодинамических циклов, работающих по циклам 1-2-3-4-1 и 1-2-3-1 соотносятся следующим образом –
1) у втор

Биохимия спиртового брожения: Основу технологии получения пива составляет спиртовое брожение, - при котором сахар превращается...

Эмиссия газов от очистных сооружений канализации: В последние годы внимание мирового сообщества сосредоточено на экологических проблемах...

Особенности сооружения опор в сложных условиях: Сооружение ВЛ в районах с суровыми климатическими и тяжелыми геологическими условиями...

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!