

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

Особенности сооружения опор в сложных условиях: Сооружение ВЛ в районах с суровыми климатическими и тяжелыми геологическими условиями...

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

Особенности сооружения опор в сложных условиях: Сооружение ВЛ в районах с суровыми климатическими и тяжелыми геологическими условиями...
Топ:
Установка замедленного коксования: Чем выше температура и ниже давление, тем место разрыва углеродной цепи всё больше смещается к её концу и значительно возрастает...
Техника безопасности при работе на пароконвектомате: К обслуживанию пароконвектомата допускаются лица, прошедшие технический минимум по эксплуатации оборудования...
Интересное:
Аура как энергетическое поле: многослойную ауру человека можно представить себе подобным...
Отражение на счетах бухгалтерского учета процесса приобретения: Процесс заготовления представляет систему экономических событий, включающих приобретение организацией у поставщиков сырья...
Мероприятия для защиты от морозного пучения грунтов: Инженерная защита от морозного (криогенного) пучения грунтов необходима для легких малоэтажных зданий и других сооружений...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Вопрос 1 «Теория строения органических соединений А.М. Бутлерова»
Основные положения теории строения органических соединений А.М. Бутлерова:
1. В молекулах атомы соединены друг с другом в определенной последовательности в соответствии с их валентностью. Порядок связи атомов называется химическим строением.
2. Свойства вещества зависят не только от того, какие атомы и в каком количестве входят в состав его молекулы, но и от того, в каком порядке они соединены между собой, т.е. от химического строения молекулы.
3. Атом или группа атомов, образовавшие молекулу, взаимно влияют друг на друга, от чего зависит реакционная способность молекулы.
Вопрос 2 «Строение оксогруппы. Химические свойства оксосоединений (на примере этаналя)»
Альдегиды и кетоны относятся к карбонильным органическим соединениям.
Карбонильными соединениями называют органические вещества, в молекулах которых имеется группа >С=О (карбонил или оксогруппа).
Общая формула карбонильных соединений:

Этаналь СН3-СНО. Химические свойства:
По химическим свойствам ацетальдегид аналогичен формальдегиду: для него также характерны реакции окисления и присоединения. Реакция"серебряного зеркала" и образования оксида меди (|).

Присоединение водорода к ацетальдегида протекает в тех же условиях, что и к формальдегиду.

При действии кислот или при длительном состоянии ацетальдегид легко полимеризуется, переходя в тример- паральдегид.

В промышленности ацетальдегид получают из ацетилена по реакции Кучерова


Вопрос 3 «Изобразите схематически перекрывание орбиталей с образованием сигма связей между sp2 гибридизованным атомом углерода и атомом водорода»
|
|
Происходит при смешивании одной s- и двух p-орбиталей. Образуются три гибридные орбитали с осями, расположенными в одной плоскости и направленными к вершинам треугольника под углом 120 градусов. Негибридная p-атомная орбиталь перпендикулярна плоскости и, как правило, участвует в образовании π-связей

Вопрос 7 «Конформация алканов»
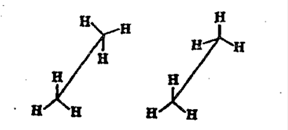
Различные положения углеродной цепи называются конформациями. В нормальных условиях конформации алканов свободно переходят друг в друга с помощью вращения С-С связей, поэтому их часто называют поворотными изомерами. Существует 2 основные конформации – «заторможенное» (энергетически более выгодна и молекула находятся в этой форме больше времени) и «заслоненное»:

Механизм I.
I стадия. Катион алкилгидроксония, отщепляя воду, превращается в карбокатион:
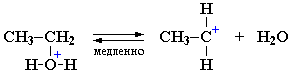
Роль кислоты, таким образом, заключается в превращении ОН-группы в Н2О, которая отщепляется легче, чем анион НО–.
II стадия. Карбокатион вызывает гетеролитический разрыв связи в галогеноводороде и присоединяет галогенид-анион с образованием конечного продукта:

Или


Освободившийся H+ идет на протонирование новых молекул спирта.
Механизм II.
Другой возможный механизм нуклеофильного замещения заключается в практически одновременном отщеплении воды и присоединении галогена (без образования карбокатиона) и идет в одну стадию.

Механизм замещения зависит от строения реагентов и условий реакции. Для третичных спиртов предпочтительней первый механизм, а для первичных - второй.
На стадии, определяющей скорость реакции (так называемой, лимитирующей стадии), в механизме I образуется карбокатион. Чем стабильнее этот катион, тем легче он образуется. Третичный катион стабильнее, чем первичный (три +I-эффекта алкильных групп в третичном катионе и один - в первичном). С другой стороны, энергия переходного состояния в механизме II тем ниже, чем меньше стерические препятствия, т.е. чем меньше алкильных групп у атакуемого атома углерода.
|
|
Изомерия алкенов
Наряду со структурной изомерией углеродного скелета для алкенов характерны, во-первых, другие разновидности структурной изомерии - изомерия положения кратной связи и межклассовая изомерия.
Во-вторых, в ряду алкенов проявляется пространственная изомерия, связанная с различным положением заместителей относительно двойной связи, вокруг которой невозможно внутримолекулярное вращение.
1. Изомерия углеродного скелета (начиная с С4Н8):

2. Изомерия положения двойной связи (начиная с С4Н8):

3. Межклассовая изомерия с циклоалканами, начиная с С3Н6:

Номенклатура
Алкены простого строения часто называют, заменяя суффикс -ан в алканах на -илен: этан — этилен, пропан — пропилен и т.д.
По систематической номенклатуре названия этиленовых углеводородов производят заменой суффикса -ан в соответствующих алканах на суффикс -ен (алкан — алкен, этан — этен, пропан — пропен и т.д.). Выбор главной цепи и порядок названия тот же, что и для алканов. Однако в состав цепи должна обязательно входить двойная связь. Нумерацию цепи начинают с того конца, к которому ближе расположена эта связь. Например:

Вопрос 11 «Химические свойства многоатомных спиртов на примере этиленгликоля»
Химические свойства многоатомных спиртов включают в себя все химические свойства одноатомных спиртов. Также многоатомные спирты реагируют с нерастворимыми основаниями.
К примеру, глицерин реагирует с гидроксидом меди в присутствии щелочи с образованием ярко-голубого соединения (глицерат меди).
В аналогичную реакцию вступает и этиленгликоль. Реакция с гидроксидом меди является качественной реакцией на многоатомные спирты.

Нитрование
Нитрование является механистическим прототипом всех остальных реакций электрофильного ароматического замещения. Эта реакция находит широкое синтетическое применение и механизм ее изучен наиболее подробно.
Номенклатура
По международной номенклатуре ИЮПАК, карбоновые кислоты называют, выбирая за основу наиболее длинную углеродную цепочку, содержащую группу -СООН, и добавляя к названию соответствующего углеводорода окончание «овая» и слово «кислота». При этом атому углерода, входящему в состав карбоксильной группы, присваивается первый номер. Например СН3-СН2-СООН — пропановая кислота, СН3-С(СН3)2-СООН — 2,2-диметилпропановая кислота.
По рациональной номенклатуре к названию углеводорода добавляют окончание «карбоновая» и слово «кислота», не включая при этом в нумерацию цепи атом углерода карбоксильной группы. Например, С5Н9СООН — циклопентанкарбоновая кислота, СН3-С(СН3)2-СООН — трет -бутилкарбоновая кислота.
Многие из карбоновых кислот имеют тривиальные названия (некоторые из них приведены в таблице).
|
|
Получение:
2. Окисление алканов:
2CH4 + + 3O2 t,kat → 2HCOOH + 2H2O
метан муравьиная кислота
2CH3-CH2-CH2-CH3 + 5O2 t,kat,p → 4CH3COOH + 2H2O
н-бутан уксусная кислота
3. Окисление алкенов:
CH2=CH2 + O2 t,kat → CH3COOH
этилен
СH3-CH=CH2 + 4[O] t,kat → CH3COOH + HCOOH (уксусная кислота+муравьиная кислота)
4. Окисление гомологов бензола (получение бензойной кислоты):
C6H5-CnH2n+1 + 3n[O] KMnO4,H+→ C6H5-COOH + (n-1)CO2 + nH2O
5C6H5-CH3 + 6KMnO4 + 9H2SO4 → 5C6H5-COOH + 3K2SO4 + 6MnSO4 + 14H2O
толуол бензойная кислота
5. Получение муравьиной кислоты:
1 стадия: CO + NaOH t,p → HCOONa (формиат натрия – соль)
2 стадия: HCOONa + H2SO4 → HCOOH + NaHSO4
6. Получение уксусной кислоты:
CH3OH + CO t,p → CH3COOH
Метанол
1. Гидролиз сложных эфиров:
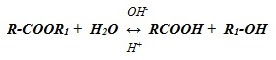
2. Из солей карбоновых кислот:
R-COONa + HCl → R-COOH + NaCl
3. Растворением ангидридов карбоновых кислот в воде:
(R-CO)2O + H2O → 2 R-COOH
4. Щелочной гидролиз галоген производных карбоновых кислот:
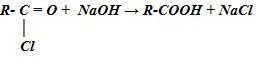
Вопрос 17 «Сложные эфиры»
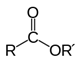
СЛОЖНЫЕ ЭФИРЫ – класс соединений на основе минеральных (неорганических) или органических карбоновых кислот, у которых атом водорода в НО-группе замещен органической группой R. Прилагательное «сложные» в названии эфиров помогает отличить их от соединений, именуемых простыми эфирами.
Номенклатура сложных эфиров. Название создается следующим образом: вначале указывается группа R, присоединенная к кислоте, затем – название кислоты с суффиксом «ат» (как и в названиях неорганических солей: карбонат натрия, нитрат хрома).

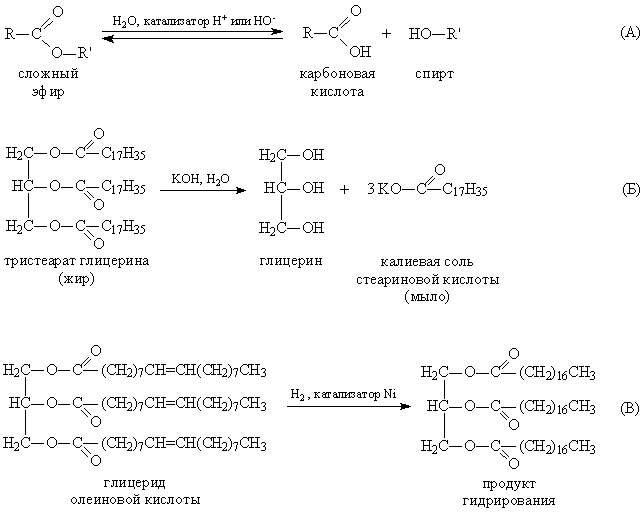
Химические свойства сложных эфиров. Наиболее характерно для эфиров карбоновых кислот гидролитическое (под действием воды) расщепление сложноэфирной связи, в нейтральной среде оно протекает медленно и заметно ускоряется в присутствии кислот или оснований, т.к. ионы Н+ и НО– катализируют этот процесс (рис. 4А), причем гидроксильные ионы действуют более эффективно. Гидролиз в присутствии щелочей называют омылением. Если взять количество щелочи, достаточное для нейтрализации всей образующейся кислоты, то происходит полное омыление сложного эфира.
|
|
Химические свойства
Фенолокислоты одновременно обладают свойствами карбоновых кислот и фенолов. Кроме того, для них характерны свойства, обусловленные наличием в молекуле обоих видов функциональных групп и бензольного ядра.
Разложение при нагревании
Фенолокислоты при нагревании разлагаются с образованием фенольных соединений и углекислого газа. Например, при нагревании салициловая кислота разлагается на фенол и углекислый газ:
НОС6Н4СООН → С6Н5ОН + СО2
салициловая кислота фенол углекислый газ
Галловая кислота при нагревании теряет карбоксильную группу и превращается в трехатомный фенол — пирогаллол.
Вопрос 1 «Теория строения органических соединений А.М. Бутлерова»
Основные положения теории строения органических соединений А.М. Бутлерова:
1. В молекулах атомы соединены друг с другом в определенной последовательности в соответствии с их валентностью. Порядок связи атомов называется химическим строением.
2. Свойства вещества зависят не только от того, какие атомы и в каком количестве входят в состав его молекулы, но и от того, в каком порядке они соединены между собой, т.е. от химического строения молекулы.
3. Атом или группа атомов, образовавшие молекулу, взаимно влияют друг на друга, от чего зависит реакционная способность молекулы.
Вопрос 2 «Строение оксогруппы. Химические свойства оксосоединений (на примере этаналя)»
Альдегиды и кетоны относятся к карбонильным органическим соединениям.
Карбонильными соединениями называют органические вещества, в молекулах которых имеется группа >С=О (карбонил или оксогруппа).
Общая формула карбонильных соединений:

Этаналь СН3-СНО. Химические свойства:
По химическим свойствам ацетальдегид аналогичен формальдегиду: для него также характерны реакции окисления и присоединения. Реакция"серебряного зеркала" и образования оксида меди (|).

Присоединение водорода к ацетальдегида протекает в тех же условиях, что и к формальдегиду.

При действии кислот или при длительном состоянии ацетальдегид легко полимеризуется, переходя в тример- паральдегид.

В промышленности ацетальдегид получают из ацетилена по реакции Кучерова


Вопрос 3 «Изобразите схематически перекрывание орбиталей с образованием сигма связей между sp2 гибридизованным атомом углерода и атомом водорода»
|
|
Происходит при смешивании одной s- и двух p-орбиталей. Образуются три гибридные орбитали с осями, расположенными в одной плоскости и направленными к вершинам треугольника под углом 120 градусов. Негибридная p-атомная орбиталь перпендикулярна плоскости и, как правило, участвует в образовании π-связей

|
|
|

Эмиссия газов от очистных сооружений канализации: В последние годы внимание мирового сообщества сосредоточено на экологических проблемах...

Историки об Елизавете Петровне: Елизавета попала между двумя встречными культурными течениями, воспитывалась среди новых европейских веяний и преданий...

Индивидуальные очистные сооружения: К классу индивидуальных очистных сооружений относят сооружения, пропускная способность которых...

Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов (88‰)...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!