Газы и пыли выделяющиеся из углистой породы, кг
SiO 59,2 · 0,5932 · 0,07 · 44 / 60 = 1,803
Al2O 59,2 · 0,3367 · 0,05 · 70 / 102 = 1,368
Са 59,2 · 0,0168 · 0,05 · 40 / 56 = 0,036
Mg 59,2 · 0,0064 · 0,15 · 24 / 40 = 0,034
P 59,2 · 0,0005 · 0,10 · 62 / 142 = 0,001
S 0,41 · 0,70 = 0,287
V 18,700
W 5,100
C + О→CO (21,69 + 20,468 ·16/12) = 48,980
Σ 76,309
Газы и пыли выделяющиеся из кварцита, кг
SiO 14,879 · 0,982· 0,07 · 44 / 60 = 0,750
Al2O 14,879 · 0,0085· 0,10 · 70 / 102 = 0,009
Са 14,879 · 0,0013 · 0,05 · 40 / 56 = 0,001
Mg 14,879 · 0,0007 · 0,15 · 24 / 40 = 0,001
S 14,879 · 0,0002 · 0,70 = 0,002
W 14,879 · 0,0019 = 0,028
О→СО 14,879 · (37,537/100)*(16/12) = 7,447
Σ 8,238
Газы и пыли выделяющиеся из стружки, кг
S 5 · 0,0002 · 0,70 = 0,001
V 5 · 0,03 = 0,150
Σ 0,151
Из электродной массы 2,8 кг также расходуются на образование СО газа.
Результаты проведенных расчетов сводится в таблицу 6 и находится количество газов, пыли и улета
Таблица 6 – Количество газов, пыли и улета
| Элемент
| Источник поступления
| Итого
|
| Кварцит
| Стружка
| УП
| кг
| %
|
| SiO
| 0,750
| -
| 1,803
| 2,553
| 2,918
|
| Al2O
| 0,009
| -
| 1,368
| 1,377
| 1,573
|
| Ca
| 0,001
| -
| 0,036
| 0,036
| 0,041
|
| Mg
| 0,001
| -
| 0,034
| 0,035
| 0,040
|
| P
| -
| -
| 0,001
| 0,001
| 0,002
|
| S
| 0,002
| 0,001
| 0,287
| 0,290
| 0,330
|
| V (ППП)
| 0,000
| 0,150
| 18,700
| 18,850
| 21,544
|
| W
| 0,028
| -
| 5,100
| 5,128
| 5,861
|
| СО
| 7,447
| 2,800*
| 48,981
| 59,228
| 67,691
|
| Всего
| 8,238
| 2,951
| 76,309
| 87,497
| 100,000
|
* поступает из электрода
Материальный баланс
Таблица 7 – Материальный баланс
| Задано
| кг
| %
| Получено
| кг
| %
|
| Углистая порода
| 105,100
| 82,2
| металл
| 37,436
| 29,3
|
| Кварцит
| 14,879
| 11,6
| шлак
| 2,946
| 2,3
|
| Стружка
| 5,000
| 3,9
| газы и прочие
| 87,497
| 68,4
|
| Электроды
| 2,900
| 2,3
| невязка
|
|
|
| Итого
| 127,879
| 100,00
|
| 127,879
| 100,00
|
В результате материального баланса невязка составляет
127,879 - 37,436 - 2,946 - 87,497 = 0,000
Удельный расход материалов
Углистая порода 1000 · 100 / 37,436 = 2807,5 кг/т
Кварцит 1000 · 14,879 / 37,436 = 397, 5 кг/т
Стружка 1000 · 5,000 / 37,436 = 133,6 кг/т
Электродная масса 1000 · 2,900 / 37,436 = 77,5 кг/т
Расчет теплового баланса
Тепловой баланс непрерывного углевосстановительного процесса получения ферросплавов определяется равенством, кДж.
Qспл. + Qшл. + Qгаз + Qэнд. + Qпот. = Qфиз. + Qэкз. + Qэл.эн.
Qспл., Qшл.,Qгаз – теплосодержание продуктов;
Qэнд. – тепловые затраты на эндотермические процессы;
Qпот. – тепловые потери процесса;
Qфиз. – физическое тепло нагретой шихты;
Qэкз . – экзотермическое тепло реакции окисления и шлакообразования;
Qэл.эн. – тепло, вводимое электроэнергией. Определяется как разность между расходной и приходной частями баланса.
Результатом составления теплового баланса является определение удельного расхода электроэнергии на тонну сплава. Правильность расчетов определяется совпадением расчетных и практических данных удельного расхода электроэнергии.
Приход тепла
Физическое тепло шихты
В расчетах, как правило, за нулевую отметку по температуре принимают температуру окружающей среды. Так как в нашем случае по условиям расчета не предусмотрен предварительный нагрев шихты, то шихта не будет вносить дополнительное количество тепла Qфиз . = 0.
Экзотермическое тепло реакций
Статья включает тепло металлообразования Qэкз.мет. и тепло шлакообразования Qэкз.шл .. Тепло от растворения кремния и углерода в сплаве, образования силикатов в шлаке рассчитывают по количеству окислившегося элемента или образовавшегося соединения gi и соответствующему тепловому эффекту (табл. 10)

1. Тепло металлообразования Qэкз.мет. складывается в основном из реакций образования в сплаве силицидов железа (остальным пренебрегаем). Принимаем, что все железо в ферросиликоалюминии связано только с кремнием и присутствует в виде FeSi. Образование силицида железа происходит по реакции
Fe + Si = FeSi ΔH = - 73,70 кДж/моль.
При растворении 6,729 кг железа в кремнии выделится тепла
Qэкз.мет. = 6,729 · 73,70 / 0,056 = 8 855 кДж.
2. Тепло шлакообразования Qэкз.шл при выплавке ферросиликоалюминия складывается в основном из реакций образования в шлаке силикатов магния и кальция, а также муллита (остальным пренебрегаем). Принимаем, что весь оксид алюминия в шлаке связан только с кремнеземом и присутствует в виде муллита 3Al2O3·2SiO2. Образование муллита из оксидов происходит по реакции
3Al2O3 + 2SiO2 = 3Al2O3·2SiO2
ΔH = - 6824,48 + 2 · 911,55 + 3 · 1676,81 = - 29,05 кДж/моль.
При образовании муллита из 1,003 кг оксида алюминия выделится тепла
Q1 = 1,003 · 29,05 / 0,306 = 286 кДж.
Принимаем, что оксид кальция в шлаке связан с кремнеземом и присутствует в виде силиката кальция CaO·SiO2. Образование силиката кальция происходит по реакции
СаO + SiO2 = СаO·SiO2
ΔH = - 1635 + 635,6 + 911,55 = 88,05 кДж/моль.
При образовании силиката кальция из 0,558 кг оксида кальция выделится тепла
Q2 = 0,558 · 88,05 / 0,056 = 1 564 кДж.
Также принимаем, что оксид магния в шлаке связан с кремнеземом и присутствует в виде форстерита 2MgO·SiO2. Образование форстерита происходит по реакции
2MgO + SiO2 = 2MgO·SiO2
ΔH = - 2173,37 + 2·601,89 + 911,55 = 58,04 кДж/моль.
На образование форстерита расходуется 0,311 кг оксида магния, при этом выделится тепла
Q3 = 0,311 ·58,04 / 0,080 = 226 кДж.
Таким образом, при шлакообразовании выделится тепла
Qэкз.шл = 286 + 1 564 + 226 = 2 075 кДж.
Qэкз. = Qэкз.мет. + Qэкз.шл = 8 855 + 2 075 = 10 931 кДж.
Расход тепла
2.2.1 Теплосодержание сплава при температуре выпуска
Теплосодержание сплава определяется теплоемкостью, температурой и массой сплава (на основе материального баланса) при нагреве сплава до температуры плавления, теплотой плавления и перегрева жидкого сплава до температуры выпуска из печи.
Для стандартных сплавов величину теплосодержания сплава следует считать по экспериментально определенным постоянным теплофизическим величинам согласно нижеприведенной формуле
 .
.
Для нестандартных сплавов, таких как ферросиликоалюминий, величину теплосодержания сплава следует считать аддитивно по основным (трем-четырем) составляющим компонентам по справочным данным согласно нижеприведенной формуле


В этом случае для каждого компонента (элемента) сплава его теплосодержание подсчитывают по справочным данным (табл. 8) для температурных данных и фазовых переходов:
- нагрев до плавления;
- плавление или растворение;
- перегрев над температурой плавления сплава.
Используя данные, приведенные в таблице 8, рассчитываем теплосодержание ферросиликоалюминия при температуре выпуска 1900°С

Таблица 8 – Теплофизические величины основных элементов ФСА
| Элемент
|  , Дж/моль∙К , Дж/моль∙К
| Энтальпия плавления Lпл, кДж/моль
| Температура плавления Тпл, К
| Теплоемкость в жидком состоянии Сж, Дж/моль∙К
|
| a
| b∙ 103
| c∙ 10-5
|
| Fe
| 17,50
| 24,79
| -
| 13,8
|
| 46,0
|
| Si
| 23,95
| 2,47
| -4,14
| 49,9
|
| 27,2
|
| Al
| 4,94
| 2,96
| -
| 10,8
|
| 31,75
|


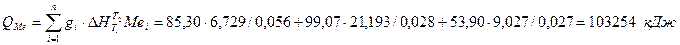
2.2.2 Теплосодержание шлака при температуре выпуска
Температура шлака на выпуске превышает аналогичные для сплавов на 50-80°С, т.е. находится на уровне 1950°С. Теплосодержание шлака при отсутствии экспериментальных данных можно оценить аддитивно, по основным (трем-четырем) составляющим компонентам по справочным данным согласно нижеприведенным формулам:


Однако температуры плавления большинства оксидов, составляющих шлак, намного выше температуры плавления самого шлака. Поэтому, строго говоря, оксиды не плавятся, образуя шлак, а растворяются. Однако однотипность физических процессов лежащих в основе плавления и растворения, позволяет уравнять изменения энтальпии в этих процессах

Таким образом, задаваясь нижеприведенным справочными данными (табл. 9), рассчитаем теплосодержание шлака при температуре 1950°С для основных составляющих шлака (MgO, SiO2, Al2O3, СаО), сумма которых превышает 99% от общей массы.
Таблица 9 – Теплофизические величины основных компонентов шлака и газа
| Элемент
|  , Дж/моль∙К , Дж/моль∙К
| Энтальпия плавления, кДж/моль
| Температура плавления, К
| Теплоемкость в жидком состоянии, Дж/моль∙К
|
| a
| b∙ 103
| c∙ 10-5
|
| Al2O3
| 114,84
| 12,81
| -35,46
| 113,04
|
| 144,96
|
| SiO2
| 46,98
| 34,33
| -11,3
| 0,63
| 0-848
| -
|
| 60,33
| 8,12
|
| 7,70
| 848-1996
| 85,82
|
| MgO
| 42,62
| 7,28
| -6,2
| 77,46
|
| 84,0
|
| Cr2O3
| 113,04
| 9,21
| -15,66
| 125,0
|
| 156,9
|
| СО
| 28,43
| 4,1
| -0,46
| -
| -
| -
|





2.2.3 Теплосодержание газообразных продуктов
Допустим, что газы покидают печь при средней температуре 1000°С. Для упрощения расчетов принимаем теплоемкости всех газообразных продуктов равными теплоемкости оксида углерода СО, основной составляющей газообразной фазы





 .
.


 , Дж/моль∙К
, Дж/моль∙К


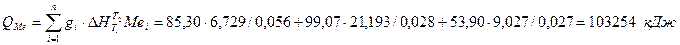



 , Дж/моль∙К
, Дж/моль∙К








