Основы:
Первый закон термодинамики гласит, что в любой изолированной системе энергия сохраняется. Ученому-физику Джоуль установил, что энергия, выделяемая гидравлической, пневматической, электрической и механической системами, может превращаться в тепло.
Если энергия никогда не теряется, то как ее может не хватать? На самом деле энергии не не хватает - она всегда имеется в изобилии, хотя лишь малая часть ее содержится в форме, пригодной для использования. Будем считать Землю изолированной системой, хотя она таковой не является, так как поглощает энергию излучения Солнца и в конечном счете повторно излучает ее в космическое пространство. Все ископаемые топлива, хранящиеся в Земле, в любой момент времени представляют собой запас высокопотенциальной энергии, которую можно выделить при горении. Если бы все ископаемые топлива сразу сгорели, то результирующее энергосодержание Земли, рассматриваемой как изолированная система, не изменилось, поскольку температура окружающей среды повысилась бы на величину, в точности соответствующую выделению энергии ископаемых топлив. Мы израсходовали бы весь запас высокопотенциальной энергии только на повышение температуры окружающей среды. Не потеряв в действительности энергии, мы стали бы тем не менее "энергетическими банкротами".
Энергия на уровне окружающей среды бесполезна для совершения работы. В холодный зимний день воздух при температуре 30°С пригоден для использования, поскольку этим воздухом можно обогревать дома. Но в теплый летний день тот же самый воздух бесполезен, так как он находится в энергетическом равновесии с окружающей средой. Таким образом, ценность конкретной формы энергии определяется ее уровнем (температурой) по отношению к окружающей среде. Холодную воду при температуре 4°С можно использовать для охлаждения, тогда как горячую воду с температурой 50°С можно использовать для стирки, но стоит их смешать, и смесь окажется почти бесполезной.
Таким образом, необходимо определить термин "экономия энергии" так, чтобы он имел смысл для наших усилий в этом направлении. Мы можем стремиться к "экономии топлива", и такая терминология может удовлетворить большинство наших критериев. Но для количественного описания наших усилий, направленных на экономию энергии, необходим общий критерий, относящийся ко всем видам энергии - топливу, электричеству, пару, солнечному излучению и т.д. Этот общий критерий можно получить из термодинамики. Применяя второй закон термодинамики, можно оценить полезность любого вида и уровня энергии. Более того, можно определить эффективность расходования этой энергии и найти способ его улучшения.
Хотя Джоулю удалось количественно описать процесс превращения работы в тепло, сделать обратное довольно трудно. Второй закон термодинамики утверждает, что тепло нельзя полностью превратить в работу в круговом процессе (т.е. некоторое количество тепла останется непреобразованным). Причина этого ограничения состоит в том, что можно достичь равновесия только в результате перетекания тепла или массы от высокого энергетического уровня к низкому. Эти соотношения можно лучше всего оценить, вводя понятия энтропии и располагаемой работы.
Энтропия как мера необратимости.
Трение в механических деталях теплового двигателя необратимо преобразует работу вала в тепло. Действительная работа, совершаемая двигателем, меньше, чем располагаемая работа, содержащаяся в жидкости: W = Q - ∆H.
Где вместо располагаемой работы и обратимого тепла стоят действительная работа и действительное тепло.
Если начальное и конечное состояния жидкости одинаковы, как в случае, когда процесс в тепловом двигателе обратим, то энтропия, потерянная жидкостью, тоже одинакова - энтропия является параметром состояния. Поэтому превышение Q над QR показывает, что энтропия окружающей среды изменилась больше, чем энтропия жидкости; в результате это приводит к возрастанию энтропии системы S: ∆S=∆S0+∆SK>0, и производимая работа является функцией энтропии, приобретенной окружающей средой.
W= - T0 ∆S0 - ∆H. Следовательно, потери располагаемой работы прямо пропорциональны результирующему приросту энтропии системы: W0 –W = T0 ∆S.
Тогда влияние трения можно количественно определить как прирост энтропии системы. Поэтому сохранение располагаемой работы заключается в сведении к минимуму прироста энтропии в любом процессе, следовательно, в сведении к минимуму его необратимости.
Располагаемая работа, обратимые процессы и необратимые процессы.
Энергию можно использовать в двух видах: в виде тепла и работы. Работа является высшей формой энергии, поскольку ее можно полностью превратить в тепло, тогда как обратное невозможно. Только часть тепловой энергии, можно превратить в работу в замкнутом круговом процессе, что зависит от следующих факторов:
а) начального и конечного состояний жидкости;
б) термодинамического к.п.д. процесса.
Из заданной массы очень горячей жидкости (например, водяного пара) можно извлечь больше работы, чем из более холодной жидкости, даже если масса последней такова, что в ней содержится достаточное количество энергии по отношению к энергии окружающей среды. Горючий газ можно использовать для приведения в действие турбины или для обогрева помещения; в то же время воздух при 50° С может обогревать помещение, но его температура недостаточна для работы турбины. Следовательно, не нужно использовать горючий газ для обогрева помещений, а нужно сохранять его для таких процессов, в которых можно наилучшим образом использовать его располагаемую работу. Наоборот, можно обогревать помещения, используя жидкости, располагаемая работа которых невелика, например нагретой солнцем водой или отработавшим паром турбины.
Поэтому жидкости с высокой температурой или топлива, продукты сгорания которых имеют высокую температуру, имеют большую ценность по сравнению с той, которая определяется только их энтальпией. Хорошей мерой их ценности является заключенная в них располагаемая работа, с помощью которой их можно сравнить с электрической или механической энергией, способной непосредственно превращаться в работу.
Процесс, в котором состояние жидкости изменяется благодаря приложенной работе и в котором жидкость, возвращаясь в исходное состояние, может произвести такое же количество работы, называется обратимым. Примером обратимого процесса является процесс в идеальном компрессоре, работающем на идеальном газе. Работа, приложенная к компрессору, может повысить давление и температуру газа. Если система совершенна, т.е. в ней нет трения или потерь тепла, расширение газа может произвести в точности такое же количество работы, которое было затрачено на его сжатие. Хотя потери на трение и тепловые потери, а также неидеальность жидкости, приведут на практике к тому, что восстановится меньшее количество работы, чем было приложено, процесс сжатия — расширения по крайней мере теоретически является обратимым.
Но если сжатый газ расширяется при истечении через отверстие и охлаждается до своего исходного состояния, работа не восстанавливается. Процесс расширения при истечении через отверстие и процесс теплопередачи теоретически необратимы. После введения термодинамических понятий тепла и работы можно определить такие процессы, которые необратимы по самой своей природе.
Однократное и повторное использование энергии
Вероятно, наибольшие возможности для экономии энергии в промышленности заключаются в многократном использовании энергии. Жидкости, имеющие в какой-либо установке наибольшие температуры и давления, содержат также наибольшее относительное количество располагаемой работы. Поэтому их следует использовать для приведения в действие двигателей, в которых происходит расширение рабочего тела (турбин), чтобы извлечь по крайней мере часть содержащейся в рабочем теле располагаемой работы и перевести ее в механическую энергию для насосов и компрессоров или для генерирования электроэнергии. Но, вместо того чтобы отводить отработавшее рабочее тело в конденсатор, следует использовать содержащееся в нем тепло в качестве технологического тепла. В установке с совершенным энергетическим балансом не должна потребляться электроэнергия и не должен конденсироваться пар над холодной водой или в холодном воздухе.
Необходимо кратко пояснить последнее утверждение. Если установка потребляет электроэнергию, то эту электроэнергию генерирует, вероятно, конденсационная паровая турбина. Поскольку энергетическая установка производит только работу и сбрасывает тепло, ее общий к.п.д. не может быть таким же высоким, как к.п.д. установки, в которой используются и работа, и тепло. Но если технологическое оборудование потребляет больше работы, чем тепла, и не потребляет электроэнергию, то необходимо конденсировать или выпускать низконапорный пар. Когда спрос на тепло превышает спрос на работу, можно обеспечить получение дополнительного количества тепла, производя электроэнергию и поставляя ее потребителям, не способным самостоятельно ее производить. Проблема энергетического баланса между работой и теплом подробно рассматривается в гл. 3. Здесь же достаточно сделать вывод, что работу по возможности следует извлекать из источника энергии высокого уровня.
С этой точки зрения сжигание топлива только для получения тепла несовместимо с задачей сохранения работы. Кроме того, преобразование работы в тепло, как в случае электрического омического нагрева, непродуктивно, и его следует по возможности избегать.
Преобразование тепла в механическую работу, а затем в электроэнергию - наиболее очевидный пример использования тепла, но он далеко не единственный. В промышленности имеется много разнообразных операций, потребляющих энергию, хотя она и не видна в продуктах производства. Эту идею мы затронули ранее при обсуждении энтропии процесса смешения. Продукты, выходящие из сепарационного агрегата, в общем случае имеют такое же энергосодержание, как и исходное сырье, но из-за того, что они чище, их энтропия меньше. Энтропия продуктов уменьшилась из-за увеличения энтропии теплоносителя, использованного для осуществления сепарации.
Поскольку энергия, которая потребляется и выделяется в технологическом процесса, по существу, одинакова по величине, ее можно использовать повторно, но это зависит от температуры энергоносителя. Такая методика давно уже применяется при многоступенчатом выпаривании концентрированных растворов. На первой ступени тепло выделяется вследствие конденсации греющего водяного пара. Затем вторичный пар, образующийся при испарении раствора на первой ступени, используется как теплоноситель на второй ступени и т.д. (рис. 1.6). В наиболее типичных установках имеются три ступени: вначале греющий водяной пар подают при давлении, например, 137 кПа на первой ступени и на последующих ступенях образуется пар при давлении 68,7, 34,3 и 13,7 кПа. На последней ступени заданное абсолютное давление поддерживают, с помощью охлаждаемого водой конденсатора; несконденсировавшиеся газы откачивают вакуумным насосом.
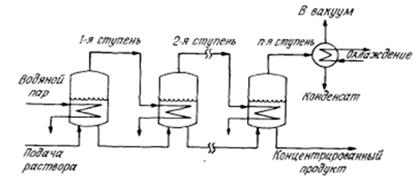
Обычно раствор бывает водным. Тогда отношение массы вторичного водяного пара к массе греющего водяного пара несколько меньше, чем число ступеней, вследствие того что потери тепла и скрытая теплота парообразования с уменьшением давления возрастают. При заданных давлении подачи греющего водяного пара и температуре охладителя число ступеней и, следовательно, преобразование греющего водяного пара во вторичной водяной пар, полученный при выпаривании раствора, определяются перепадом температуры на каждой поверхности, через которую происходит передача тепла. Если уменьшить перепады температуры, увеличив поверхности теплообмена, то можно увеличить число ступеней и, следовательно, получить большую экономичность. Но разности температур обусловлены не только потоком тепла, но Tatoce и повышением температуры точки кипения из-за наличия твердых примесей, статическим давлением и скоростным напором. Эти практические соображения определяют оптимальную поверхность теплообмена и, следовательно, число ступеней.
Если подавать греющий водяной пар при высоком давлении, то число ступеней и, следовательно, экономичность системы можно существенно увеличить. Эту процедуру нельзя продолжать бесконечно, так как многие продукты весьма чувствительны к температуре. Тем не менее при использовании водяного пара с очень высоким давлением можно предусмотреть гораздо больше ступеней выпаривания, чем при использовании водяного пара с низким давлением. Это показывает, что для получения водяного пара низкого давления путем, сжигания топлива может потребоваться значительно больше топлива, чем для получения пара высокого давления.
Если средний перепад температуры на каждой ступени составляет 18°С, то на водяном паре при давлении 137 кПа может работать ступенчатый выпарной аппарат, описанный выше. Пренебрегая потерями тепла, находим, что 1 кг водяного пара может испарить 2,88 кг воды из раствора. Если аппарат снабжается паром при давлении 962 кПа, то можно использовать семь ступеней. Тогда, пренебрегая потерями тепла, находим, что 1 кг водяного пара может испарить 6,37 кг воды из раствора. Хотя потери тепла и другие причины могут уменьшить привлекательность такого метода, приведенный пример демонстрирует ценность водяного пара высокого давления.
Применить принцип многоступенчатости к другим процессам не так просто. Параллельные дистилляционные колонны могут работать при разных давлениях, так что тепло, сбрасьюаемое одной колонной, можно повторно использовать для выпаривания в следующих колоннах. Ступенчатое использование энергии можно применять также в прямом или возвратном токе при последовательной перегонке многокомпонентной смеси. Эти примеры подробно рассматриваются в соответствующих главах книги. Здесь же сделан упор на то, что во многих общих технологических процессах энергию можно использовать повторно, и дано достаточное предварительное обоснование необходимости высокопотенциальной энергии и регулирующих устройств для координации ее многократного использования. Во всяком случае теплообмен необходимо производить при максимальной обратимости, т.е. при минимальном перепаде температур. Регулирующие устройства не должны мешать достижению этой цели.






