Влажность вторичного пара в реальных условиях может повышаться за счет выбросов более крупных капель раствора в сепарационный объем вследствие колебаний рабочего давления аппарата и неравномерной тепловой нагрузки труб нагревательной камеры. Так как на практике Нс>Нп, вторичный пар может уносить также капли, для которых справедливо неравенство wв>wp. Для отделения вторичного пара от подобных капель внутри сепарационного объема располагают различные дополнительные сапарирующие устройства разнообразных конструкций. Брызгоуловители, принцип действия которых основан на многократном резком изменении
скорости и направления потока вторичного пара, способствующем
коалесценции и осаждению капель.
Для уменьшения влажности вторичного пара горизонтальных паротрубных испарителей в паровом пространстве над зеркалом испарения целесообразно делать по меньшей мере два ряда шахматно расположенных паровых труб, служащих как для удержания капель влаги от уноса, так и для досушки получающегося вторичного пара.
Таким образом, со стороны эксплоатационного персонала для получения высококачественного дистиллата требуется поддержание заданной величины непрерывной продувки и содержание в надлежащем состоянии паросепарирующих устройств.
Вопрос 122
Каково назначение хлорирования охлаждающей воды?
Для борьбы с биологическими отложениями, приводящими к ухудшению вакдума в конденсаторах и интенсифицирующими коррозионными процессы, применяют обработку охлаждающей воды сильными окислителями – хлором и его производными, а также солями тяжелых металлов. Механизм бактерицидного действия хлора и его кислородосодержащих соединений заключается во взаимодействии с составными частями клетки микроорганизма, в первую очередь с ферментами, что ведет к нарушению обмена веществ в клетке и отмиранию микроорганизмов. В практике обработки воды применяют свободный хлор, соли хлорноватистой кислоты (гипохлориты) и диоксид хлора ClO2. При растворении хлора в воде происходит гидролиз с образованием хлорноватистой и хлороводородной кислот:
Cl2 + H2O ↔ HClO + HCl.
Равновесие этой реакции устанавливается в зависимости от значения рН воды. С повышением рН реакция смещается вправо, а при рН = 5,6 HOCl диесоциирует с образованием гипохлорита OCl-. Воздействие на бактерии HOCl в 70 – 80 раз выше, чем OCl-, поэтому ввод хлора в воду будет эффективен лишь при рН ≥ 7. Это важно, т.к. обработка окислителями обычно сочетается с другими видами ее обработки. Дозу хлора определяют по результатам пробного хлорирования с учетом заданной концентрации остаточного свободного хлора (0,3 – 0,5 мг/кг).
Часть 2
Река: Иртыш;
Тип станции: ТЭЦ;
Тип котла: барабанный;
Параметры котла:
- паропроизводительность: 50 т/ч;
- давление: 40 ата;
- температура: 460 °С.
Содержание ионов и оксидов, мг/кг:
Ca2+ = 28,1 Cl- = 34
Mg2+ = 17,0 NO 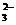 = 3,0
= 3,0
Na+ + K+ = 36,1 SiO 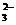 = 5,65
= 5,65
HCO3- = 165 Fe2O3 + Al2O3 = -
SO 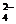 = 31,7
= 31,7
Взвешенные вещества, мг/кг: 172,4
окисляемость, мгО2/кг: 14,8
Ж0 = 2,8 мг-экв/л;
Жк = 2,7 мг-экв/л.
Жи.в. = 28,1/20,04 + 17/12,16 = 2,8 = Ж0 (мг-экв/л);
[HCO3-]и.в. = 165/61,02 = 2,7 (мг-экв/л);
Жи.в. > Щи.в...
[HCO3-]и.в. = Жк = Щи.в. = 2,7 (мг-экв/л);
Жнк. = Жи.в. - Щи.в. = 2,8 – 2,7 = 0,1 (мг-экв/л).
Минерализация:
[Cl-] + [SO 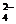 ] = 34/35,48 + 31,7/48,03 = 1,62 - маломинерализованная
] = 34/35,48 + 31,7/48,03 = 1,62 - маломинерализованная
вода.
Вода со средней жесткостью, гидрокарбонатная, кальциевая.
Предочистка:
- К – И – М -, где
К – коагуляция примесей воды в осветлителе;
И – известкование дозированной СаО;
М – фильтрация воды на механических фильтрах.
Коагуляция (сернокислым железом FeSO4 · 7H2O):
Суммарная реакция:
2FeSO4 + O2 + H2O + 8OH- → 4Fe(OH)3 ↓ + 4SO 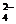
Известкование:
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
Ca(HCO3)2 + Ca(OH)2 → 2CaCO3 ↓ + 2H2O
Mg(HCO3)2 + 2Ca(OH)2 → Mg(OH)2 ↓ + 2CaCO3 ↓ + 2H2O
MgCl2 + Ca(OH)2 → Mg(OH)2 ↓ + CaCl2
MgSO4 + Ca(OH)2 → Mg(OH)2 ↓ + CaSO4.
Качество воды после предочистки:
Остаток коагулянта, мг/л Fe3+ < 0,1
Снижение окисляемости, % 40 – 50
Снижение содержания кремниевой кислоты, % 30 – 40
за счет осаждения с Mg2+
Свободная углекислота, СО2 мг/л 0
Щелочность общая, мг-экв/л, в т.ч.:
гидратная ОН-: 0,1 – 0,2 ± 0,05
карбонатная СО 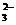 : 0,6 – 1,2
: 0,6 – 1,2
бикарбонатная НСО  : 0
: 0
рН 9,5 – 10,4
Остаточная жесткость, мг-экв/л: (0,7 – 1,3) + Ж  + Дк
+ Дк
в том числе:
общая:
некарбонатная: увеличивается на Дк
магнезиальная: снижается
Содержание взвеси, мг/л: менее 3
Солесодержание, мг/л: уменьшается, примерное конечное =
= солесодержание исходной + 19Дк –
- 50∆Щобщ. – 3,5∆Ок.
Стабильность - доумягчаемость, мг-экв/л: 0 – 0,05
Ионитная обработка воды:
- HNa – D – NaII –
HNa – фильтры HNa – катионирования в смешанном слое
D – декарбонизатор
NaII – натрий – катионитные фильтры II ступени.
- HNa –:
2NaHCO3 + H2SO4 → Na2SO4 + 2H2O + 2CO2
NaHCO3 + HCl → NaCl + H2O + CO2
– D –:
CaCO3 · MgO + 3 CO2 + 2H2O ↔ Ca(HCO3)2 + Mg(HCO3)2
– NaII –:
2R/NA+ + Ca2+ ↔ R2/Ca2+ + 2Na+
2R/Na+ + Mg2+ ↔ R2/Mg2+ + 2Na+
Показатели качества воды после ионитной обработки:
- остаточная жесткость: 0,1 мг-экв/л
- Що.в.: 0,3 – 0,4 мг-экв/л
- S (сухой остаток Na): Sн.в. + 2,69 ЖСа + 10,84Жмд.
- Sн: Sн.в. – 20,04 ЖСа – 12,16Жмд. + 61,02Жк/2
- кислотность фильтрата: Кф = Жо – Жк
- углекислота, мг/л О2: [СО2]ОС.
Качество питательной воды котлов с естественной циркуляцией должно удовлетворять следующим номам:
Общая жесткость, мкг-экв/дм3 для котлов, (не более):
- на жидком топливе: 5
- на других видах топлива: 10
Содержание соединений железа, мкг/дм3 для котлов (не более):
- на жидком топливе: 50
- на других видах топлива: 100
Содержание соединений меди в воде перед
деаэратором, мкг/дм3 для котлов (не более):
- на жидком топливе: 10
- на других видах топлива: не нормируется
Содержание растворенного кислорода в воде после
деаэратора, мкг/дм3, не более: 20
Содержание нефтепродуктов, мг/дм3, не более: 0,5
Значение рН: 8,5 – 9,5
Содержание кремниевой кислоты, мкг/дм3, не более:
- для ГРЭС и отопительных ТЭЦ: 80
- для ТЭЦ с производственным отбором пара: устанавливается теплотехническими испытаниями
C писок литературы:
1. Правила технической эксплуатации электрических станций и сетей. – М.: Энергоатомиздат, - 1989 год.
2. Громогласов А.А., Копылов А.С., Пильщиков А.П. Водоподготовка: Процессы и аппараты. – М.: Энергоатомиздат, - 1990 год.
3. Стерман Л.С., Покровский В.Н. Физические и химические методы обработки воды. – М.: Энергоатомиздат, - 1991 год.
4. Кострикин Ю.М., Мещерский Н.А., Коровина О.В. Водоподготовка и водный режим энергообъектов низкого и среднего давления. Справочник – М.: Энергоатомиздат, - 1990 год.
5. Мещерский Н.А. Эксплуатация водоподготовительных установок электростанций высокого давления. – М.: Энергоатомиздат, - 1984 год.
6. Лифшиц О.В. Справочник по водопроводке котельных установок. – М.: Энергия, - 1976 год.
7. Маргулова Т.Х., Мартынова О.И. Водные режимы тепловых и атомных электростанций. М.: Высш. шк., - 1987 год.
8. Лапотышкина Н.П., Сазонов Р.П. Водоподготовка и водно-химический режим тепловых сетей. – М.: Энергоатомиздат, - 1982 год.
9. Вихрев В.Ф., Шкроб М.С. Водоподготовка. – М.: Энергия, - 1973 год.
10. Белан Ф.И. Водоподготовка. М.: - Энергия. – 1979 год.
11. Минькина Н.Н. Физико-химические процессы в пароводяном цикле электростанций. М.: Энергия, - 1977 год.
12. Маргулова Т.Х. Химические очистки теплоэнергетического оборудования. Выпуск 2. – М.: Энергия, - 1978 год.



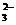 = 3,0
= 3,0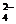 = 31,7
= 31,7 : 0
: 0 + Дк
+ Дк


