Бензопироны:
2) Кумарин – белое кристаллическое вещество со слабым запахом свежего сена. Представляет собой конденсированную гетероциклическую систему, состоящую из бензольного и α–пиронового колец. По строению кумарин является δ-лактоном кумариновой кислоты (цис–орто–гидроксикоричной кислоты). Кумарин и его гидроксипроизводные встречаются во многих лекарственных растениях: семейства зонтичных, рутовых бобовых, пасленовых, сложноцветных, конско-каштановых (например, цветки ромашки, календулы, семена конского каштана и многие другие).
У соединений, производные кумарина: эскулетин, эскулин, умбеллиферон, скополетин и другие, обнаружены спазмолитические, противоопухолевые, антикоагуляционные свойства.
Для обнаружения производных кумарина используют реакцию азосочетания, при этом образуются азокрасители, окрашенные в красно-оранжевый, малиновый, фиолетовый цвета. А также лактонную пробу, основанную на способности лактонного кольца размыкаться в щелочной среде и смыкаться в кислой среде, образующаяся орто-кумаровая кислота хорошо растворима в воде, поэтому образуется прозрачный раствор жёлтого цвета, при подкислении раствора – не растворимые в воде кумарины выпадают в осадок.
3) Хромон – конденсированная система, состоящая из бензольного и γ– пиронового колец.
3.1) Флавон и изофлавон. Производные флавона – флавоноиды, изофлавона – изофлавоноиды широко распространены в растениях, часто встречаются в виде гликозидов. Флавоны:
Кверцетин (3,3’,4’,5,7–пентагидроксифлавон) – содержится во многих фруктах, овощах и ягодах красного и багрового цвета, оливковом масле, мёде, грече, луке, чесноке. Обладает антиоксидантным, противоопухолевым, противоотёчным, спазмолитическим и противовоспалительным действием.
Лютеолин (3’,4’,5,7–тетрагидроксифлавон) – содержится в зелёном перце, ромашке, сельдерее, тимьяне, мяте, моркови, розмарине. Обладает антиоксидантным, противовоспалительным действием, препятствует возрастным изменениям в головном мозге, улучшает память.
3) Хроман – гетероциклическая система хромана лежит в основе токоферолов – витаминов группы Е (антистерильные), которые содержатся в большом количестве в зародышах пшеницы, обладают мощным антиоксидантным действием и регулируют в репродуктивную функцию. Хромановая система обнаружена также в тетрагидроканнабиноле (психотропном компоненте марихуаны).
VI. 6 ГЦ с 2 ГА

Производные пиримидин
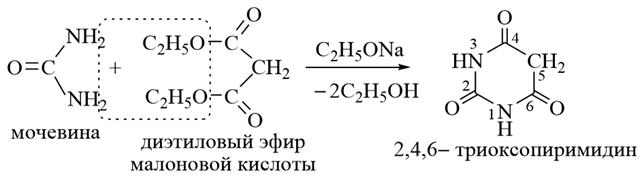
Барбитуровая кислота
2) Цитозин, урацил и тимин



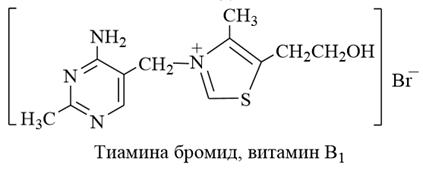
Аллоксан (2,4,5,6-тетраоксопиримидин)

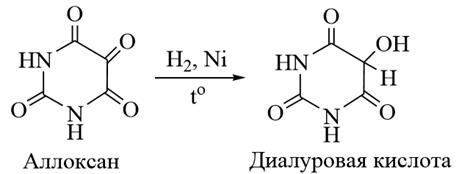
Фенотиазин и производные
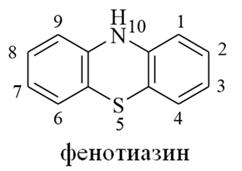
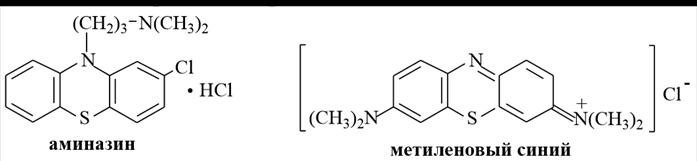
Феноксазин и производные
Пиридазин, пиримидин, пиразин и их производные – бесцветные вещества, растворимые в воде, являются ароматическими соединениями (4n+2=6, n=1). Атомы азота являются сильными электроноакцепторами по отношению друг к другу и существенно снижают реакционную способность диазинов в сравнении с пиридином. По этой же причмне, диазины – более слабые основания, чем пиридин, и образуют соли только с одним эквивалентом минеральной кислоты, то есть по одному атому азота. Значения рК ВН+: пиридазин – 2,33, пиримидин – 1,3, пиразин – 0,6.
Среди биологически значимых диазинов, важнейшими являются производные пиримидина.
1. Пиримидин – бесцветное вещество со слабым запахом; т. пл= 21оС, т. кип.=124оС, растворяется в воде. Пиримидин используют в органическом синтезе, пиримидиновое ядро входит в состав витамина В1 (тиамин), фолиевой кислоты (витамина ВС), пиримидиновых нуклеиновых оснований, барбитуровой кислоты, алкалоидов и др.
2. Фенотиазин (дибензо -1,4-тиазин) – конденсированная система, состоящая из 4Н-1,4-тиазинового и двух бензольных циклов. Фенотиазин – бесцветное кристаллическое вещество, нерастворимое в воде, диэтиловом эфире, хорошо растворимое в горячем этаноле. В настоящее время ряд производных фенотиазина используются в качестве лекарственных средств, обладающих нейролептическим действием, например, аминазин. К производным фенотиазина относится также краситель метиленовый голубой (метиленовый синий – кристаллы тёмно-зеленого цвета), который применяется для окрашивания препаратов в микробиологии, а также как антисептическое лекарственное средство.
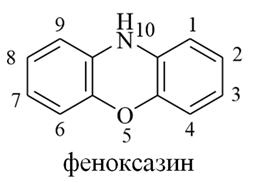
3. Феноксазин (дибензо-1,4-оксазин) – конденсированная система, состоящая из 4Н-1,4-оксазинового и двух бензольных циклов. Феноксазин – бесцветное кристаллическое вещество, нерастворимое в воде. Феноксазин является фрагментом структуры противоопухолевых антибиотиков группы актиномицина – дактиномицина (актиномицина D).
Производные пиримидина
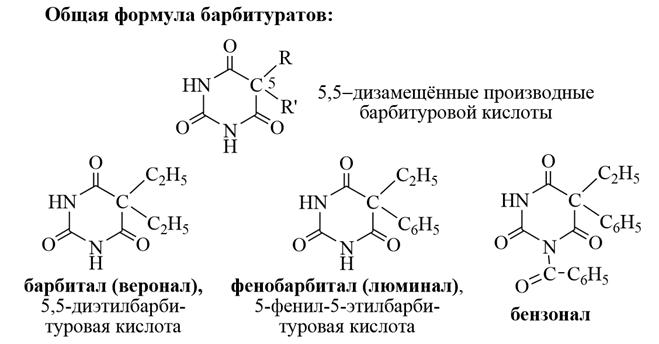
1) Барбитуровая кислота – бесцветное кристаллическое вещество, плохо растворимое в холодной воде и этаноле, хорошо растворимое в горячей воде и диэтиловом эфире.
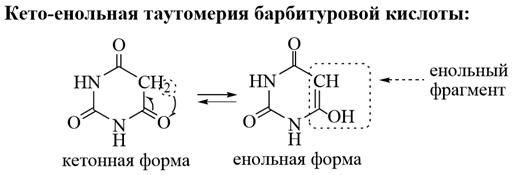
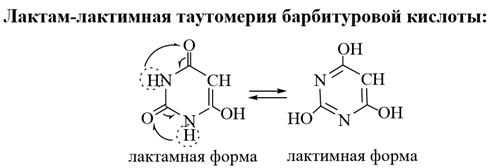
Барбитуровая кислота – таутомерное соединение, в котором проявляется два вида таутомерии: кето-енольная и лактам-лактимная.
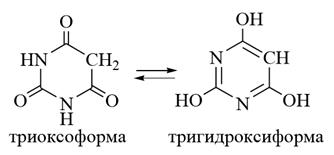
В результате совместного проявления кето–енольной и лактам–лактимной таутомерии барбитуровая кислота может существовать в виде двух таутомерных форм. Более устойчивой и преобладающей в равновесии является триоксо-форма.
Барбитуровая кислота – сильная кислота (рКа=3,9), примерно в 5,5 раз сильнее, чем уксусная. Кислотные свойства барбитуровой кислоты обусловлены подвижностью атомов водорода, особенно в енольном фрагменте. Некоторые производные барбитуровой кислоты, у которых в положении 5 находится два (реже один) углеводородных заместителя, называются барбитуратами, и применяют в медицине как снотворные и противосудорожные средства. Барбитал применяется в медицинской практике как снотворное средство, обладает наркотическим действием, вызывает привыкание – веронализм. Фенобарбитал применяется как успокаивающее, снотворное и противосудорожное (противоэпилептичекое) средство. Бензонал (1-бензолил-5фенил-5-этилбарбитуровая кислота) практически не обладает снотворным действием, но проявляет ярко выраженное противосудорожное действие, применяется в детской практике.
В молекулах барбитуратов атомы водорода при С-5 метиленовой группы СН2 замещены на радикалы, поэтому для барбитуратов характерен только один вид таутомерии: лактам–лактимной таутомерии. Барбитураты проявляют слабые NH-кислотные свойства и образуют хорошо растворимые в воде соли с одним эквивалентом щёлочи.
Мединал (барбитал-натрий) хорошо растворяется в воде и применяется как снотворное средство.
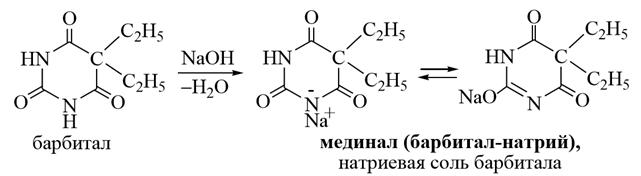
2) Цитозин, урацил и тимин – пиримидиновые нуклеиновые азотистые основания.
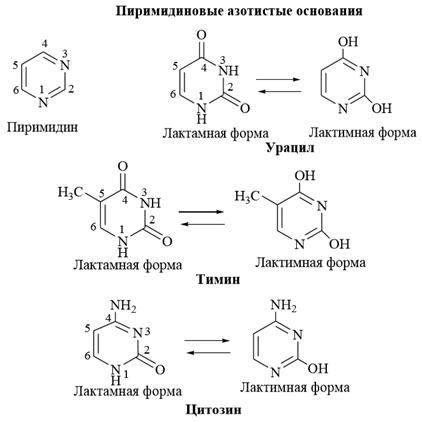
Урацил, тимин и цитозин в виде N-гликозидов рибозы или дезоксирибозы содержатся во всех клетках живых организмов, так как они входят в состав нуклеиновых кислот: РНК или ДНК. Урацил, тимин и цитозин могут существовать в виде двух таутомерных форм: лактамной и лактимной. Более устойчива лактамная форма.
Урацил входит только в РНК, тимин – в ДНК. Цитозин – универсальное основание, он может входить в ДНК и в РНК. При действии азотистой кислоты на цитозин промежуточно образуется неустойчивая соль диазония, которая тут же превращается с выделением азота в оксо-производное – урацил. В данной реакции цитозин ведёт себя как алифатический первичный амин, а не ароматический. В организме человека данная реакция приводит к замене одного нуклеинового основания другим, т.е. к изменениям в структуре нуклеиновых кислот и, следовательно, к генетическим нарушениям.
Производные урацила:
2.1) 5–бромурацил – сильный химический мутаген, применяется в генетике при точечных мутациях;
2.2) 5–фторурацил – противоопухолевое средство, выступает в роли антиметаболита, нарушающего синтез нуклеиновых кислот в опухолевой клетке;
2.3) 6–метилурацил (метилурацил, метацил) – обладает анабалической и антикатабалической активностью, применяется для заживления ран, ожогов, обладает противовоспалительным действием («Левомеколь», «Левосин», «Метилурацил»).
2.4) Пентоксил (5-гидроксиметил-6-метилурацил) – иммуностимулирующий препарат, стимулирует лейкопоэз, синтез нуклеиновых кислот, способствует клеточной регенерации и заживлентю ран.
2.5) Оротовая кислота (2,6-диоксопиримидин-4-карбоновая кислота, витамин В13) – содержится в молоке, стимулирует рост клеток, нормализует обмен веществ и деятельность печени. В медицине применяется в виде оротата калия.
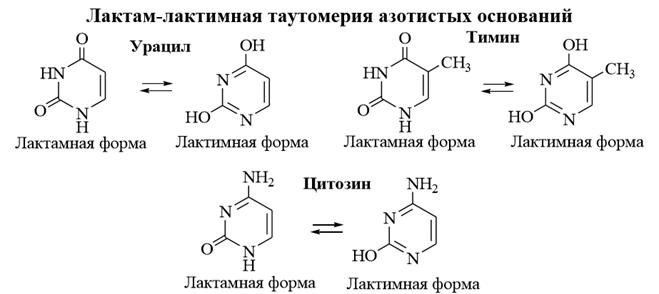
2.6) Сульфазин, сульфадимезин, сульфамонометоксин, сульфадиметоксин – сульфаниламидные препараты.
3. Тиамин (Витамин В1) содержится в чёрном хлебе, сое, фасоли, картофеле, капусте, неочищенных злаках. При недостатке в организме витамина В1 возникает заболевание Бери–бери (полиневрит, сопровождающийся параличом нижних конечностей и истощением. Витамин В1 играют важную роль в углеводном, белковом и жировом обмене, а также в процессах проведения нервного импульса в синапсах. Защищает мембраны клеток от токсического действия продуктов перекисного окисления липидов.
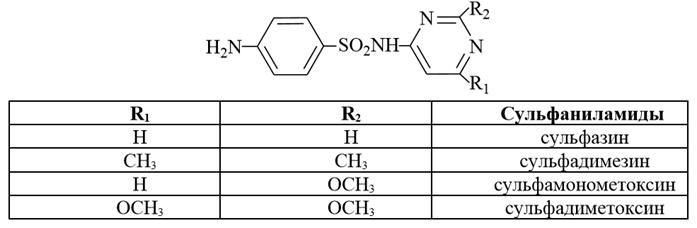
4. Аллоксан (2,4,5,6-тетраоксопиримидин) можно рассматривать как циклический уреид мезоксалевой кислоты. При восстановлении аллоксана получается диалуровая кислота. Аллоксан и диалуровая кислота являются продуктами превращения мочевой кислоты.
VII. Конденсированные ГЦ











VII. Конденсированные ГЦ
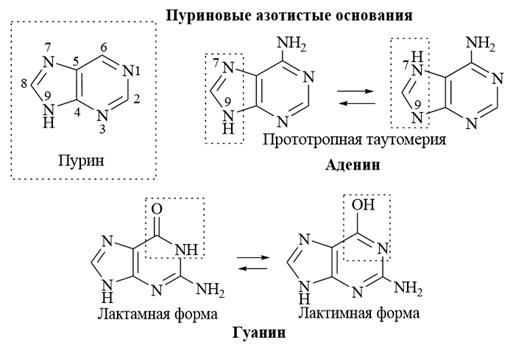
Наиболее важное значение из этой группы гетероциклов имеют широко распространённые в природе соединения пуринового ряда.
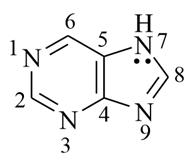
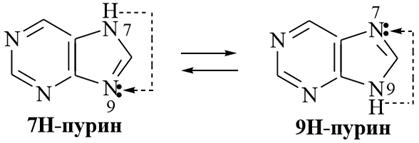
1. Пурин (имидазопиримидин) – конденсированная гетероциклическая система, состоящая из пиримидинового и имидазольного колец. Пурин является ароматическим соединением, (4n+2=10, n=2). Нумерация предложена Э. Фишером в конце 19 века, ИЮПАК признана как исключение. В свободном виде пурин в природе не встречается, но широко представлен во многих биологически активных соединениях. Пурин является амфотерным соединением и образует соли с сильными кислотами и основаниями, оснóвность пурина в 3 раза ниже (pKBH+= +2,4), чем в пиридине, а кислотность – выше, чем в феноле ≈ в 1,5 раза (pKa=8,9).
Атомы азота пиримидинового цикла вследствие электроноакцепторного влияния друг на друга минеральными кислотами не протонируются. В химическом отношении пурин представляет собой π-недостаточную систему. Для пурина не характерны реакции SE, а SN-реакции протекают легко, особенное значение из которых имеют синтезы на основе 2,6,8-трихлорпурина.
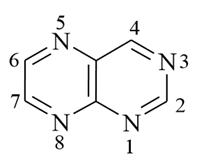
2. Птеридин (пиразинопиримидин). Молекула птеридина представляет собой конденсированную гетероциклическую систему, состоящую из пиразинового и пиримидинового циклов. Производные птеридина довольно широко распространены в природе. Впервые птеридины были выделены в 1895 г из пыльцы крыльев бабочек, что нашло отражение в названии (греч. «pter» – крыло). Птеридин – кристаллическое вещество светло–жёлтого цвета, хорошо растворимое в воде, этаноле, малорастворимое в диэтиловом эфире и бензоле (t плавл.=140оС). Птеридин является ароматическим соединением. Ядро птеридина устойчиво к действию окислителей, проявляет слабые основные свойства. Вследствие электроноакцепторного влияния четырёх атомов азота пиридинового типа электронная плотность на атомах углерода значительно понижается и соответственно ослабляется ароматический характер птеридиновой системы. Птеридин неустойчив к действию кислот и щелочей, которые в зависимости от условий вызывают раскрытие пиримидинового или пиразинового циклов, но легче расщепляется пиримидиновое кольцо. Птеридин не вступает в реакции электрофильного замещения. Как слабое основание (рКВН+= +4,12) птеридин протонируется по атому азота в положении 1.
Производные пурина
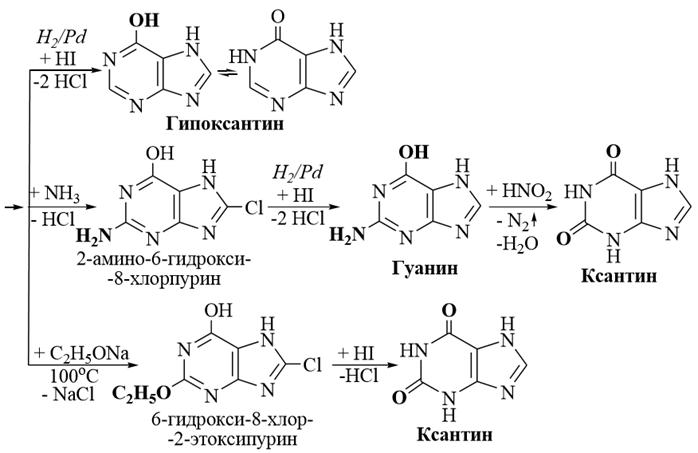
1) Аминопурины Важнейшими аминопроизводными пурина являются аденин (6–аминопурин) и гуанин (2–амино–6–гидроксипурин), входящие в состав нуклеиновых кислот в качестве пуриновых оснований. Гуанин существует в виде двух таутомерных форм – лактамной и лактимной. Наиболее устойчива лактамная форма, в виде которой гуаниновый фрагмент находится в нуклеиновых кислотах.
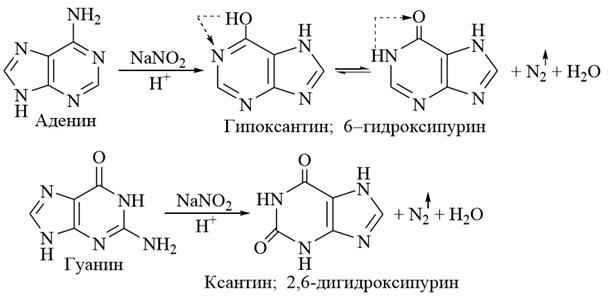
Аденин и гуанин представляют собой бесцветные кристаллические вещества, трудно растворимые в воде, хорошо растворимые в щелочах. Они образуются при гидролизе нуклеиновых кислот. В организме аденин и гуанин подвергаются дезаминированию с образованием гипоксантина и ксантина, которые далее окисляются в мочевую кислоту. Аналогично цитозину, для аденина и гуанина протекает реакция с азотистой кислотой.
Аденин входит в состав нуклеозидфосфатов, которые отвечают в организме за хранение биологической энергии (аденозинфосфаты – АТФ, АДФ, АМФ) и коферментов в окислительно-восстановительных реакциях (никотинамидадениндинуклеотиды и их фосфаты – НАД+, НАДН, НАДФ+, НАДФН; флавинадениндинуклеотиды – ФАД, ФАДH2). Гуанин и аденин используются в медицине как противоопухолевые средства, действующие по принципу антиболитов этих нуклеиновых оснований, подавляющих рост опухолевых клеток. Кроме того, аденин входит в состав ряда природных антибиотиков, противовирусных средств и др. 6-Меркаптопурин и тиогуанин подавляют рост опухолевых клеток (противоопухолевые средства), азитиоприн – иммунодепрессант, ацикловир – антигерпесный препарат.
2) Оксопурины Представителями оксопуринов являются мочевая кислота, ксантин и гипоксантин, которые образуются в организме при метаболизме нуклеиновых кислот.
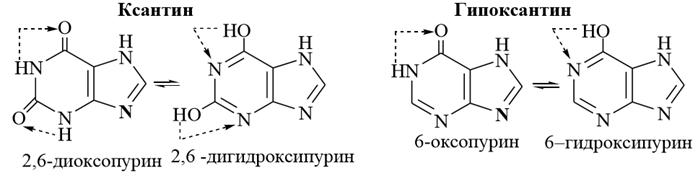
Мочевая кислота, ксантин и гипоксантин являются таутомерными соединениями. В результате лактам–лактимной таутомерии они существуют в двух таутомерных формах – оксоформе (лактамная форма) и гидроксиформе (лактимная форма). Поэтому в литературе оксопурины часто называют гидроксипуринами.
Наряду с лактам–лактимной таутомерией, у оксопуринов возможна азольная таутомерия, связанная с миграцией атома водорода между атомами азота в имидазольном цикле.
3) Гипоксантин и ксантин Гипоксантин (6–гидроксипурин) и ксантин (2,6–дигидроксипурин) по химическим свойствам напоминают мочевую кислоту. Они существуют в двух таутомерных формах – лактамной и лактимной. Подобно мочевой кислоте, эти соединения образуют соли со щелочами. Но в отличие от мочевой кислоты, гипоксантин и ксантин обладают также слабо выраженными основными свойствами (слабее пурина) и образуют соли с сильными минеральными кислотами, то есть гипоксантин и ксантин обладают амфотерным характером
Гипоксантин и ксантин широко распространены в растительном и животном мире. Большое значение в фармации имеют N–метильные производные ксантина – теофиллин, теобромин и кофеин.
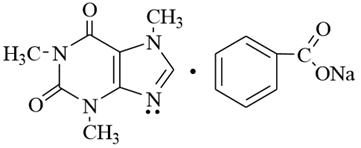
Метилированные ксантины – природные вещества, относящиеся к алкалоидам. Теофиллин содержится в листьях чая, теобромин – в бобах какао, кофеин – в листьях чая и зернах какао. Теофиллин, теобромин и кофеин получают из природного сырья или синтетически – метилированием ксантина, который в свою очередь синтезируют из более доступного и дешёвого сырья – мочевой кислоты. По физическим свойствам метилированные ксантины представляют собой бесцветные кристаллические вещества, легко растворимые в горячей воде, плохо – в холодной. Теофиллин и теобромин являются амфотерными веществами. Их кислотные свойства обусловлены подвижностью атома водорода в NH–фрагменте молекул, основные – наличием пиридинового атома N–9. Кофеин проявляет только слабые основные свойства, обусловленные наличием атома азота в положении 9. Теофиллин и теобромин применяются как сердечно-сосудистые, бронхорасширяющие и мочегонные средства. Кофеин оказывает возбуждающее действие на центральную нервную систему, повышает артериальное давление. В медицинской практике кофеин обычно применяется в виде двойной соли с бензоатом натрия – кофеин бензоата натрия.
4) Мочевая кислота – бесцветное кристаллическое вещество, плохо растворимое в воде, этаноле, диэтиловом эфире, растворимо в разбавленных растворах щелочей и глицерине. Мочевая кислота является конечным продуктом обмена пуриновых соединений в организме. Она выделяется с мочой человека в количестве 0,5–1 г в сутки. Мочевая кислота является двухосновной кислотой (рКа1=5,75; рКа2=10,3). С водными растворами щелочей она образует кислые и средние соли. Соли мочевой кислоты называют уратами.
Кислые ураты, за исключением солей лития, представляют собой мало растворимые в воде соединения. При некоторых заболеваниях, в частности, подагре они откладываются в суставах, при почечно-каменной болезни – накапливаются в почках в виде почечных камней. Основной составной частью почечных камней является мононатриевая соль мочевой кислоты. В гидроксиформе мочевая кислота вступает в реакции нуклеофильного замещения, например, с POCl3, образует 2,4,6–трихлорпурин.
Вследствие высокой подвижности атомов хлора, 2,6,8–трихлорпурин широко используется в синтезе производных пурина – аденина, гуанина, гипоксантина, ксантина и других. Активность (подвижность) атомов хлора по отношению к нуклеофильным реагентам в различных положениях пуринового ядра неодинакова и уменьшается в ряду 6 > 2 > 8, поэтому существует возможность их избирательного замещения. Ценным свойством трихлорпурина является также то, что при необходимости атом хлора может быть легко удалён восстановлением или каталитическим гидрогенолизом.
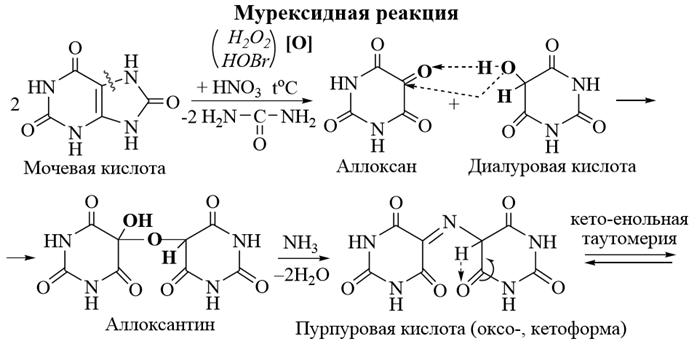
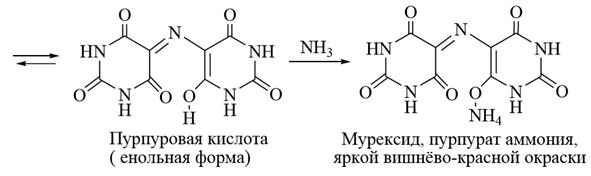
Окисление мочевой кислоты, а также ксантина и его производных лежит в основе качественного метода определения этих соединений, называемого мурексидной пробой. При действии таких окислителей, как азотная кислота, пероксид водорода или бромная вода, размыкается имидазольный цикл и образуются пиримидиновые производные аллоксан и диалуровая кислота. Эти соединения превращаются далее в своеобразный полуацеталь – аллоксантин, при обработке которого аммиаком получаются тёмно-красные кристаллы мурексида – пурпурата аммония (аммониевая соль пурпуровой кислоты в енольной форме).
Производные птеридина
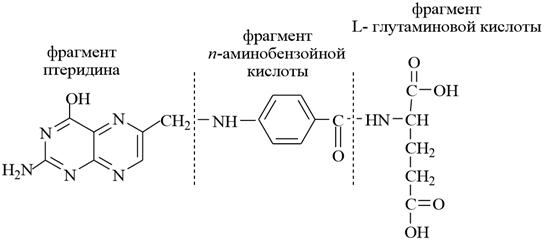
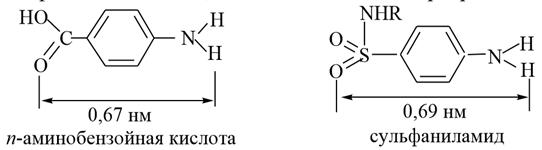
1) Фолиевая кислота (витамин ВС, витамин В9). Молекула фолиевой кислоты включает три структурных фрагмента – птеридиновое ядро, остатки пара–аминобензойной кислоты (ПАБК) и L–глутаминовой кислоты. Фолиевая кислота впервые выделена в 1938 г из экстракта печени. В большом количестве она содержится в листьях шпината, моркови и других овощах. Потребность организма в этом витамине удовлетворяется за счёт поступления с продуктами питания и синтеза микроорганизмами кишечника. Фолиевая кислота стимулирует кроветворение, биосинтез нуклеиновых кислот, белковый и углеводный обмен. Применяется в медицинской практике для лечения некоторых форм анемии.
Фолиевая кислота является стимулятором роста микроорганизмов. Бактериостатическое действие сульфаниламидных препаратов основано на нарушении биосинтеза фолиевой кислоты. Сульфаниламиды имеют структурное сходство с пара–аминобензойной кислотой, поэтому связываются с птеридиновым фрагментом вместо пара–аминобензойной кислоты. В результате блокируется последующая конденсация с глутаминовой кислотой и прекращается биосинтез фолиевой кислоты, что ведёт к гибели микроорганизмов.
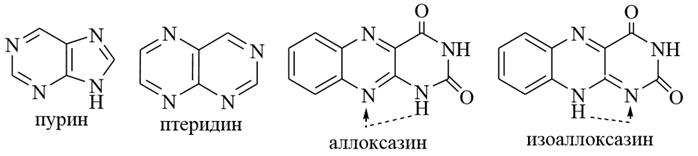
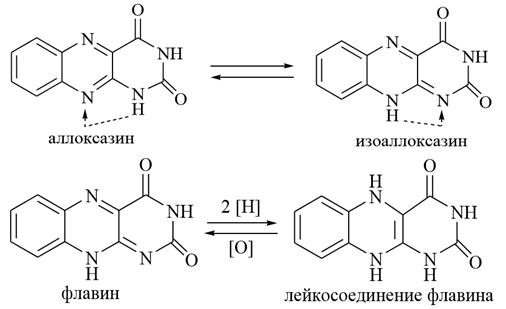
2. Аллоксазин и изоаллоксазин (флавин)
Аллоксазин представляет собой конденсированную гетероциклическую систему, состоящую из бензольного и птеридинового циклов, по сути, из трёх циклов – бензольного, пиразинового и гидрированного пиримидинового, в котором два атома углерода находятся в составе карбонильных групп. Изоаллоксазин является таутомерной формой аллоксазина, которая образуется вследствие азольной таутомерии. Изоаллоксазин имеет жёлтую окраску и поэтому называется флавином (от лат. flavus–жёлтый). Важным свойством флавина является его способность к восстановлению с образованием бесцветного соединения (лейкосоединение), которое при окислении превращается снова в исходный флавин. В процессе восстановления водород присоединяется к сопряжённой системе, включающей атомы азота в положениях 1 и 10.
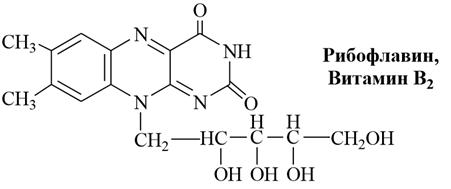
1) Рибофлавин (витамин В2) содержит ядро флавина. Название «рибофлавин» отражает наличие в молекуле остатка пятиатомного спирта рибита и флавина. Рибофлавин (7,8–диметил–10–[D–1–рибитил]–изоаллоксазин) широко распространён в природе, особенно богаты им дрожжи, бобовые, мясо, яичный желток. Его применяют при гипоавитаминозе и арибофлавинозе, для лечения ряда глазных заболеваний, при длительно незаживающих ранах, язвах, при общих нарушениях питания, при лучевой болезни, астении и других заболеваний.
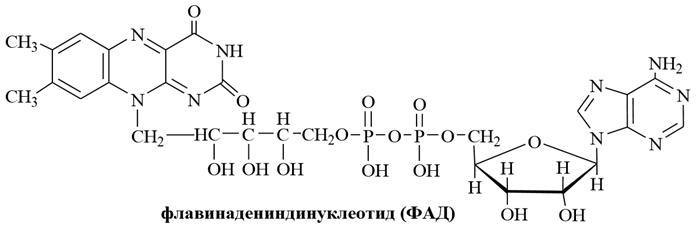
Витамин В2 входит в структуру окислительных ферментов – флавопротеидов: флавинмононуклеотида (ФМН) и флавинадениндинуклеотида (ФАД), который представляет собой эфир рибофлавина и АДФ. Эти флавиновые коферменты обычно являются простетическими группами белков. Они участвуют в окислительно-восстановительных реакциях. Эти реакции происходят в цепи дыхания.
Восстановленный кофермент ФАДН2 окисляется кислородом с образованием пероксида водорода и регенерацией кофермента ФАД. Действие этих ферментов как переносчиков водорода при окислительно–восстановительных процессах в живых организмах обусловлено способностью флавина превращаться в лейкосоединение и наоборот. Отсутствие или недостаток витамина В2 в пище вызывает задержку роста, воспаление слизистых оболочек рта, нарушение процессов нервной деятельности. Синтетический препарат выпускается для применения в лечебной практике и в качестве профилактического средства в виде поливитаминных препаратов.
Нуклеиновые кислоты












РНК: Ц-Г-У-А-Ц







ДНК: Ц-Г-Т-А-Ц
Я тоже не понял. Этой части лекции ещё не было, а в PDF такая шняга. Ждём:)
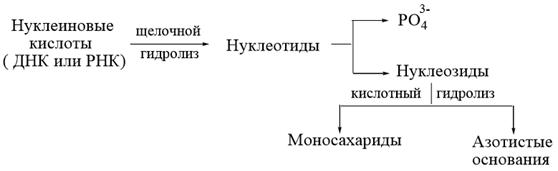
Нуклеиновые кислоты являются составной частью всех живых клеток, входят в состав вирусов. Впервые были выделены из клеточных ядер в 1869г. Позже было установлено, что нуклеиновые кислоты представляют собой высокомолекулярные соединения, в макромолекулы которых входят производные пиримидина и пурина, фосфорная кислота и моносахарид – рибоза или дезоксирибоза.
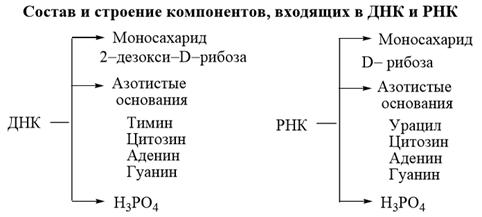
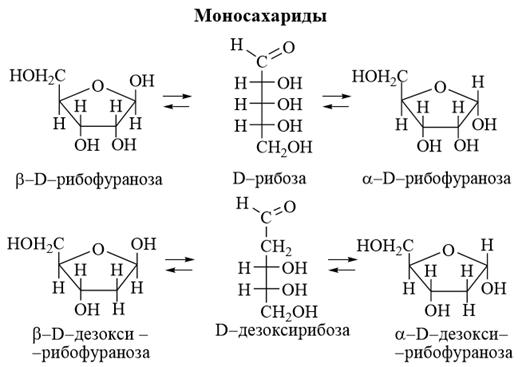
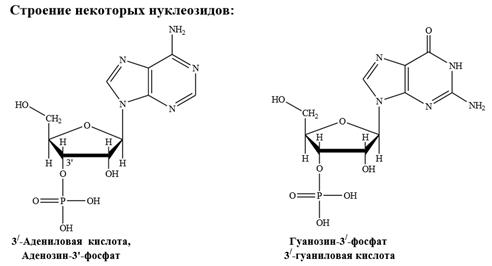
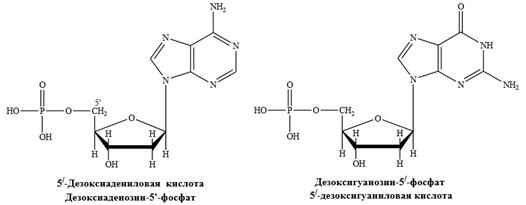
В результате гидролиза РНК в зависимости от условий получают соединения производных пиримидина или пурина с рибозой и фосфорной кислотой – нуклеотиды, или соединения производных пиримидина или пурина с рибозой – нуклеозиды. Конечными продуктами гидролиза являются урацил, цитозин, аденин и гуанин, D- рибоза и фосфорная кислота. В результате гидролиза ДНК соответственно получаются дезоксирибонуклеотиды, дезоксирибонуклеозиды и, в конечном итоге, тимин, аденин, гуанин, D-дезоксирибоза и фосфорная кислота. Нуклеиновые кислоты играют исключительную роль в жизненных процессах живых организмов. Они являются, с одной стороны, носителем генетической информации, с другой стороны, матрицей, на которой синтезируются специфические белки и нуклеиновые кислоты. В состав нуклеиновых кислот D–рибоза и D–дезоксирибоза входят в виде β–аномеров.
1. Азотистые основания В состав нуклеиновых кислот входят нуклеиновые основания – гетероциклические соединения пиримидинового и пуринового рядов, содержащие в качестве заместителей в гетероциклическом ядре оксо– (урацил, тимин), или аминогруппу (аденин), или обе эти группы одновременно (цитозин, гуанин). Гидрокси– и аминопроизводные гетероциклического ряда способны к лактим–лактамной и амино–иминной таутомерии соответственно. Но при физиологических условиях в живом организме нуклеиновые основания существуют только в лактамной и аминной формах. В лактамной (оксо–форме) гетероциклы так же сохраняют ароматический характер и имеют плоское строение. Ароматичность гетероциклов лежит в основе их относительно высокой термодинамической устойчивости.
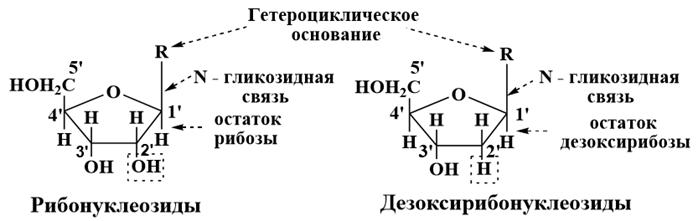
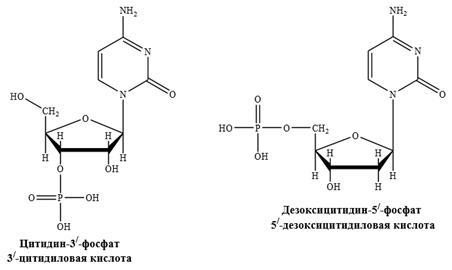
2. Нуклеозиды представляют собой соединения гидрокси- или аминопроизводных пиримидина или пурина с рибозой или дезоксирибозой, в которых осуществляется связь C-N между углеродным атомом С-1 моносахарида и соответствующим атомом азота гетероцикла, при этом остаток гетероцикла находится в β-положении цикла фуранозы (N-гликозиды). В зависимости от природы углеводного остатка различают рибонуклеозиды и дезоксирибонуклеозиды.
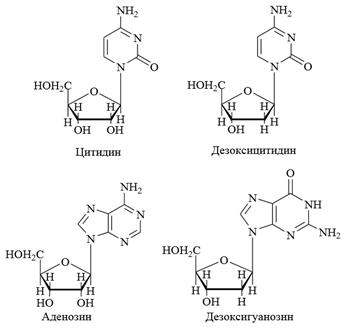
Названия нуклеозидов наиболее часто производят от тривиального названия соответствующего нуклеинового основания с суффиксами -идин у пиримидиновых и -озин у пуриновых нуклеозидов. Цитозин + Рибоза = Цитидин; Цитозин + Дезоксирибоза = Дезоксицитидин; Аденин + рибоза = Аденозин; Аденин + Дезоксирибоза = Дезоксиаденозин. Исключение: тимидин (а не дезокситимидин), используемое для дезоксирибозида тимина, входящего в состав ДНК.
Нуклеозиды представляют собой бесцветные кристаллические водорастворимые вещества, обладающие химическими свойствами соответствующего гетероциклического соединения и сахара (рибозы или дезоксирибозы). Являясь N–гликозидами, нуклеозиды устойчивы к гидролизу в слабощелочной среде, но расщепляются в кислой среде. Пуриновые нуклеозиды гидролизуются легко, пиримидиновые гидролизуются труднее.
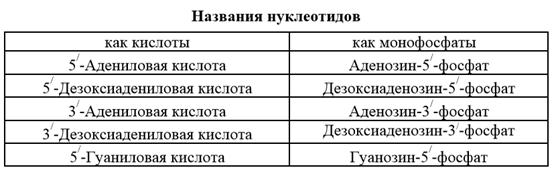
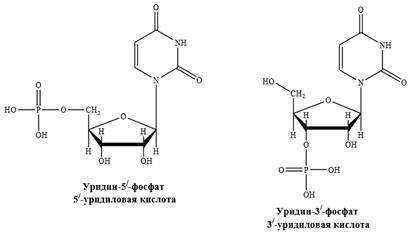
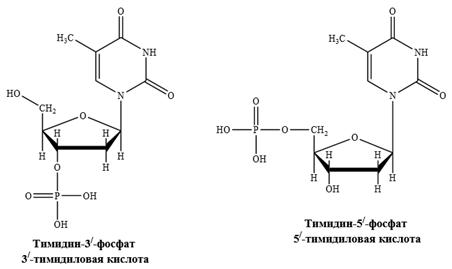
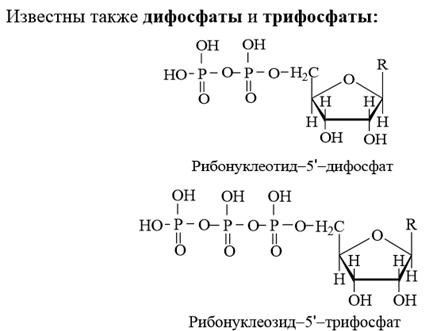
3. Нуклеотиды являются сложными эфирами нуклеозидов и фосфорной кислоты − нуклеозидфосфата. Обычно этерифицирована гидроксильная группа рибозы или дезоксирибозы в положении 3/- или 5/-. Нуклеотиды называют или как соответствующие кислоты, или как соли – монофосфаты с указанием в обоих случаях положения фосфатного остатка.
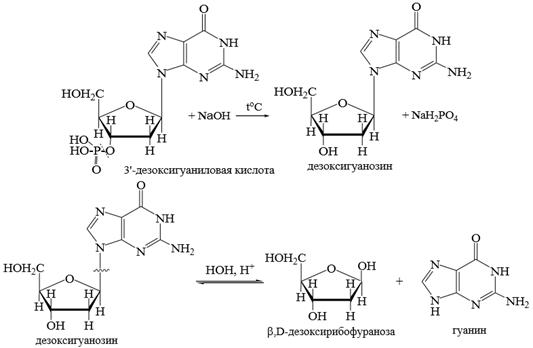
Гидролиз нуклеотидов. Сложноэфирная связь гидролизуется в кислой и щелочной среде. N–гликозидная связь в нуклеотидах устойчива к гидролизу в слабощелочной среде, но расщепляется в кислой. Пуриновые нуклеозиды гидролизуются легко, пиримидиновые гидролизуются труднее. Чтобы из нуклеотида получить нуклеозид, нужно разорвать сложноэфирную связь, т.е. провести гидролиз только в щелочной среде. В кислой среде образующийся нуклеозид сразу же будет гидролизоваться до соответствующего сахара и азотистого основания.
Нуклеотиды являются составными частями нуклеиновых кислот и некоторых ферментов. Многие нуклеотиды обладают физиологической активностью. Они участвуют в биохимических процессах, и особенно важны в роли коферментов, т.е. веществ, тесно связанных с ферментами и необходимых для проявления ферментативной активности.
3.1) Уридин-5’-монофосфорная кислота – бесцветное кристаллическое вещество с т. пл.=202°С, хорошо растворяется в воде. Является кислотой (рКа=6,4), вследствие ионизации связи O−H остатка фосфорной кислоты, образует соли. Характерны свойства урацила и рибозы. Соединение содержится в живых организмах, как в свободном состоянии, так и в составе нуклеиновых кислот.
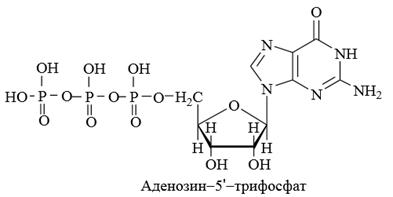
3.2) Аденозин-5’-трифосфорная кислота (аденозинтрифосфат, АТФ) – бесцветное кристаллическое вещество, хорошо растворяется в воде, образует стабильные соли. Трифосфатная группа содержит две ангидридные связи (PO-P), называемые макроэргическими, которые легко гидролизуются, при этом выделяется значительное количество энергии (33-46 кДж/моль). Основная функция АТФ заключается в хранении энергии.
АТФ играет важную роль в процессах обмена веществ в живых организмах. Она является своеобразным аккумулятором энергии, поставщиком химической энергии в различных процессах биосинтеза и в таких физиологических процессах, как сокращение мышц.
3.3) НАД+ - никотинамидадениндинуклеотид и его фосфат НАДФ+ – является одним из наиболее общих окисляющих агентов в природных системах. Функция НАД+ и НАДФ+ как окисляющих агентов формально состоит в отщеплении Н+ от органических соединений частью молекулы содержащим пиридиновый фрагмент.
4. Полинуклеотиды и нуклеиновые кислоты Динуклеотиды, тринуклеотиды, полинуклеотиды образуются при использовании фосфатной связи C-O-P. Нуклеиновые кислоты являются полинуклеотидами, в которых остатки нуклеотидов связаны между собой 3’-5’-фосфатной связью С-О-Р-О-С. Нуклеиновые кислоты – фосфорсодержащие биополимеры, которые построены из остатков нуклеозидов (N−гликозидов рибозы и дезоксирибозы и производных пиримидина или пурина), связанных между собой фосфодиэфирными связями.
ФРАГМЕНТ МОЛЕКУЛЫ РНК. Нуклеиновые кислоты, как и белки, очень разнообразны, соответственно различны и их специфические функции в организме. Молекулярные массы нуклеиновых кислот также различны – от нескольких тысяч до миллиардов (остатков нуклеозидов от 10 до 106). Первичная структура нуклеиновых кислот определяется последовательностью расположения нуклеозидов, связанных фосфодиэфирной связью, или просто последовательностью производных пиримидина или пурина. Обычно это относится к урацилу (У), тимину (Т), цитозину (Ц), аденину (А), гуанину (Г). Другие соединения встречаются очень редко. Первичная структура схематично изображается совокупностью букв, например: ЦфГфУфАф…. («ф» -остаток фосфорной кислоты). Он ставится слева от обозначения нуклеозида, если у него этерифицирован углеводный остаток по С-5’, и справа, если он этерифицирован по С-3’. Иногда букву “ф” упускают и заменяют её чёрточкой, тогда приведённый выше фрагмент цепи РНК можно записать так: Ц-Г-У-А-Ц.
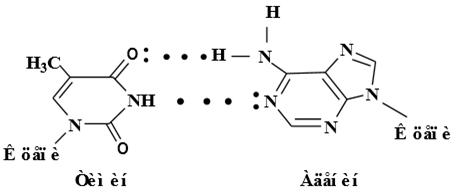
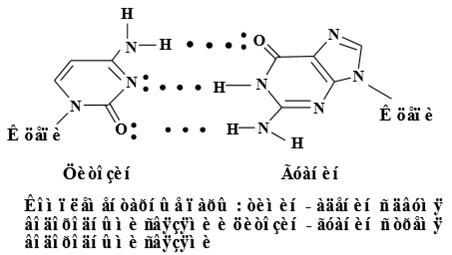
ФРАГМЕНТ МОЛЕКУЛЫ ДНК Вторичная структура нуклеиновых кислот представляет собой пространственное расположение макромолекул. Это определяется внутримолекулярным и межмолекулярным взаимодействием, главным образом посредством водородных связей. Известны различные вторичные структуры. Встречаются одноцепочные (однонитевые) нуклеиновые кислоты, цепь которых может принимать различные пространственные формы, в том числе спиралеобразные, в которых плоские молекулы производных пиримидина и пурина, как правило, расположены одна над другой в виде стопки, расстояние между плоскостями около 0,34 нм. Основу молекулы нуклеиновых кислот составляет полиэфир фосфорной кислоты и рибозы или дезоксирибозы. К этой макромолекуле присоединены производные пурина и пиримидина. Но именно при помощи этих пиримидиновых и пуриновых остатков осуществляются внутримолекулярные и межмолекулярные взаимодействия, которые обусловливают все функции нуклеиновых кислот в живом организме. Для многих ДНК характерно существование в виде комплексов, образующихся из двух полинуклеотидных цепей, которые стабилизируются водородными связями. Такие нуклеиновые кислоты называют двухцепочными (двухнитевыми). Как показали на основе рентгеноструктурного анализа и химических данных Д. Уотсон и Ф. Крик (1953 г.), двухцепочные нуклеиновые кислоты образуют в пространстве структуру двойной спирали. Две макромолекулы нуклеиновых кислот закручены в спирали, при этом спирали находятся одна в другой и связаны между собой посредством водородных связей, которые образуются между пиримидиновыми и пуриновыми остатками. Спираль образует полиэфир фосфорной кислоты, а плоские молекулы производных пурина и пиримидина находятся внутри спирали, образуя её сердцевину. В полный виток каждой спирали укладывается около 10 нуклеотидных единиц и две цепи выстраиваются в противоположных направлениях так, чтобы могло произойти спаривание оснований. Две цепи образуют комплементарную (дополняющую одна другую пару), причём остаток тимина в одной цепи всегда спарен с остатком аденина в другой цепи, а остаток цитозина с остатком гуанина. Это подтверждается опытами по гидролизу, которые показывают, что в ДНК соотношение тимин: аденин равно 1:1; цитозин: гуанин равно 1:1. Специфическое спаривание соответствующих оснований осуществляется с помощью водородных связей.
Если раздвинуть две связанные водородными связями цепи молекулы ДНК, то на каждой образовавшейся половине может быть точно дополняющая её цепь с заданной последовательностью нуклеотидов. Т.е. вместо одной молекулы ДНК образуются две, в точности идентичные исходной. Такой процесс самоудвоения молекул ДНК называется репликацией.
Биологическая функция ДНК в жив























































































